Дефосфорилирование глюкозо-б-фосфата.
Образование фруктозо-6-фосфата.
Следующая необратимая реакция гликолиза, катализируемая фосфофруктокиназой-образование из фруктозо-6-фосфата фруктозо-1,6-дифосфата с потреблением одной молекулы АТФ. Биосинтез глюкозы идет в обход этой реакции, что достигается при участии фермента фруктозодифосфатазы,осуществляющего необратимое отщепление фосфатной группы от первого углеродного атома фруктозо-1,6-дифосфата:
Фруктозо-1,6-дифосфат + НгО -> Фруктозо-6-фосфат + Фн.
Далее на обратимой стадии глюконеогенеза фруктозо-6-фосфат превращается при участии фермента фосфогексоизомеразы в глюкозо-6-фосфат. В большинстве клеток организма образующийся в процессе глюконеогенеза глюкозо-6-фосфат используется как предшественник резервных полисахаридов, дисахаридов и моносахаридов (кроме глюкозы), и только в печени и корковом веществе почек глюкозо-6-фосфат может дефосфорилироваться с образованием свободной глюкозы. Расщепление до свободной глюкозы невозможно путем обращения гексокиназной реакции гликолиза.
В организме свободная глюкоза образуется в цитозоле при участии глюкозо-6-фосфатазы— фермента эндоплазматической сети клеток печени и почек:
глюкозо-6-фосфат + НгО -> глюкоза + Pi.
Таким образом, на образование каждой молекулы глюкозы расходуется шесть макроэр-гических фосфатных связей, две молекулы НАДН используются в качестве восстановителей. Процесс протекает с выделением энергии, тогда как в случае превращения глюкозы в пируват при гликолизе образуется только две молекулы АТФ. То есть избыточная «цена» глюконеогенеза равна четырем высокоэнергетическим связям в расчете на одну молекулу глюкозы, синтезируемой из пирувата.
Наиболее интенсивно обмен глюкозы протекает в печени, и только там могут одновременно протекать два противоположно направленных процесса — гликолизи глюконеогенез.
Переключение печени с гликолиза на глюконеогенез и наоборот происходит с участием инсулина и глюкагона и осуществляется с помощью:
— ковалентной модификации ферментов путем фосфорилирования/дефосфорилирования;
— индукции/репрессии синтеза ключевых ферментов, катализирующих реакции субстратных циклов.
Регулируются необратимые стадии гликолиза и глюконеогенеза. Запуск реакций гликолиза регулируется главным образом концентрацией глюкозы в крови. При пищеварении концентрация глюкозы в крови повышается. Активность глюкокиназы в этих условиях максимальна. Вследствие этого ускоряется гликолитическая реакция фосфор ил ирования глюкозы.Кроме того, повысившаяся в это время концентрация инсулина индуцирует синтез глюкокиназы и ускоряет тем самым фосфорилирование глюкозы. Основная часть глюкозо-6-фосфата направляется по гликолитическому пути.
Следующий регуляторный фермент гликолиза — фосфофруктокиназа аллостерически активируется концентрацией фруктозо-2,6-дифосфата (Ф-2,6-ДФ),который уменьшает ин-гибирующее действие АТФ на фосфофруктокиназу и ингибирует фруктозо-1,6-дифосфатазу (фермент глюконеогенеза). Ф-2,6-ДФ образуется путем фосфорилирования фруктозо-6-фосфата, катализируется бифункциональным ферментом (БИФ)и требует затрат АТФ.
При высоком инсулин-глюкагоновом индексе в период пищеварения активность БИФ высокая, количество Ф-2,6-ДФ увеличивается и гликолиз активируется.
При низком инсулин-глюкагоновом индексе, характерном для периода длительного голодания, активность БИФ низкая, количество Ф-2,6-ДФ снижается, происходит замедление гликолиза и переключение на глюконеогенез.
В регуляции третьей необратимой реакции гликолиза основная роль принадлежит пируваткиназе, фосфорилированная форма которой неактивна, а дефосфорилированная — активна. В период пищеварения инсулин активирует протеинфосфатазу, которая дефосфорили-рует пируваткиназу, переводя ее в активное состояние. Следовательно, гликолитическая реакция фосфоенолпируват —» пируват ускоряется при пищеварении и замедляется в постаб-сорбтивном состоянии.
Дата добавления: 2015-07-13 ; Просмотров: 801 ; Нарушение авторских прав? ;
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
источник
Гликолиз регулируется двумя основными путями:
1. Аллостерическая регуляция : период действия кратковременный — от нескольких минут до часов. Осуществляется с помощью аллостерических регуляторов — молекул, связывающихся с ферментами гликолиза и активирующих/выключающих их (регуляторы указаны выше в разделе 2.7).
2. Гормональная регуляция : период действия как кратковременный, так и длительный — от нескольких часов до нескольких дней. Гормоны, связываясь с рецепторами, вызывают фосфорилирование/дефосфорилирование ключевых регуляторных ферментов, а также повышают частоту транскрипции и трансляции этих же ферментов гликолиза. Таким образом достигается 10–20-кратное увеличение скорости реакций.
Регуляция гликолиза и глюконеогенеза взаимосвязана. Особенности этой связи будут рассмотрены ниже.
А Аллостерическая регуляция
В аллостерической регуляции участвуют три фермента гликолиза: гексокиназа , фосфофруктокиназа и пируваткиназа . Это наглядно подтверждается данными об из-
менении свободной энергии в реакциях гликолиза — значение G для 1-й, 3-й и 10-й реакций имеет отрицательное значение (реакции экзергонические). Все остальные реакции находятся в термодинамическом равновесии. Скорость этих реакций очень высока, поэтому они едва ли могут ограничивать скорость гликолиза в целом.
Гексокиназа аллостерически ингибируется продуктом своей же реакции — глюкозо-6-фосфатом, а активируется субстратом — глюкозой. Регуляция гексикиназы связана с регуляцией фосфофруктокиназы: если фосфофруктокиназа ингибирована, накапливается её субстрат — фруктозо-6-фосфат, который быстро превращается в глюкозо-6-фосфат в ходе обратной реакции с помощью фосфоглюкоизомеразы. Однако это не относится к печёночному изоферменту глюкокиназе , который имеет меньшее сродство к глюкозе и не ингибируется глюкозо-6-фосфатом.
Фосфофруктокиназа является важнейшим регуляторным ферментом гликолиза. Мышечная фосфофруктокиназа аллостерически ингибируется высокими концентрациями АТФ, который связывается с регуляторным сайтом, расположенным вне активного центра, и снижает сродство фермента к субстрату — фруктозо-6-фос- фату. В результате скорость реакции падает. АМФ оказывает обратное действие, повышая сродство фосфофруктокиназы к субстрату. Таким образом, скорость реакции (и гликолиза в целом) повышается. Об энергетическом обеспечении клетки позволяет судить показатель АТФ/АМФ. Такая регуляция фосфофруктокиназы логична, поскольку, если АТФ в клетке достаточно, то абсолютно незачем тратить всю глюкозу на его избыток, когда можно израсходовать эту глюкозу в других метаболических пу-
тях или запасти в клетке. Иными словами, гликолиз ускоряется, когда в клетке мало энергии, и замедляется, когда её много. Всё вышесказанное характерно и для печёночной фосфофруктокиназы. Однако она имеет и некоторые свои особенности: ингибируется цитратом (цитрат участвует в биосинтезе жирных кислот, повышение его концентрации говорит о достаточном количестве энергии в клетке) и активируется фруктозо-2,6-бисфосфатом , важным аллостерическим регулятором (см. ниже).
Пируваткиназа катализирует последнюю реакцию аэробного гликолиза. Мышечный изотип этого фермента ингибируется АТФ, ацетил-КоА и аланином, а активируется фруктозо-1,6-бисфосфатом и фосфоенолпируватом. Печёночная пируваткиназа дополнительно ингибируется путем фосфорилирования под действием глюкагона. Биохимический смысл этой реакции в том, чтобы снизить потребление глюкозы печенью в период голодания, когда глюкоза нужна мышцам и нервным клеткам.
Инсулин . Печень является основным эффекторным органом панкреатических гормонов. Инсулин оказывает множественное действие на печень: он активирует гликолиз, синтез гликогена, жирных кислот и белка, ингибирует глюконеогенез, а
Введение в обмен углеводов
также распад перечисленных выше соединений. Инсулин активирует транскрипцию генов глюкокиназы, фосфофруктокиназы, пируваткиназы и бифункционального фермента в печени. Кроме того, инсулин активирует ферменты фосфофруктокиназу 1 и пируваткиназу, ускоряя при этом весь гликолиз в целом.
Активация фосфофруктокиназы требует запуска сложного сигнального каскада. Этапы этого процесса приведены ниже:
1. Инсулин связывается с рецептором IR на поверхности мембраны гепатоцита и запускает сигнальный каскад.
2. Результатом сигнального каскада является дефосфорилирование ферментом протеинфосфатазой другого ключевого фермента — бифункционального фермента (БИФ). Кроме этого, происходит дефосфорилирование пируваткиназы.
3. БИФ представляет собой гомодимерный белок массой
100 кДа. Этот белок содержит 2 активных центра, которые имеют отдельные наименования: фосфофруктокиназа-2 (синтезирует фруктозо-2,6-бисфосфат) и фруктозобисфосфатаза-2 (расщепляет фруктозо-2,6-бисфосфат). Фруктозо-2,6-бисфосфат — важный аллостерический активатор фермента гликолиза фосфофруктокиназы.
4. Инсулин вызывает дефосфорилирование БИФ и, следовательно, ингибирование фруктозо-2,6-бисфосфатазы-2. Активируется фосфофрукто- киназа-2, которая синтезирует фруктозо-2,6-бисфосфат.
5. Фруктозо-2,6-бисфосфат (не метаболит гликолиза) аллостерически ак-
тивирует фосфофруктокиназу, фермент гликолиза.
Глюкагон оказывает противоположное инсулину действие. Он стимулирует захват печенью аминокислот, активирует глюконеогенез, ингибирует гликолиз и биосинтез жирных кислот. Глюкагон ингибирует транскрипцию трех регулируемых ферментов гликолиза и активирует продукцию двух ферментов глюконеогенеза.
Сигнальный каскад, запускаемый глюкагоном, приводит к фосфорилированию пируваткиназы и БИФ и, следовательно, к активации фруктозобисфосфатазы и ингибированию фосфофруктокиназы-2. Фруктозобисфосфатаза расщепляет фруктозо- 2,6-бисфосфат, в результате чего снижается скорость гликолиза и запускается глюконеогенез (см. Тему 3).
Адреналин ингибирует гликолиз в печени, подобно глюкагону. Однако он оказывает слабовыраженное активирующее действие на гликолиз в мышцах. Кроме этого, адреналин активирует распад жиров (липолиз), гликогена и глюконеогенез.
Кортизол ингибирует гликолиз и активирует катаболические процессы в организме: распад гликогена, жиров, белков.
1 Фосфофруктокиназа (или фосфофруктокиназа-1) — это фермент гликолиза, фосфорилирующий фруктозо-6-фосфат до фруктозо-1,6-бисфосфата. Не следует путать с фосфофруктокиназой-2, которая не является ферментом гликолиза, а лишь участвует в синтезе регуляторной молекулы — ф руктозо-2,6-бисфосфата .
источник
Из крови в клетки тканей глюкоза поступает по механизму облегчённой диффузии с участием белков-переносчиков. Исключение составляют клетки мышц и жировой ткани, где облегчённая диффузия регулируется инсулином (гормон поджелудочной железы). В отсутствие инсулина плазматическая мембрана этих клеток непроницаема для глюкозы, так как она не содержит белки-переносчики (транспортёры) глюкозы.
Глюкозные транспортёры (ГЛЮТ) обнаружены во всех тканях.
Локализация в органах
Преимущественно в мозге, плаценте, почках, толстом кишечнике
Преимущественно в печени, почках, β-клетках островков Лангерханса, энтероцитах
Во многих тканях, включая мозг, плаценту, почки
В мышцах (скелетной, сердечной), жировой ткани
Содержится в отсутствие инсулина почти полностью в цитоплазме
В тонком кишечнике. Возможно, является переносчиком фруктозы.
Описанные 5 типов ГЛЮТ имеют сходные первичную структуру и доменную организацию.
ГЛЮТ-1 обеспечивает стабильный поток глюкозы в мозг;
ГЛЮТ-2 обнаружен в клетках органов, выделяющих глюкозу в кровь. Именно при участии ГЛЮТ-2 глюкоза переходит в кровь из энтероцитов и печени. ГЛЮТ-2 участвует в транспорте глюкозы в β-клетки поджелудочной железы;
ГЛЮТ-3 обладает большим, чем ГЛЮТ-1, сродством к глюкозе. Он также обеспечивает постоянный приток глюкозы к клеткам нервной и других тканей;
ГЛЮТ-4 — главный переносчик глюкозы в клетки мышц и жировой ткани;
ГЛЮТ-5 встречается, главным образом, в клетках тонкого кишечника. Его функции известны недостаточно.
Все типы ГЛЮТ могут находиться как в плазматической мембране, так и в мембранных везикулах в цитоплазме. Однако только ГЛЮТ-4, локализованный в везикулах цитоплазмы, встраивается в плазматическую мембрану клеток мышечной и жировой ткани при участии гормона поджелудочной железы инсулина. В связи с тем, что поступление глюкозы в мышцы и жировую ткань зависит от инсулина, эти ткани называются инсулинзависимыми.
Влияние инсулина на перемещение транспортёров глюкозы из цитоплазмы в плазматическую мембрану.
1 — связывание инсулина с рецептором; 2 — участок инсулинового рецептора, обращённый внутрь клетки, стимулирует перемещение транспортёров глюкозы; 3, 4 — транспортёры в составе содержащих их везикул перемещаются к плазматической мембране клетки, включаются в её состав и переносят глюкозу в клетку.
Известны различные нарушения в работе транспортёров глюкозы. Наследственный дефект этих белков может лежать в основе инсулинонезависимого сахарного диабета. Нарушения функции ГЛЮТ-4 возможны на следующих этапах:
передача сигнала инсулина о перемещении этого транспортёра к мембране;
источник
По сравнению с другими органами печень отличается наиболее сложным обменом глюкозы. Кроме пары противоположных процессов (синтеза и распада гликогена), в печени могут происходить ещё два противоположно направленных процесса — гликолиз и глюконеогенез. В большинстве других органов происходит только гликолиз. Переключение печени с гликолиза на глюконеогенез и обратно происходит с участием инсулина и глюкагона и осуществляется с помощью:
• аллостерической регуляции активности ферментов;
• ковалентной модификации ферментов путём фосфорилирования/дефосфорилирования;
• индукции/репрессии синтеза ключевых ферментов.
Регуляторные воздействия направлены на ферменты, катализирующие необратимые стадии гликолиза и глюконеогенеза, сочетание которых называют «субстратными», или «холостыми» циклами.
А. Регуляция скорости реакций гликолиза и глюконеогенеза, составляющих субстратные циклы
«Субстратные» циклы — парные комбинации процессов синтеза и распада метаболитов. Как уже упоминалось, сочетание процессов синтеза и распада гликогена или необратимых реакций гликолиза и соответствующих им необратимых реакций глюконеогенеза может составить подобный цикл. Название «субстратный цикл» означает объединение реакций синтеза и распада субстрата. Название «холостой» отражает результат работы подобного цикла, заключающийся в бесполезном расходовании АТФ. Хотя существование «холостых» циклов нелогично, тем не менее они могут функционировать. Более того, эти циклы могут быть мишенью регуляторных воздействий, так как составляющие их реакции катализируют разные ферменты. Реципрокное изменение активности этих ферментов предотвращает одновременное протекание противоположных процессов.
Изменение в печени гликолитического направления на глюконеогенез и обратно при смене абсорбтивного состояния на постабсорбтивное или при голодании происходит главным образом в результате регуляции активности ферментов, катализирующих реакции субстратных циклов. Эти циклы обозначены цифрами I, II, III на рис. 7-54, представляющем общую картину регуляции гликолиза и глюконеогенеза в печени.
Рис. 7-54. Регуляция метаболизма глюкозы в печени. БИФ — бифункциональный фермент (фруктозо-2,6-бисфосфатаза/фосфофруктокиназа-2); БИФ-ОН — дефосфорилированный фермент; БИФ-Р — фосфорилированный фермент, ПДК-ОН — дефосфорилированный пируватдегидрогеназный комплекс; ПК-ОН — дефосфорилированная пируваткиназа; ГАФ — глицеральдегидфосфат; ДАФ — дигидроксиацетонфосфат, ФЕП — фосфоенолпируват. I-III — субстратные циклы: в рамках — регуляторные ферменты глиполиза и глюконеогенеза.
Направление реакции первого субстратного цикла регулируется главным образом концентрацией глюкозы. При пищеварении концентрация глюкозы в крови повышается (до 8— 10 ммоль/л). Активность глюкокиназы в этих условиях максимальна. Вследствие этого ускоряется гликолитическая реакция образования глюкозо-6-фосфата. Кроме того, инсулин индуцирует синтез глюкокиназы и ускоряет тем самым фосфорилирование глюкозы. Поскольку глюкокиназа печени не ингибируется глюкозо-6-фосфатом (в отличие от гексокиназы мышц), то основная часть глюкозо-6-фосфата в абсорбтивном периоде направляется на синтез гликогена и по гликолитическому пути.
Направление реакций второго субстратного цикла зависит от активности фосфофруктокиназы и фосфатазы фруктозо-1,6-бисфосфата. Активность этих ферментов зависит от концентрации фруктозо-2,6-бисфосфата. Фруктозо-2,6-бисфосфат — метаболит, образующийся в незначительных количествах из фруктозо-6-фосфата и выполняющий только регуляторные функции. Образование фруктозо-2,6-бисфосфата путём фосфорилирования фруктозо-6-фосфата катализирует бифункциональный фермент (БИФ),который катализирует также и обратную реакцию (рис. 7-55, А). Однако превращение фрукгозо-2,6-бисфосфата в фруктозо-6-фосфат не является обратимым процессом. Образование фруктозо-2,6-бисфосфата требует затрат АТФ, а при образовании фруктозо-6-фосфата из фруктозо-2,6-бисфосфата гидролитически отщепляется неорганический фосфат.
Рис. 7-55. Реакции, катализируемые бифункциональным ферментом (БИФ) в печени (А). Регуляция активности БИФ (Б).
В реакции фосфорилирования фруктозо-6- фосфата фермент проявляет киназную активность, а при дефосфорилировании образованного фруктозо-2,6-бисфосфата — фосфатазную. Это обстоятельство и определило название фермента «бифункциональный».
Киназная активность БИФ проявляется, когда фермент находится в дефосфорилированной форме (БИФ-ОН). Дефосфорилированная форма БИФ характерна для абсорбтивного периода, когда инсулин/глюкагоновый индекс высокий. В этот период количество фруктозо-2,6-бисфосфата увеличивается (рис. 7-55, Б).
При низком инсулин-глюкагоновом индексе, характерном для периода длительного голодания, происходит фосфорилирование БИФ, и он функционирует как фосфатаза. Результат — снижение количества фруктозо-2,6-бисфосфата.
Киназную и фосфатазную реакции катализируют разные активные центры БИФ, но в каждом из двух состояний фермента (фосфорилированном и дефосфорилированном) один из активных центров ингибирован. Регуляторное влияние фруктозо-2,6-бисфосфата заключается в том, что он аллостерически активирует фосфофруктокиназу (фермент гликолиза). При этом фруктозо-2,6-бисфосфат снижает ингибирующее действие АТФ на этот фермент в абсорбтивном периоде и повышает его сродство к фруктозо-6- фосфату. В то же время фруктозо-2,6-бисфосфат ингибирует фруктозо-1,6-бисфосфатазу (фермент глюконеогенеза). Итак, в абсорбтивном периоде уровень фруктозо-2,6-бисфосфата повышается, что приводит к активации фосфофруктокиназы и ускорению гликолиза.
Результатом уменьшения количества фрукто- зо-2,6-бисфосфата в постабсорбтивном периоде будет снижение активности фосфофруктокиназы, замедление гликолиза и переключение гликолиза на глюконеогенез. Регуляторное влияние фруктозо-2,6-бисфосфата представлено на рис. 7-56.
Рис. 7-56. Регуляция реакций II субстратного цикла фруктозо-2,6-бисфосфатом.
В регуляции третьего субстратного цикла основная роль принадлежит пируваткиназе, фосфорилированная форма которой неактивна, а дефосфорилированная — активна (рис. 7-57).
Рис. 7-57. Регуляция пируваткиназы в печени.
В период пищеварения инсулин активирует фосфопротеинфосфатазу, которая дефосфорилирует пируваткиназу, переводя её в активное состояние. Кроме того, инсулин в печени влияет на количество ферментов, индуцируя синтез пиру- ваткиназы и репрессируя синтез фосфоенолпируваткарбоксикиназы. Следовательно, гликолитическая реакция фосфоенолпируват —> пируват ускоряется при пищеварении. Эта же реакция замедляется в постабсорбтивном состоянии под влиянием глюкагона, который опосредованно через цАМФ-зависимую протеинкиназу фосфорилирует и инактивирует пируваткиназу.
При длительном голодании глюкагон ускоряет глюконеогенез. Это достигается не только путём фосфорилирования пируваткиназы и снижением скорости гликолиза, но и путём индукции синтеза ферментов глюконеогенеза: фосфоенолпируваткарбоксикиназы, фруктозо- 1,6-бисфосфатазы и глюкозо-6-фосфатазы. Известно, что глюкагон, фосфорилируя опосредованно транскрипционные факторы, влияет на их активность и таким образом индуцирует синтез этих ферментов глюконеогенеза. Кроме того, синтез фосфоенолпируваткарбоксикиназы при длительном голодании индуцируется кортизолом, однако это происходит в результате включения другого механизма действия, характерного для стероидных гормонов (см. разделы 5, 11).
Координация скорости реакции II и III субстратных циклов достигается с помощью фруктозо-1,6-бисфосфата — продукта II субстратного цикла (гликолитическое направление), который является аллостерическим активатором пируваткиназы. В период пищеварения вследствие ускорения начальных стадий гликолиза концентрация фруктозо-1,6-бисфосфата повышается, что приводит к дополнительной активации пируваткиназы.
Общая картина регуляции процессов, составляющих метаболизм глюкозы в печени, представлена на рис. 7-54.
Необходимо отметить, что противоположные реакции каждого из субстратных циклов могут протекать одновременно. Соответственно, гликолиз и глюконеогенез в печени в какой-то мере тоже могут происходить одновременно, хотя их относительные скорости изменяются. Так, при пищеварении преобладает гликолитическое направление, а в постабсорбтивном состоянии — направление глюконеогенеза. Например, реакция глюконеогенеза пируват —> оксалоацетат может протекать при любых состояниях организма. Это объясняется необходимостью поддерживать концентрацию оксалоацетата на определённом уровне, потому что оксалоацетат используется не только в глюконеогенезе, но и в других процессах, таких как цитратный цикл, трансмембранный перенос веществ, синтез аминокислот.
Б. Значение гликолиза в печени для синтеза жиров
Основным значением ускорения гликолиза в печени в период пищеварения является образование дигидроксиацетонфосфата и ацетил-КоА — исходных веществ для синтеза жира. Образование ацетил-КоА из пирувата в ходе реакции, катализируемой ПДК, регулируется разными способами и подробно описывалось в разделе 6.
В абсорбтивном периоде ПДК находится в дефосфорилированной (активной) форме, следовательно, декарбоксилирование пирувата ускоряется. Образуемый ацетил-КоА используется в основном двумя путями: для синтеза жирных кислот и в цитратном цикле. В период пищеварения ускоряются образование ацетил-КоА и его использование для синтеза жирных кислот. Необходимый для синтеза жира α-глицерофосфат образуется в реакции восстановления из дигидроксиацетонфосфата (рис. 7-58). Подробно этот процесс рассматривается в разделе 8.
Рис. 7-58. Синтез жира из углеводов. 1 — окисление глюкозы до пирувата и окислительное декарбоксилирование пирувата приводят к образованию ацетил-КоА; 2 — ацетил-КоА является строительным блоком для синтеза жирных кислот; 3 — жирные кислоты и α-глицеролфосфат, образующийся в реакции восстановления дигидроксиацетонфосфата, участвуют в синтезе триацилглицеролов.
В. Аллостерическая регуляция аэробного распада глюкозы и глюконеогенеза в печени энергетическим статусом клетки
Аллостерическая регуляция скорости гликолиза, зависимая от изменения соотношения АТФ/АДФ, направлена на изменение скорости использования глюкозы непосредственно клетками печени. Глюкоза в клетках печени используется не только для синтеза гликогена и жиров, но также и как источник энергии для синтеза АТФ. Основными потребителями АТФ в гепатоцитах являются процессы трансмембранного переноса веществ, синтез белков, гликогена, жиров, глюконеогенез. От скорости утилизации АТФ в этих процессах зависит скорость его синтеза. АТФ, АДФ и АМФ, а также NAD + и NADH служат аллостерическими эффекторами некоторых гликолитических ферментов и ферментов глюконеогенеза. В частности, АМФ активирует фосфофруктокиназу и ингибирует фруктозо-1,6- бисфосфатазу. АТФ и NADH ингибируют пируваткиназу, а АДФ ингибирует пируваткарбоксилазу.
Следовательно, при усилении расходования АТФ и снижении его концентрации с одновременным увеличением концентрации АМФ, активируется гликолиз и образование АТФ, а глюконеогенез при этом замедляется. Кроме того, от соотношения АТФ/АДФ, АМФ и NAD/ NADH зависит скорость реакций общего пути катаболизма (см. раздел 6).
источник
Печень отличается наиболее сложным обменом глюкозы по сравнению с другими органами. Кроме двух противоположных процессов — синтеза и распада гликогена — в печени могут происходить два других противоположно направленных процесса — гликолиз и глюконеогенез.
В случае как синтеза и распада гликогена, так и гликолиза и глюконеогенеза направление метаболизма глюкозы в печени связано с ритмом питания. При пищеварении значительная часть глюкозы (около половины) из крови воротной вены задерживается печенью, откладывается в форме гликогена, а также используется для синтеза жиров. Исходные субстраты для синтеза жиров — a-глицерофосфат и жирные кислоты — образуются в процессе гликолиза и ОПК. Синтез жиров из глюкозы происходит подобным образом и в жировой ткани.
2. Переключение печени с гликолиза на глюконеогенез и наоборот происходит с участием инсулина и глюкагона и осуществляется с помощью:
1. аллостерических механизмов;
2. ковалентной модификации ферментов путем фосфорилирования / дефосфорилирования;
3. индукции / репрессии синтеза ключевых ферментов, катализирующих реакции субстратньх циклов.
Регуляция направлена на необратимые стадии гликолиза и глюконеогенеза.
В период пищеварения после приема богатой углеводами пищи инсулин-глюкагоновый индекс возрастает, индуцируется транскрипция генов и увеличивается количество гликолитических ферментов глюкокиназы, фосфофруктокиназы и пируваткиназы, что стимулирует гликолитический путь.
При уменьшении инсулин-глюкагонового индекса транскрипция гена и синтез этих ферментов снижаются, но синтез ферментов глюконеогенеза — фосфоенолпируваткарбоксикиназы, фруктозо-6-фосфатазы и глюкозо-6-фосфатазы — увеличивается, в результате чего стимулируется глюконеогенез.
Регуляция энергетического статуса гепатоцитов осуществляется путем изменения скорости аэробного распада глюкозы.
Глюкоза в клетках печени используется не только для синтеза гликогена и жиров, но и как источник энергии, который необходим для синтеза веществ на экспорт и для жизнеобеспечения самих гепатоцитов. АТР синтезируется в реакциях субстратного и окислительного фосфорилирования при аэробном гликолизе, в результате окислительного декарбоксилирования пирувата и окисления ацетил-КоА в цитратном цикле.
Основными потребителями АТР в гепатоцитах являются трансмембранный перенос веществ, синтез белков, гликогена, жиров, глюконеогенез. От скорости утилизации АТР в этих процессах зависит скорость его синтеза. Это достигается тем, что АТР и AMP являются аллостерическими эффекторами некоторых гликолитических ферментов. В частности, AMP активирует фосфофруктокиназу и ингибирует фосфатазу фруктозо-1,6-бифосфата, а АТФ ингибирует пируваткиназу.
Следовательно, при усилении расходования АТФ и снижении его концентрации (при одновременном увеличении концентрации АМФ) активируется гликолиз и синтез АТФ, а глюконеогенез замедляется. От АТФ и АМФ зависит и скорость реакций общего пути катаболизма.
источник
1. Переключение метаболизма печени с гликолиза на глюконеогенез и наоборот происходит при помощи:
— аллостерических механизмов регуляции активности ключевых ферментов;
— ковалентной модификации ферментов путем фосфорилирования (дефосфорилирования) с участием инсулина и глюкагона;
— индукции (репрессии) синтеза ключевых ферментов, катализирующих реакции субстратных циклов.
Регуляция гликолиза и глюконеогенеза в печени направлена на необратимые стадии гликолиза и глюконеогенеза, которые формируют три субстратных цикла (на рис. 6.20 обозначены I, II, III). Название «субстратный цикл» означает объединение реакций синтеза и распада субстрата.
2. Направление реакций первого субстратного цикла регулируется главным образом концентрацией глюкозы. При пищеварении (абсорбтивный период) концентрация глюкозы в крови повышается (до 120-140 мг/дл, или 7-8 ммоль/л). Активность глюкокиназы в этих условиях максимальна. Вследствие этого ускоряется реакция Глюкоза — Глюкозо-6-фосфат. Поскольку глюкокиназа печени не ингибируется глюкозо-6-фосфатом (в отличие от гексокиназы мышц), то основная часть глюкозо-6-фосфата направляется в гликолиз и на синтез гликогена.
3. Направление реакций второго субстратного цикла зависит от активности фосфофруктокиназы и фосфатазы фруктозо-1,6-бисфосфата. В этом цикле действует фруктозо-2,6-бисфосфат, который одновременно выполняет функцию аллостерического активатора фосфофруктокиназы (регуляторный фермент гликолиза) и аллостерического ингибитора фосфатазы фруктозо- 1,6-бисфосфата (регуляторный фермент глюконеогенеза).
Фруктозо-2,6-бисфосфат образуется в абсорбтивный период путем фосфорилирования фруктозо-6-фосфата при участии бифункционального фермента (БИФ), который в дефосфорилированной форме (БИФ-ОН) проявляет киназную активность (рис. 6.24). Дефосфорилирование БИФ происходит с помощью фермента фосфопротеинфосфатазы, который активируется при высоком инсулин-глюкагоновом индексе за счет инсулинового рецептора.
При низком инсулин-глюкагоновом индексе, характерном для периода голодания, происходит фосфорилирование БИФ (БИФ-ОРО3Н2) с помощью протеинкиназы А, которая активируется вследствие активации аденилатциклазной системы в результате взаимодействия гормона глюкагона с рецепторами. При этом БИФ проявляет фосфатазную активность. В результате
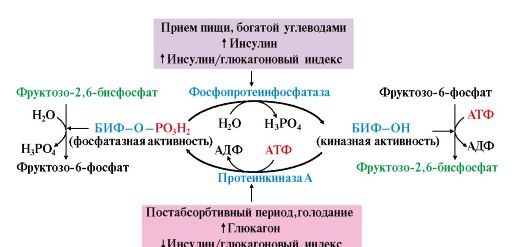
БИФ катализирует реакции обратимого превращения фруктозо-6-фосфата в фруктозо-2,6-бисфосфат. БИФ может находиться в двух формах: дефосфорилированной (БИФ-ОН) и фосфорилированной (БИФ-ОРО3Н2). БИФ-ОН обладает киназной активностью и способствует образованию фруктозо-2,6-бисфосфата. БИФ-ОРО3Н2 обладает фосфатазной активностью и способствует уменьшению концентрации фруктозо-2,6-бисфосфата и образованию фруктозо-6-фосфата. Фосфорилирование и дефосфорилирование БИФ связано с ритмом питания и регулируется гормонами. Инсулин (абсорбтивный период) активирует фермент фосфопротеинфосфатазу, что приводит к появлению формы БИФ-ОН, а глюкагон (постабсорбтивный период) активирует аденилатциклазную систему, что вызывает активацию протеинкиназы А и появление формы БИФ-ОРО3Н2
Уменьшается количество фруктозо-2,6-бисфосфата, что приводит к замедлению гликолиза и переключению метаболизма на глюконеогенез. Наличие двух активностей (киназной и фосфатазной) у БИФ определило название фермента — «бифункциональный».
БИФ присутствует только в гепатоцитах. Киназную и фосфатазную реакции катализируют разные активные центры БИФ, которые функционируют по очереди в зависимости от состояния фермента фосфорилированного или дефосфорилированного. Превращение фруктозо-2,6-бисфосфата в фрукто- зо-6-фосфат не является обратимым процессом. Образование фруктозо-2,6- бисфосфата требует затрат АТФ, а при образовании фруктозо-6-фосфата из фруктозо-2,6-бисфосфата высвобождается неорганический фосфат.
4. В регуляции третьего субстратного цикла основная роль принадлежит пируваткиназе, фосфорилированная форма которой неактивна, а дефосфорилированная активна (рис. 6.25). Дефосфорилирование пируваткиназы происходит в период пищеварения, когда инсулин активирует фосфопротеинфосфатазу, которая дефосфорилирует пируваткиназу, переводя ее в активное состояние. Следовательно, реакция превращенияфосфоенолпируват в пируват ускоряется при пищеварении (абсорбтивный период). В постабсорбтивном состоянии пируваткиназа при действии глюкагона на печень переходит в фосфорилированное неактивное состояние.
Реакция глюконеогенеза превращения пирувата — оксалоацетат катализитуется биотин-зависимым ферментом — пируваткарбоксилазой с участием АТФ в качестве источника энергии. Регуляция этой реакции осуществляется с помощью аллостерической активации ацетил-КоА.Биологическое значение этого эффекта объясняется тем, что при голодании организм начинает использовать жирные кислоты как источник энергии.

Последнее изменение этой страницы: 2017-01-24; Нарушение авторского права страницы
источник
Так как синтез и окисление глюкозы являются крайне важными для существования клетки (гликолиз) и всего организма (глюконеогенез), то регуляция этих процессов отвечает запросам органов и тканей при различных условиях существования.
Поскольку гликолитическое окисление глюкозы
- является способом получения энергии в аэробных и анаэробных условиях, то оно непрерывно происходит во всех клетках и, конечно, должно и будет активировано при усилении работы клетки, например, сокращение миоцита, движение нейтрофилов;
- служит источником глицерола и ацетил-SКоА, используемых для синтеза жиров в гепатоцитах и адипоцитах, то такое окисление активируется при избытке глюкозы в этих клетках.
Глюконеогенез , как образование глюкозы в печени из неуглеводных источников, необходим:
- при гипогликемии во время мышечной нагрузки – синтез глюкозы из молочной кислоты , поступающей из работающих мышц, и из глицерола , образующегося при мобилизации жиров;
- при гипогликемии при кратком голодании (до 24 часов) – синтез преимущественно из молочной кислоты , непрерывно поступающей в печень из эритроцитов,
- при гипогликемии при длительном голодании – в основном синтез из аминокислот , образующихся при катаболизме белков, и также из молочной кислоты и глицерина .
Таким образом, глюконеогенез, идущий в печени, обеспечивает глюкозой все остальные клетки и органы (эритроциты, нервная ткань, мышцы и др.), в которых активны процессы, требующие глюкозу. Поступление глюкозы в эти клетки также необходимо, чтобы поддержать концентрацию оксалоацетата и обеспечить сгорание в ЦТК ацетил-SКоА, получаемого из жирных кислот или кетоновых тел.
В целом можно выделить два способа регуляции гликолиза и глюконеогенеза: гормональная при участии гормонов и метаболическая , т.е. при помощи промежуточных или конечных продуктов обмена глюкозы.
Существуют три основных участка, на которых происходит регуляция этих процессов:
- первая реакция гликолиза,
- третья реакция гликолиза и обратимая ей,
- десятая реакция гликолиза и обратимые ей.
Гормональная активация глюконеогенеза осуществляется глюкокортикоидами , которые увеличивают синтез пируваткарбоксилазы, фосфоенолпируват-карбоксикиназы, фруктозо-1,6-дифосфатазы. Глюкагон стимулирует те же самые ферменты через аденилатциклазный механизм путем фосфорилирования.
Энергия для глюконеогенеза поступает от β-окисления жирных кислот. Конечный продукт этого окисления, ацетил-SКоА аллостерически стимулирует активность первого фермента глюконеогенеза – пируваткарбоксилазы. Кроме этого, фруктозо-1,6-дифосфатаза стимулируется при участии АТФ .
В печени гликолиз стимулируется инсулином , повышающим количество ключевых ферментов гликолиза (гексокиназы, фосфофруктокиназы, пируваткиназы).
В печени активность глюкокиназы, кроме инсулина, регулируется другими гормонами:
- активацию вызывает ан дро гены ,
- подавляют ее активность глюкокортикоиды и эстрогены .
В других тканях активность гексокиназ
- повышается тиреоидными гормонами,
- снижается – глюкокортикоидами и соматотропином .
Гексокиназа непеченочных клеток ингибируется продуктом собственной реакции – глюкозо-6-фосфатом .
Фосфофруктокиназа:
- активируется АМФ и собственным субстратом ( фруктозо-6-фосфат ),
- ингибируется – АТФ , лимонной кислотой, жирными кислотами.
Пируваткиназа активируется фруктозо-1,6-дифосфатом (прямая положительная регуляция).
Молекулы АМФ, стимулирующие гликолиз, образуются в аденилаткиназной реакции, активируемой при появлении избытка АДФ. Особенно ярко значение такой регуляции проявляется при мышечной работе:
источник
Печень отличается наиболее сложным обменом глюкозы по сравнению с другими органами. В ней происходят противоположные процессы: синтез/распад гликогена и гликолиз/глюконеогенез.
Направление метаболизма глюкозы в печени связано с ритмом питания. При пищеварении около половины глюкозы из крови воротной вены задерживается печенью, откладывается в форме гликогена, а также используется для синтеза жиров.
Переключение печени с гликолиза на глюконеогенез и наоборот происходит с участием инсулина и глюкагона и осуществляется с помощью:
— ковалентной модификации ферментов путем
фосфорилирования / дефосфорилирования;
— индукции/репрессии синтеза ключевых ферментов.
Регуляция направлена на необратимые стадии гликолиза и глюконеогенеза.
При уменьшении инсулин-глюкагонового индекса синтез ключевых ферментов гликолиза снижается, а ферментов глюконеогенеза (фосфоенолпируваткарбоксикиназа, фруктозо-6-фосфатаза, глкозо-6-фосфатаза) — увеличивается, и стимулируется глюконеогенез.
Направление реакций гликолиза регулируется содержанием глюкозы. При пищеварении концентрация глюкозы в крови возрастает до 10-20 мкмоль/л и активность глюкокиназы будет максимальной. Ускоряется гликолитическая реакция
Инсулин индуцирует синтез глюкокиназы и поэтому ускоряет фосфорилирование глюкозы.
Т.к. глюкокиназа печени не ингибируется глюкоза-6-фосфатом, то большая часть последнего направляется погликолитическому пути.
Активность фосфофруктокиназы (фермент гликолиза) и фосфатазы фруктозо-1,6-бисфосфата (фермент глюконеогенеза) зависит от концентрации фруктозо-2,6-бисфосфата.
Фруктозо-2,6-бисфосфат аллостерически активирует фосфофруктокиназу (усиливается гликолиз ) и ингибирует фосфатазу фруктозо-1,6-бифосфата (замедляется глюконеогенез ).
Фруктозо-2,6-бисфосфат образуется фосфорилированием фруктозо-6-фосфата при участии бифункционального фермента (БИФ).
Киназная активность проявляется при дефосфорилированной форме БИФ, которая характерна для абсорбтивного периода (инсулин-глюкагоновый индекс высокий) – гликолиз усиливается.
Фосфатазная активность проявляется при фосфорилированной форме БИФ (длительное голодание, инсулин/глюкагоновый индекс низкий): снижается количество фруктозо-2,6-бисфосфата, гликолиз замедляется и переключается на глюконеогенез.
В период пищеварения инсулин активирует протеинфосфатазу, которая дефосфорилирует пируваткиназу, и переводит ее в активное состояние: реакция
фосфоенолпируват → пируват (гликолитическая)
ускоряется при пищеварении и замедляется в постабсорбтивном периоде.
пируват → оксалоацетат → фосфоенолпируват
могут протекать при любом состоянии организма. Это необходимо для поддержания постоянной концентрации оксалоацетата, использующегося, помимо глюконеогенеза, в цикле Кребса, при трансмембранном переносе веществ, в синтезе аминокислот.
В период пищеварения из-за ускорения начальных стадий гликолиза повышается содержание фруктозо-1,6-бисфосфата, что ведет к активации пируваткиназы (гликолиз усиливается ).
После приема пищи, богатой углеводами, инсулин-глюкагоновый индекс возрастает, увеличивается количество глюкокиназы, фосфофруктокиназы, пируваткиназы (гликолитические ферменты), что стимулирует гликолитический путь.
Регуляция энергетического статуса гепатоцитов осуществляется путем изменения скорости аэробного распада глюкозы.
Глюкоза в клетках печени используется не только для синтеза гликогена и жиров, но и для энергообеспечения гепатоцитов. Для этого АТФ синтезируется в реакциях субстратного и окислительного фосфорилирования при аэробном гликолизе, при окислительном декарбоксилировании ПВК и при окислении ацетил-KoA в цикле Кребса.
Основными потребителями АТФ в гепатоцитах являются трансмембранный перенос веществ, синтез белков, гликогена, жиров, глюконеогенез. Скорость синтеза АТФ зависит от скорости его расходования в этих процессах.
АТФ и АМФ – аллостерические эффекторы некоторых гликолитических ферментов: АМФ активирует фосфофруктокиназу и ингибирует фосфатазу фруктозо-1,6-бисфосфата, АТФ ингибирует пируваткиназу.
Т.о., при расходовании АТФ (растет концентрация АМФ) активируются гликолиз и синтез АТФ, а глюконеогенез замедляется.
Нарушения углеводного обмена
Нарушение гидролиза и всасывания углеводов
Всасывание углеводов нарушается при недостаточности амилолитических ферментов желудочно-кишечного тракта (амилаза панкреатического сока и др.). При этом поступающие с пищей углеводы не расщепляются до моносахаридов и не всасываются. Развивается углеводное голодание.
Всасывание углеводов страдает также при нарушении фосфорилирования глюкозы в кишечной стенке, возникающем при воспалении кишечника, при отравлении ядами, блокирующими фермент гексокиназу (флоридзин, монойодацетат).
Гликогенозы — группа наследственных заболеваний, обусловленная недостаточностью ферментов, участвующих в синтезе или распаде гликогена.
Болезнь Гирке – глюкозо-6-фосфатаза (печень).
Болезнь Помпе – a-1,4-глюкозидаза (все органы).
Болезнь Кори (болезнь остаточного декстрина) – амило-1,6-глюко-зидаза (печень, миокард, скелетные мышцы).
Болезнь Андерсона – гликогенветвящийся фермент (печень, миокард, скелетные мышцы).
Болезнь Мак-Ардла – мышечная фосфорилаза (мышцы).
Болезнь Херса – печеночная фосфорилаза (печень).
При недостаточности гликогенсинтазы нарушается синтез гликогена, и больные умирают в раннем возрасте.
Нарушения промежуточного обмена углеводов
1. Гипоксические состояния (при недостаточности дыхания или кровообращения, при анемиях и др.), анаэробная фаза превращения углеводов преобладает над аэробной. Происходит избыточное накопление в тканях и крови молочной и пировиноградной кислот. Возникает ацидоз. Нарушаются ферментативные процессы. Снижается образование АТФ.
2. Расстройства функции печени, где в норме часть молочной кислоты ресинтезируется в глюкозу и гликоген. При поражении печени ресинтез нарушается. Развиваются гиперлакцидемия и ацидоз.
3. Гиповитаминоз В1. Нарушается окисление ПВК, т. к. витамин B1 входит в состав пируватдегидрогеназного комплекса. ПВК накапливается в избытке и частично переходит в молочную кислоту, содержание которой также возрастает. При нарушении окисления ПВК снижается синтез ацетилхолина и нарушается передача нервных импульсов. Уменьшается образование из ПВК ацетил-KoA.
ПВК является фармакологическим ядом для нервных окончаний. При увеличении ее концентрации в 2-3 раза возникают нарушения чувствительности, невриты, параличи и др.
При гиповитаминозе B1 нарушается пентозофосфатный путь обмена углеводов, в частности, образование рибозы.
При некоторых состояниях можно наблюдать повышение содержания глюкозы в крови — гипергликемию, а также понижение концентрации глюкозы — гипогликемию.
Гипергликемия может наблюдаться при гипофизарных заболеваниях, опухолях коркового вещества надпочечников, гиперфункции щитовидной железы. Иногда — во время беременности. Гипергликемия возможна при органических поражениях ЦНС, расстройствах мозгового кровообращения, болезнях печени воспалительного или дегенеративного характера.
Исследуются изменения во времени уровня глюкозы в крови, обычно после приема 50 г или 100 г глюкозы, растворенной в теплой воде, — так называемая сахарная нагрузка.
При оценке построенных гликемических кривых обращают внимание на время максимального подъема, высоту этого подъема и время возврата концентрации глюкозы к исходному уровню.
У здорового человека после одномоментного приема 100 г глюкозы содержание глюкозы в крови нарастает, достигая максимума — 1,5-1,7 г/л через 30-45 мин. Затем ее содержание в крови начинает падать и через 2 ч снижается до нормы (0,8-1,2 г/л), а через 3 ч оказывается даже несколько ниже нормы.
Для оценки гликемических кривых введено несколько показателей, из которых наиболее важное значение имеет коэффициент Бодуэна:
где А — уровень глюкозы в крови натощак; В — максимальное содержание глюкозы в крови после нагрузки глюкозой.
В норме этот коэффициент составляет около 50%. Значения, превышающие 80%, свидетельствуют о серьезном нарушении обмена углеводов.
Гормональные гипергликемии. Возникают при нарушении функции эндокринных желез, гормоны которых участвуют в регуляции углеводного обмена. Например, гипергликемия развивается при повышении продукции глюкагона — гормона α -клеток островков Лангерганса поджелудочной железы, который, активируя фосфорилазу печени, способствует гликогенолизу.
Сходным действием обладает адреналин.
К гипергликемии ведет избыток глюкокортикоидов (стимулируют глюконеогенез и тормозят гексокиназу) и соматотропного гормона гипофиза (тормозит синтез гликогена, способствует образованию ингибитора гексокиназы).
Недостаточность инсулина – сахарный диабет.
Углеводный обмен при сахарном диабете характеризуется следующими особенностями:
1. Резко снижен синтез глюкокиназы, которая при диабете почти полностью исчезает из печени, что ведет к уменьшению образования глюкозо-6-фосфата. Этот момент наряду со сниженным синтезом гликогенсинтетазы обусловливает резкое замедление синтеза гликогена. Происходит обеднение печени гликогеном. При недостатке глюкозо-6-фосфата тормозится пентозофосфатный цикл.
2. Активность глюкозо-6-фосфатазы резко возрастает, поэтому глюкозо-6-фосфат дефосфорилируется и поступает в кровь в виде глюкозы.
3. Понижается прохождение глюкозы через клеточные мембраны.
5. Ускоряется глюконеогенез, что обусловлено отсутствием подавляющего влияния инсулина на ферменты, обеспечивающие глюконеогенез: пируваткарбоксилазу, глюкозо-6-фосфатазу и др.
При сахарном диабете имеют место избыточная продукция и недостаточное использование глюкозы тканями, вследствие чего возникает гипергликемия. Содержание глюкозы в крови при тяжелых формах может достигать 4-5 г/л и выше. При этом резко возрастает осмотическое давление крови, что ведет к обезвоживанию клеток организма. В связи с обезвоживанием глубоко нарушаются функции центральной нервной системы (гиперосмолярная кома).
Гликемическая кривая при диабете по сравнению с таковой у здоровых значительно растянута во времени.
Значение гипергликемии при сахарном диабете двояко:
— она играет адаптивную роль, так как при ней тормозится распад гликогена и частично усиливается его синтез. При гипергликемии глюкоза лучше проникает в ткани и они не испытывают резкого недостатка углеводов;
— гипергликемия имеет и отрицательное значение. При ней повышается концентрация гликозилированных белков. Поэтому для сахарного диабета характерно раннее поражение сосудов атеросклерозом и ретинопатии (поражение сосудов сетчатки глаза). Атеросклеротический процесс захватывает коронарные сосуды сердца (коронарная недостаточность), сосуды почек (гломерулонефриты) и др.
Гипогликемия связана с понижением функций тех эндокринных желез, повышение функций которых приводит к гипергликемии. Гипогликемию можно наблюдать при гипофизарной кахексии, аддисоновой болезни, гипотиреозе, аденомах поджелудочной железы вследствие повышенной продукции инсулина. Гипогликемия может быть вызвана голоданием, продолжительной физической работой, приемом β -ганглиоблокаторов, иногда отмечается при беременности, лактации. Гипогликемия может возникнуть при введении больным сахарным диабетом больших доз инсулина.
Является результатом нарушения углеводного обмена вследствие патологических изменений в поджелудочной железе (сахарный диабет, острый панкреатит и т.д.).
При тяжелых формах сахарного диабета содержание глюкозы в моче может достигать 8-10%. Осмотическое давление мочи повышается. Суточный диурез возрастает до 5-10 л и более (полиурия). Развивается обезвоживание организма и как следствие его — усиленная жажда (полидипсия).
Реже встречается глюкозурия почечного происхождения, связанная с недостаточностью резорбции глюкозы в почечных канальцах.
Как временное явление глюкозурия может возникнуть при некоторых острых инфекционных и нервных заболеваниях, после приступов эпилепсии, сотрясения мозга.
Отравления морфином, стрихнином, хлороформом, фосфором также обычно сопровождаются глюкозурией.
Может быть глюкозурия алиментарного происхождения, глюкозурия беременных и глюкозурия при нервных стрессовых состояниях (эмоциональная глюкозурия).
Врожденный недостаток фермента фруктокиназы (не образуется фруктозо-1-фосфат). Накопление фруктозы в крови, фруктозурия.
Недостаток фермента гексозо-1-фосфатуридилтрансферазы. Накопление галактозы и галактозо-1-фосфата в крови. Умственная отсталость, катаракта хрусталика.
Активность ферментов второго субстратного цикла зависит от концентрации фруктозо-2,б-бисфосфата. Как и фруктозо-1,б-бисфосфат, фруктозо-2,6-бисфосфат образуется из фруктозо-б-фосфата и может снова превращаться во фруктозо-б-фосфат, т. е. тоже получается субстратный цикл. Обе реакции этого цикла катализирует один фермент — бифункциональный фермент (БИФ), который регулируется путем фосфорилирования-дефосфорилирования.

Дефосфори-лированный фермент (БИФ-ОН) обладает киназной активностью (фруктозо-б-фосфат-2-киназа), а фосфорилированный (БИФ-Р) — фосфатазной активностью (фосфатаза фруктозо-2,б-бисфосфата). Киназная и фосфатазная реакции катализируются разными активными центрами, но в каждом из двух состояний фермента — фосфорилированном и дефосфорилированном — один из активных центров инги-бирован.
Фруктозо-2,б-бисфосфат активирует фосфофруктокиназу (б-фосфофруктокина-зу), т.
е. гликолитический фермент, и ингибирует фосфатазу фруктозо-1,б-бисфос-фата — фермент глюконеогенеза. При пищеварении БИФ дефосфорилирован, следовательно, проявляет киназную активность, увеличивает концентрацию фрукто-зо-2,б-бисфосфата, который активирует гликолитическое направление цикла II, и ингибирует направление глюконеогенеза этого цикла.
В постабсорбтивном состоянии БИФ фосфорилирован, проявляет фосфатаз-ную активность, и концентрация фруктозо-2,6-бисфосфата снижается. Вследствие этого активность б-фосфофрукто-1-киназы тоже снижается, а активность фосфа-тазы фруктозо-1,6-фосфата увеличивается, т. е. гликолитическое направление тормозится, а направление глюконеогенеза активируется.
Субстратный цикл III регулируется главным образом концентрацией глюкозы. При пищеварении концентрация глюкозы в гепатоцитах существенно повышается и, соответственно, повышается скорость фосфорилирования глюкозы глюко-киназой (см. разд. «Фосфорилирование глюкозы»). Поскольку в этих условиях активированы гликолитические ветви субстратных циклов II и I, то основная часть глюкозо-6-фосфата направляется на путь гликолиза.
Фруктозо-1,б-бисфосфат является аллостерическим активатором пируваткина-зы. При ускорении начальных стадий гликолиза после приема пищи концентрация фруктозо-1,б-бисфосфата повышается, что приводит к дополнительной активации пируваткиназы. Этим достигается координация функционирования I и II субстратных циклов.
В целом за счет распада гликогена и глюконеогенеза печень поставляет в кровь около 300 г глюкозы за сутки, из них примерно 2Д — из гликогена.
Один из основных результатов гликолиза в печени — образование исходных веществ для синтеза жиров. Конечный продукт аэробного гликолиза — пируват подвергается окислительному декарбоксилированию, и образующийся ацетил-КоА используется для синтеза жирных кислот (наряду с окислением в цитратном цикле). Необходимый для синтеза жиров сс-глицерофосфат образуется из другого метаболита гликолиза — диоксиацетонфосфата.
Так как синтез и окисление глюкозы являются крайне важными для существования клетки (гликолиз) и всего организма (глюконеогенез), то регуляция этих процессов отвечает запросам органов и тканей при различных условиях существования.
Поскольку гликолитическое окисление глюкозы является:
- способом получения энергии и в аэробных и в анаэробных условиях, то оно непрерывно происходит во всех клетках и, конечно, должно и будет активировано при усилении работы клетки, например, сокращение миоцита, движение нейтрофилов;
- источником глицерола и ацетил-SКоА, используемых для синтеза жиров в гепатоцитах и адипоцитах, то такое окисление активируется при избытке глюкозы в клетке.
Глюконеогенез, как образование глюкозы из неуглеводных компонентов, необходим:
- при гипогликемии во время мышечной нагрузки — синтез из молочной кислоты, поступающей из мышц, из глицерола, образующегося при мобилизации жиров;
- при гипогликемии при голодании — синтез из аминокислот, образующихся при катаболизме белков.
Таким образом, при голодании или физической нагрузке глюконеогенез, идущий в печени, обеспечивает глюкозой все остальные органы (эритроциты, нервная ткань, мышцы и др.), в которых активен гликолиз и другие процессы, производящие энергию. Наличие глюкозы в указанных клетках необходимо, чтобы поддержать концентрацию оксалоацетата и обеспечить сгорание ацетил-SКоА (получаемого также из жирных кислот или кетоновых тел) в цикле трикарбоновых кислот.
В целом можно выделить два способа регуляции гликолиза и глюконеогенеза: гормональная при участии гормонов и метаболическая, то есть при помощи промежуточных или конечных продуктов обмена глюкозы.
Существуют три основных участка, на которых происходит регуляция этих процессов:
- первая реакция гликолиза,
- третья реакция гликолиза и обратимая ей,
- десятая реакция гликолиза и обратимые ей.
Гормональная активация глюконеогенеза осуществляется глюкокортикоидами, которые увеличивают синтез пируваткарбоксилазы, фосфоенолпируват-карбоксикиназы, фруктозо-1,6-дифосфатазы. Глюкагон стимулирует те же самые ферменты через аденилатциклазный механизм путем фосфорилирования.
Также имеется метаболическая регуляция, при которой аллостерически активируется пируваткарбоксилаза при помощи ацетил-SКоА, фруктозо-1,6-дифосфатаза при участии АТФ.
Гликолиз стимулируется инсулином, повышающим количество молекул гексокиназы, фосфофруктокиназы, пируваткиназы.
В печени активность глюкокиназы регулируется гормонами: активацию вызывает инсулин и андрогены, подавляют ее активность глюкокортикоиды и эстрогены.
Для метаболической регуляции чувствительной является фосфофруктокиназа. Она активируется АМФ и собственным субстратом, ингибируется — АТФ, лимонной кислотой, жирными кислотами. Пируваткиназа активируется фруктозо-1,6-дифосфатом. Гексокиназа непеченочных клеток ингибируется продуктом собственной реакции — глюкозо-6-фосфатом.

«Субстратные» циклы— парные комбинации процессов синтеза и распада метаболитов. Как уже упоминалось, сочетание процессов синтеза и распада гликогена или необратимых реакций гликолиза и соответствующих им необратимых реакций глюконеогенеза может составить подобный цикл. Название «субстратный цикл» означает объединение реакций синтеза и распада субстрата. Название «холостой» отражает результат работы подобного цикла, заключающийся в бесполезном расходовании АТФ. Хотя существование «холостых» циклов нелогично, тем не менее они могут функционировать. Более того, эти циклы могут быть мишенью регуляторных воздействий, так как составляющие их реакции катализируют разные ферменты. Реципрокное изменение активности этих ферментов предотвращает одновременное протекание противоположных процессов.
Изменение в печени гликолитического направления на глюконеогенез и обратно при смене абсорбтивного состояния на постабсорбтивное или при голодании происходит главным образом в результате регуляции активности ферментов, катализирующих реакции субстратных циклов. Эти циклы обозначены цифрами I, II, III на рис. 7-54, представляющем общую картину регуляции гликолиза и глюконеогенеза в печени.
Направление реакции первого субстратного цикларегулируется главным образом концентрацией глюкозы. При пищеварении концентрация глюкозы в крови повышается (до 8-10 ммоль/л). Активность глюкокиназы в этих условиях максимальна. Вследствие этого ускоряется гликолитическая реакция образования глюкозо-6-фосфата. Кроме того, инсулин индуцирует синтез глюкокиназы и ускоряет тем самым фосфорилирование глюкозы.
Поскольку глюкокиназа печени не ингибируется глюкозо-6-фосфатом (в отличие от гексокиназы мышц), то основная часть глюкозо-6-фосфата в абсорбтивном периоде направляется на синтез гликогена и по гликолитическому пути.
Направление реакций второго субстратного циклазависит от активности фосфофруктокиназы и фосфатазы фруктозо-1,6-бисфосфата. Активность этих ферментов зависит от концентрации фруктозо-2,6-бисфосфата. Фруктозо-2,6-бисфосфат— метаболит, образующийся в незначительных количествах из фруктозо-6-фосфата и выполняющий только регуляторные функции. Образование фруктозо-2,6-бисфосфата путём фосфорилирования фруктозо-6-фосфата катализирует бифункциональный фермент(БИФ), который катализирует также и обратную реакцию (рис. 7-55, А). Однако превращение фруктозо-2,6-бисфосфата в фруктозо-6-фосфат не является обратимым процессом. Образование фруктозо-2,6-бисфосфата требует затрат АТФ, а при образовании фруктозо-6-фосфата из фруктозо-2,6-бисфосфата гидролитически отщепляется неорганический фосфат.
В реакции фосфорилирования фруктозо-6-фосфата фермент проявляет киназную активность, а при дефосфорилировании образованного фруктозо-2,6-бисфосфата — фосфатазную. Это обстоятельство и определило название фермента «бифункциональный».
Киназная активность БИФ проявляется, когда фермент находится в дефосфорилированной форме (БИФ-ОН). Дефосфорилированная форма БИФ характерна для абсорбтивного периода, когда инсулин/глюкагоновый индекс высокий. В этот период количество фруктозо-2,6-бисфосфата увеличивается (рис. 7-55, Б).
При низком инсулинглюкагоновом индексе, характерном для периода длительного голодания, происходит фосфорилирование БИФ, и он функционирует как фосфатаза. Результат — снижение количества фруктозо-2,6-бисфосфата.
7-53. Превращение глицерола в дигидроксиацетонфосфат.
Киназную и фосфатазную реакции катализируют разные активные центры БИФ, но в каждом из двух состояний фермента (фосфорилированном и дефосфорилированном) один из активных центров ингибирован. Регуляторное влияние фруктозо-2,6-бисфосфата заключается в том, что он аллостерически активирует фос-фофруктокиназу (фермент гликолиза). При этом фруктозо-2,6-бисфосфат снижает ингибирующее действие АТФ на этот фермент в абсорбтивном периоде и повышает его сродство к фруктозо-6-фосфату. В то же время фруктозо-2,6-бисфосфат ингибирует фруктозо-1,6-бисфосфатазу (фермент глюконеогенеза). Итак, в абсорбтивном периоде уровень фруктозо-2,6-бисфосфата повышается, что приводит к активации фосфофруктокиназы и ускорению гликолиза.
Результатом уменьшения количества фруктозо-2,6-бисфосфата в постабсорбтивном периоде
Рис. 7-54. Регуляция метаболизма глюкозы в печени. БИФ — бифункциональный фермент (фруктозо-2,6-бисфосфатаза/фос-фофруктокиназа-2); БИФ-ОН — дефосфорилированный фермент; БИФ-Р — фосфорилированный фермент, ПДК-ОН — дефосфорилированный пируватдегидрогеназный комплекс; ПК-ОН — дефосфорилированная пируваткиназа; ГАФ — глицеральдегидфосфат; ДАФ — дигидроксиацетонфосфат, ФЕП — фосфоенолпируват. I-III — субстратные циклы: в рамках — регупяторные ферменты глиполиза и глюконеогенеза.
Рис. 7-55. Реакции, катализируемые бифункциональным ферментом (БИФ) в печени (А). Регуляция активности БИФ (Б).
будет снижение активности фосфофруктокиназы, замедление гликолиза и переключение гликолиза на глюконеогенез. Регуляторное влияние фруктозо-2,6-бисфосфата представлено на рис. 7-56.
В регуляции третьего субстратного циклаосновная роль принадлежит пируваткиназе, фосфорилированная форма которой неактивна, а дефосфорилированная — активна (рис. 7-57).
В период пищеварения инсулин активирует фосфопротеинфосфатазу, которая дефосфорилирует пируваткиназу, переводя её в активное состояние. Кроме того, инсулин в печени влияет на количество ферментов, индуцируя синтез пируваткиназы и репрессируя синтез фосфоенолпи-руваткарбоксикиназы. Следовательно, гликолитическая реакция фосфоенолпируват → пируват ускоряется при пищеварении. Эта же реакция замедляется в постабсорбтивном состоянии под влиянием глюкагона, который опосредованно через цАМФ-зависимую протеинкиназу фосфо-рилирует и инакгивирует пируваткиназу.
При длительном голодании глюкагон ускоряет глюконеогенез. Это достигается не только путём фосфорилирования пируваткиназы и снижением скорости гликолиза, но и путём индукции синтеза ферментов глюконеогенеза: фосфоенолпируваткарбоксикиназы, фруктозо-1,6-бисфосфатазы и глюкозо-6-фосфатазы. Известно, что глюкагон, фосфорилируя опосредованно транскрипционные факторы, влияет на их активность и таким образом индуцирует синтез этих ферментов глюконеогенеза. Кроме того, синтез фосфоенолпируваткарбоксикиназы при длительном голодании индуцируется кортизолом, однако это происходит в результате включения другого механизма действия, характерного для стероидных гормонов (см. разделы 5, 11).
Координация скорости реакции II и III субстратных цикловдостигается с помощью фруктозо-1,6-бисфосфата — продукта II субстратного цикла (гликолитическое направление), который является аллостерическим активатором пируваткиназы. В период пищеварения вследствие ускорения начальных стадий гликолиза концентрация фруктозо-1,6-бисфосфата повышается, что приводит к дополнительной активации пируваткиназы.
Общая картина регуляции процессов, составляющих метаболизм глюкозы в печени, представлена на рис. 7-54.
Рис. 7-56. Регуляция реакций II субстратного цикла фруктозо-2,6-бисфосфатом.
Рис. 7-57. Регуляция пируваткиназы в печени.
Необходимо отметить, что противоположные реакции каждого из субстратных циклов могут протекать одновременно. Соответственно, гликолиз и глюконеогенез в печени в какой-то мере тоже могут происходить одновременно, хотя их относительные скорости изменяются. Так, при пищеварении преобладает гликолитическое направление, а в постабсорбтивном состоянии — направление глюконеогенеза. Например, реакция глюконеогенеза пируват → оксалоацетат может протекать при любых состояниях организма. Это объясняется необходимостью поддерживать концентрацию оксалоацетата на определенном уровне, потому что оксалоацетат используется не только в глюконеогенезе, но и в других процессах, таких как цитратный цикл, трансмембранный перенос веществ, синтез аминокислот.
Date: 2015-09-19; view: 315; Нарушение авторских прав
| Понравилась страница? Лайкни для друзей: |
Глюконеогенез – синтез глюкозы из веществ неуглеводной природы. Его основной функцией является поддержание уровня глюкозы в крови в период длительного голодания и интенсивных физических нагрузок. Основными субстратами глюконеогенеза являются лактат, глицерол, аминокислоты. Глюконеогенез является обратным процессом гликолиза, который протекает в цитоплазме и матриксе митохондрий. Необратимые реакции гликолиза (1, 3 и 10), катализируемые гексокиназами, фруктокиназами и пируваткиназами обходятся с участием 4 специфических ферментов глюконеогенеза: пируваткарбоксилазы, фосфоенолпируват-карбоксикиназы, фруктозо-1,6-фосфотазы и глюкозо-6-фосфотазы. Кроме того, в глюконеогенезе участвуют ферменты ЦТК, например, малат ДГ.
Реакции глюконеогенеза представлены на схеме. Ключевые (необратимые) реакции глюконеогенеза:
1. Пируваткарбоксилаза (ПВК: СО2-синтетаза (АТФ→АДФ+Фн)) содержит биотин, находиться в митохондриях, превращает ПВК в ЩУК. Индуктор: глюкагон, адреналин, кортизол. Репрессор: инсулин. Ингибитор: АМФ, активатор АцетилКоА. Образующийся ЩУК проходит внутреннюю мембрану митохондрий в своей восстановленной (в виде малата) или аминоформе (в виде аспартата).
2. Фосфоенолпируваткарбоксикиназа (ГТФ: ЩУК-2-фосфотрансфераза (декарбоксили-рующая)) находиться в цитоплазме, превращает ЩУК в ФЕП. Индуктор: глюкагон, адреналин, кортизол.
3. Фруктозо-1,6-фосфотаза (Фруктозо-1,6дф: фосфо-гидролаза) дефосфорилирует фруктозо-1,6дф. Индуктор: глюкагон, адреналин, кортизол. Репрессор: инсулин. Ингибирует АМФ, фруктозо-2,6дф. Активатор: цитрат, жирные кислоты.
Глюкозо-6-фосфотаза (Глюкозо-6ф: фосфо-гидролаза) дефосфорилирует глюкозо-6ф. Индуктор: глюкагон, адреналин, кортизол. Репрессор: инсулин.
Энергетический баланс глюконеогенеза. На образование 1 глюкозы из 2 лактатов требуется 6 АТФ: 2 АТФ для пируваткарбоксилазы, 2 ГТФ для ФЕПкарбоксикиназы, 2 АТФ для фосфоглицераткиназы. Обще уравнение глюконеогенеза:
2 лактат + 4 АТФ + 2 ГТФ + 4 Н2О → 1 глюкоза + 4 АДФ + 2 ГДФ + 6 Фн
Регуляция глюконеогенеза. Регуляция глюконеогенеза осуществляется реципрокно с реакциями гликолиза: активация глюконеогенеза, сопровождается ингибированием гликолиза и наоборот. Регуляция обмена глюкозы происходит с участием гормонов и метаболитов, которые изменяют активность и количество регуляторных ферментов гликолиза и глюконеогенеза. Инсулин индуцирует синтез ключевых ферментов гликолиза и репрессирует синтез ключевых ферментов глюконеогенеза. Глюкагон, кортизол и адреналин индуцирует синтез ключевых ферментов глюконеогенеза. Ключевые ферменты гликолиза активируют – АМФ, фруктозо-2,6дф, фруктозо-1,6дф, ингибируют – АТФ, НАДН2, цитрат, жирные кислоты, аланин, АцетилКоА, глюкагон, адреналин. Ключевые ферменты глюконеогенеза активируют – АцетилКоА, глюкагон, ингибируют – АМФ, фруктозо-2,6дф.

Наибольшая активность глюконеогенеза отмечается в печени, меньше в почках и слизистой оболочке кишечника, в них может синтезироваться до 80-100г глюкозы в сутки. В этих органах глюконеогенез идет до конца с образованием свободной глюкозы, которая может выходить из клеток, поддерживая гомеостаз глюкозы в крови. В норме гомеостаз глюкозы в крови обеспечивается глюконеогенезом печени до 80%, почек до 20%.
Небольшая активность глюконеогенеза наблюдается в мышечных тканях, однако из-за отсутствия у них последних ферментов глюконеогенеза, вместо свободной глюкозы образуются только ее производные, которые не способны покинуть клетку. Таким образом, углеводы синтезируются в мышечных тканях только для собственных нужд. Например, в скелетных мышцах и жировой ткани нет глюкозо-6-фосфотазы, продукт глюконеогенеза – глюкозо-6ф. В миокарде и гладких мышцах нет фруктозо-1,6-дифосфотазы, продукт глюконеогенеза – фруктозо-1,6-дф.
Биологическое значение глюконеогенеза. Необходимость поддержание постоянного уровня глюкозы в крови связана с тем что, для многих тканей глюкоза является основным (нервная ткань), а для некоторых единственным (эритроциты) источником энергии. Потребность в синтезе глюкозы объясняется тем что, гликогенолиз печени может самостоятельно обеспечивать гомеостаз глюкозы в крови только в течение 8-12 часов, далее запас гликогена в течение суток почти полностью истощается. В условиях длительного голодания (больше суток) глюконеогенез является единственным источником глюкозы в организме.
Дата добавления: 2017-09-19; просмотров: 68;
источник




