Вирусная инфекция является наиболее неисследованной формой жизни. Ученые описали около пяти тысяч различных вирусов, но есть предположение, что их общее число значительно превосходит эту цифру.
Одним из самых серьезных инфекционных заболеваний, поражающих печень, является гепатит С. Возбудитель заболевания – это РНК-содержащий вирус, который имеет различные квазивиды. Если уничтожается один, на смену ему приходит другой, который обладает большей резистентностью, то есть устойчивостью, к проводимой терапии.
Определить тип вируса с помощью генотипирования является первым шагом, предшествующим лечению. Первый генетический вариант плохо поддается лечению. Он, в свою очередь, подразделяется на генотип 1а и 1б.
Вирусная популяция гепатита С имеет отличные друг от друга типы, которые, в свою очередь, подразделяют на более мелкие субтипы. Рассмотрим, что собой представляет гепатит с генотип 1, а также каковы особенности его лечения.
Механизм развития РНК-содержащего вирус до конца не изучен. Квазивиды первого типа являются настоящими приспособленцами, это значит, что они с легкостью адаптируются в изменяющихся условиях и быстро привыкают к воздействию лекарственных препаратов. РНК-содержащий вирус легко меняет свою антигенную структуру. После проникновения в человеческий организм он начинает мутировать.
Первый генетический вариант делится на два основных субтипа, а именно:
- А – его еще называют американским;
- Б – называется японским.
Несмотря на такие названия, распространены субтипы не только в Америке и Японии, но и по всему миру. Для того чтобы лучше понять, что из себя представляют генотипы первой группы, проведем аналогию с тюльпанами. Эти красивые цветы могут иметь различную окраску: красную, желтую, розовую. То есть в рамках одного сорта имеются различные субтипы. Тот же принцип относится и к РНК-содержащему вирусу.
Среди жителей европейских стран больше распространён субтип 1б, поэтому рассмотрим его немного детальнее:
- высокие риски перехода острой формы в хронический процесс;
- примерно в тридцати процентах случаев развивается цирроз печени;
- в пятнадцати процентах случаев развивается гепаттоцеллюлярная карцинома;
- вероятность развития внепеченочных осложнений, в частности, воспаление стенки кровеносных сосудов и опухолевые процессы лимфатической системы;
- в более половине случаев наблюдается стойкий вирусологический ответ.
В человеческий организм РНК-содержащий вирус может проникнуть следующим образом:
- переливание крови;
- нестерильный материал;
- половой контакт;
- во время родовой деятельности от матери ребенку.
В группе риска находятся наркоманы. Гепатит С в большей степени является гемоконтактной инфекцией, то есть для заражения необходима кровь больного. После проникновения вирусной инфекции в рану происходит его быстрое распространение по всему организму. В итоге возбудитель заболевания вызывает гибель печеночных клеток. Болезнетворные микроорганизмы угнетают работу иммунной системы и подавляют действие многих лекарственных препаратов.
Клиническая симптоматика первого генотипа не имеет характерных симптомов, которые бы отличали его от других генетических вариантов. В большинстве своем заболевание протекает бессимптомно. Пациенты могут предъявлять жалобы через десять, а то и двадцать лет после заражения.
По мере развития патологического процесса появляются следующие симптомы:
- боль в районе эпигастрия и правого подреберья, которая усиливается после приема еды и физической активности;
- метеоризм;
- диарея;
- приступ тошноты, рвота;
- повышенная температура;
- ухудшение аппетита;
- истощение организма на фоне снижения веса;
- снижение устойчивости к физическим нагрузкам;
- увеличение печени и селезенки в размерах;
- потемнение мочи и осветление кала;
- желтушность склер и кожных покровов;
- вялость, слабость, снижение работоспособности;
- зуд кожных покровов;
- неприятный запах изо рта, изменение вкуса в ротовой полости.
Клиническая картина может отличаться в зависимости от фазы инфекционного процесса:
- Первичный этап . Это острый процесс, возникающий после воздействия вирусной инфекции. Симптомы могут быть стертыми или же ярко выраженными. Часто наблюдаются астеновегетативные признаки, при которых больной чувствует слабость, головокружение, повышенную усталость. Первичный этап длится около шести месяцев. В тридцати процентах случаев наступает выздоровление.
- Носительство . Это значит, что организм заражен, но отсутствуют клинические проявления. Есть вероятность самоизлечения, когда вирус покидает организм. В противном случае вирусоноситель становится источником заражения других людей. Эта инфекционная стадия может длиться несколько лет.
- Латентная фаза . Еще ее называют бессимптомной формой. Именно из-за нее гепатит С также называют ласковым убийцей. РНК-вирус поражает гепатоциты, а человек даже это и не подозревает. Болезнь характеризуется внепеченочными осложнениями.
- Клиническая стадия . Она может наступить спустя несколько лет после инфицирования. Сколько живут люди при гепатите С? Ответ на этот вопрос во многом зависит от состояния иммунной системы и наличия сопутствующих осложнений.
С помощью определения маркеров наличия вируса можно поставить точный диагноз. Идентификация генетического варианта необходима для подбора лечебной тактики. Обследование включает в себя следующее:
- биохимический анализ крови;
- иммуноферментное исследование;
- общий анализ мочи и крови;
- полимеразная цепная реакция;
- ультразвуковая диагностика органов брюшной полости;
- биопсия для исключения цирроза.
Подбор лечебной терапии – это задача лечащего врача, самолечение может привести к серьезным последствиям. На вопрос о том, чем лечить гепатит С, вам ответит специалист после результатов исследования.
Больным, которые еще не проходили лечение по поводу гепатита С, рекомендована комбинация следующих препаратов: пегилированный интерферон,Рибавирин, ингибитор протеазы (боцепривир, телапревир).
Клинические исследования показывают, что при отсутствии эффекта после применения интерферона и Рибавирина, а также при наличии цирроза и фиброза, хорошие результаты дают такие схемы лечения гепатита С: Даклатасвир + Асунапревир (на протяжении трех месяцев), Даклатасвир + Софосбувир (в течение 12 недель).
источник
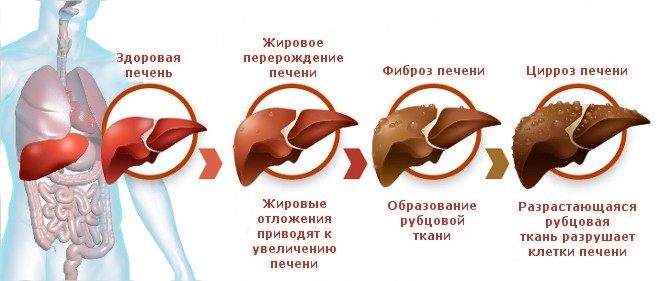
Цирроз печени – это последняя стадия различных хронических заболеваний, которые приводят к прогрессирующей гибели ее клеток. Этот диагноз ставят, когда изменения уже необратимы и затрагивают большую площадь.
Кратко процесс развития заболевания заключается в гибели гепатоцитов, организм замещает погибшие клетки печени соединительной тканью, которая не выполняет функции по очистке организма от различных токсинов и наступает тяжелая интоксикация.
Гибель клеток печени – это процесс не одного месяца, заболевание прогрессирует постепенно, захватывая новые участки здоровых тканей. Длительное время патологические изменения могут никак себя не проявлять, особенно если развивается цирроз, причиной которого стал гепатит С. Клинически протекание гепатита и цирроза тесно взаимосвязано. Цирроз печени – это осложнение после перенесенного гепатита С.
Наиболее распространенными причинами возникновения цирроза печени можно считать:
- хронический вирусный гепатит С и В;
- алкоголизм;
- гепатоз (жировая болезнь печени);
- бесконтрольный прием противоревматических медикаментов.
Гепатит С с исходом в цирроз печени – это причина более 27% случаев патологического изменения печени по всему миру.
Пациент при циррозе печени и гепатите С может жаловаться на:
- вялость, быструю утомляемость;
- снижение работоспособности;
- во рту появляется горечь и сухость, особенно по утрам;
- сонное состояние в дневное время суток, ощущение постоянного недосыпа;
- нарушение когнитивных функций – забывчивость, потеря концентрации при выполнении рабочих задач.
- расстройства пищеварения – диспепсия, боли и чувство тяжести в животе периодического характера, повышенное газообразование;
- потеря веса;
- бесцветные ногтевые пластины;
- субфебрильная температура.
Внешние проявления, симптомы цирроза:
- покраснения кожных покровов на ладонях и стопах;
- сосудистые звездочки;
- наблюдается потеря волос в подмышечной и лобковой области;
- фаланги пальцев становятся похожи на барабанные палочки.
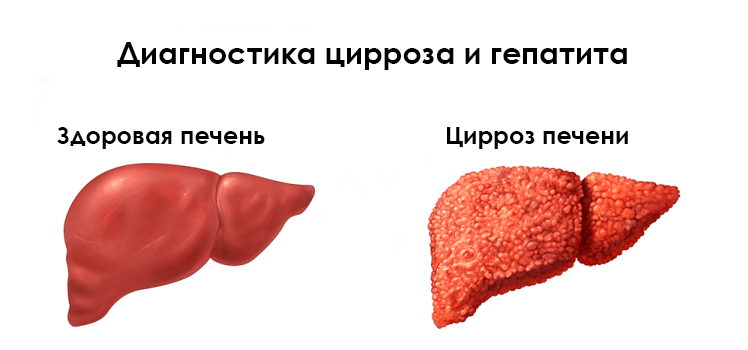
Диагноз цирроз ставиться на основании не только симптомов, но и после получения результатов исследований, при подозрении на вирусную инфекцию – хронический гепатит и цирроз печени, проводятся лабораторные исследования:
- Общий анализ крови – определение уровня лейкоцитов, гемоглобина, СОЭ. По показателям можно будет дать оценку общего состояния организма.
- Биохимия крови – помогает понять на какой стадии находится разрушение печени, помогают в этом показатели билирубина, фосфатазы, определение трансминаз (АЛТ, АСТ).
- Исследование уровня гамма-глобулина – повышенный уровень говорит о циррозе.
- Анти-HCV, анти-HBV – дает понимание о присутствии вируса гепатита Ц в организме.
- ПЦР – анализ полимеразной цепной реакции, помогает выявить присутствие РНК вируса гепатита С, который и стал причиной цирроза печени.
Кроме лабораторных анализов крови используются следующие аппаратные методики:
- Компьютерная томография – дает наиболее точное представление о состоянии печени.
- Биопсия – из печени берется небольшая ее часть, этот метод позволяет в полной мере оценить стадию развития заболевания (наличие некроза и фиброза), ее причины.
- УЗИ – помогает оценить размеры печени и селезенки, увидеть есть ли фиброзная ткань.
Принято выделять три основные стадии в прогрессировании цирроза печени и гепатита С:
- Компенсированная – яркая симптоматика цирроза отсутствует, уцелевшие клетки активно работают, стараясь заменить погибшие.
- Субкомпенсированная – появляются первые признаки цирроза, описанные выше.
- Декомпенсированная – поражены уже значительные области печени, компенсационные механизмы небольшого числа здоровых клеток уже не справляются со своей работой. На этой стадии печеночная недостаточность нарастает, сильнее проявляются признаки энцефалопатии, асцита, желтухи, анемии и атрофии мышц. Этой стадии присущи такие осложнения как: печеночная кома, тромбозы вен, кровотечения, инфекционные процессы, связка гепатит – цирроз – рак здесь проявляется в полной мере.
Основное отличие компенсированного от декомпенсированного цирроза печени и гепатита С – это то, что на первой стадии процесс разрушения печени можно довольно быстро повернуть вспять. Для этого нужно вначале полностью вылечить гепатит, а затем уже заниматься восстановлением функций печени.
Прогноз длительности жизни при компенсированном циррозе и гепатите С в стадии ремиссии обычно благоприятный.
Декомпенсированный цирроз отличает развитие осложнений, протекающих в тяжелой форме – гипертензия портальных вен, увеличение селезенки, как следствие, кровотечения, накопление лишней жидкости в брюшине.
Последствия прогрессирующего цирроза, отягощенного гепатитом С могут проявляться как:
- Острая печеночная недостаточность – необходима интенсивная терапия, внутривенное введение альбумина.
- Асцит – жидкость просачивается в брюшину из-за портальной гипертензии.
- Бактериальный перитонит – когда скопившаяся жидкость в брюшной полости инфицируется патогенной микрофлорой. Температура тела может подниматься до опасных 40 градусов, пациент ощущает сильный болевой синдром в абдоминальной области.
- Печеночная энцефалопатия – вначале головная боль, усталость, заторможенность, затем может прогрессировать и закончиться комой.
- Кровотечение варикозных вен пищевода.
Цирроз при наличии гепатита С можно скорректировать, но все зависит от стадии заболевания. Однако в любом случае нужно вылечить гепатит С, затем начинать восстановление работоспособности печени.
Интересно знать! В Шотландии с апреля 2014 по март 2017 было проведено исследование, которое нашло поддержку на государственном уровне. Пациентам общим числом 4800 человек с хроническим гепатитом С и компенсированным циррозом было назначено лечение прямыми противовирусными препаратами. В итоге у 94% был зарегистрирован устойчивый вирусологический ответ. И по сравнению со статистикой предыдущих лет на 29% снизилось число случаев развития декомпенсированного цирроза, среди больных с диагнозом – хронический гепатит С.
Полностью избавиться от присутствия в организме вирусных вирионов гепатита можно при помощи комбинированной терапии прямыми противовирусными препаратами – Софосбувир, Даклатасвир, Велпатасвир, Ледиспавир.
При компенсированном циррозе и гепатите С, в стадии ремиссии, используется следующее терапевтическое лечение:
- назначение лекарственных средств на основе уродезоксихолевой кислоты;
- применение фосфолипидных препаратов;
- при асците используются диуретики;
- энцефалопатия предполагает коррекцию состояния седативными и противосудорожными медикаментами.
Кроме медикаментозной терапии, назначается диета при циррозе и гепатите С. Ее основу составляет ограничение белка и соли. Чтобы в организм поступало достаточное количество питательных веществ в рационе должны присутствовать овощи, фрукты, злаки и крупяные продукты. Привычное меню – жареное, консервированное, жирное, бобовые, кислые ягоды и фрукты, кофе, чай, находятся под запретом.
Необходимо придерживаться здорового образа жизни (прогулки, плавание), полностью отказаться от алкоголя и табачных изделий.
При декомпенсированном циррозе и гепатите 100% поможет трансплантация донорской печени, до проведения операции ее работу нужно поддерживать такими же методами как при компенсированной стадии.
Сколько живут при циррозе и гепатите С? Ответом на этот вопрос будет – долгие годы, при своевременном начале лечения прямыми противовирусными препаратами и соблюдении рекомендаций специалистов.
Как вылечиться от гепатита C навсегда?
Препараты нового поколения Софосбувир и Даклатасвир, а также Велпатасвир, Ледипасвир способны с 98-100% вероятностью навсегда излечить вас от гепатита C. Современные лекарства можно приобрести в России у официального представителя индийской фармкомпании Zydus Heptiza.
Получите бесплатную консультацию по применению новейших препаратов и узнайте о способах приобретения на официальном сайте поставщика Zydus в России. Читать далее. >>
источник
Понятия «гепатит С» и «цирроз» часто объединяют потому, что оба этих заболевания печени считаются плохо излечимыми. Хронический вирусный гепатит часто протекает в латентной форме, а через несколько лет нередко осложняется циррозом. Узнав о патологиях, больные и родственники сразу интересуются, можно ли вылечить цирроза печени, возникшем на фоне гепатита С. Однозначный ответ дать сложно.
Прогноз продолжительности жизни человека зависит от ряда факторов: времени выявления заболевания, сопутствующих патологий, состояния иммунной системы. На развитие патологии влияет поведение больного, его вкусовые пристрастия, вредные привычки. В 20% случаях организм перебарывает гепатит С, цирроз излечим на стадии компенсации. Для борьбы с патологией применяются хирургические методы, народная медицина. Нельзя отчаиваться при диагностировании гепатита С, осложненного циррозом.
Гепатит С часто называют предвестником цирроза, для этого есть основания. Когда пораженные вирусом гепатоциты погибают, их место занимает соединительная ткань, на паренхиме образуются рубцы. Циррозом заболевают не все инфицированные гепатитом С, а только каждый четвертый. Одновременно гепатит С и цирроз чаще диагностируют:
- у мужчин, это связано с физиологическим особенностями и образом жизни;
- людей, старше 45 лет, когда начинаются гормональные сбои возрастного характера;
- лиц, злоупотребляющих алкоголем, наркоманов – токсическое поражение этанолом приводит к поражению функциональной ткани печени;
- ВИЧ-инфицированных, иммунитет не справляется с вирусом гепатита С, поэтому болезнь переходит в цирроз;
- больных с повышенным уровня железа в крови.
Почему-то люди, далекие от медицины, считают, что гепатит С это вид цирроза печени. По причинам возникновения, морфологической форме, последствиям они различны. Вирус гепатита С передается гематогенным путем. Хватит небольшого количества компонентов зараженной крови, чтобы заболеть. Заразиться им можно:
- при пользовании общими предметами быта, которые способны травмировать кожу (бритва, ножницы;
- когда не обработаны инструменты в стоматологических кабинетах, салонах, оказывающих услуги, связанные с возможными повреждениями кожных покровов;
- через один шприц при инъекции;
- при незащищенном половом контакте;
- при случайном попадании зараженной крови на травмированные участки кожных покровов.
Вирус гепатита С, попав в кровоток через стенки кишечника, размножается в тканях печени. Для гепатита С свойственен инкубационный период. Заболевание проходит в острой или хронической форме. Выздоровление наступает, когда организм вырабатывает антитела к вирусу. Поражения паренхимы обратимые, со временем поврежденные гепатоциты восстанавливаются.
Цирроз – необратимое патологическое изменение печени, когда здоровая функциональная ткань повреждается, на ее месте образуются рубцы. Пораженные участки убирают хирургическим путем. Они не восстанавливаются. Цирроз неизлечим, его только приостанавливают. Он возникает на фоне поражений, вызванных гепатитом С и по другим причинам.
Вначале заболевание протекает бессимптомно, очаги поражения уже есть, но функции паренхимы угасают постепенно. Когда нарастает интоксикация, появляется:
- общая слабость;
- повышенная усталость;
- раздражительность;
- иногда возникает дискомфорт с правой стороны живота;
- возникают расстройства пищеварения, метеоризм;
- головная боль.
На следующей стадии цирроза болезнь становится узнаваема. Специфические признаки печеночной патологии:
- пожелтение кожи;
- потеря мышечной массы;
- кожный зуд из-за избытка билирубина в крови;
- кровоточивость назальной слизистой и десен;
- болевой синдром.
На стадии декомпенсации больной меняется внешне:
- изменяются верхние фаланги пальцев рук и ног, это называется эффектом барабанных палочек;
- возникает водянка (асцит);
- на животе проступает венозный рисунок (голова медузы);
- кожа истончается, становится прозрачной.
При раннем выявлении цирроз приостанавливают. Больной обязан изменить образ жизни, чтобы не провоцировать рост очагов поражения. При дальнейшем развитии некротического процесса возможно лечение хирургическими способами, кардинальный – трансплантация части здорового органа.
При плохом состоянии здоровья больного поддерживают медикаментами в условиях стационара, проводят физиотерапевтические процедуры. Дома больные лечатся с применением методов народной медицины, придерживаются лечебного питания, здорового образа жизни. Нужны физические нагрузки: умеренные, но регулярные. От вредных привычек придется отказаться до конца жизни.
Больному назначаются препараты различных фармакологических групп:
- Интерферон и его аналоги для стимуляции организма в борьбе с вирусом;
- противовирусные средства нового поколения Софосбувир, Даклатасвир, Ледипасвир, их принимают комплексно, в зависимости от генотипа вируса гепатита;
- мочегонные для снятия отеков и улучшения микроциркуляции крови;
- желчегонные для лучшей эвакуации желчи;
- витаминные комплексы;
- гепатопротекторы, поддерживающие здоровые гепатоциты;
- кортикостероиды группы кортизонов, они останавливают образование рубцов на паренхиме;
- блокаторы выработки гистамина, чтобы избежать аллергических реакций;
- альбумин содержащие препараты для восстановления уровня белка в крови назначаются при асците;
- противоварикозные средства нужны, если у больного диагностируется портальная гипертензия.
Больным рекомендуется стол № 5 по Певзнеру, в тяжелых случаях – № 5 а. Запрещена вредная пища:
- жареная;
- копченая;
- жирная (нельзя субпродукты, гусятину, жирную свинину и говядину);
- с красителями, консервантами, другой пищевой химией;
- вызывающая газообразование (бобовые, грубая клетчатка);
- нельзя пить алкоголь, газированные напитки, есть сладости, сдобу.
В сутки потребляют до 2600 калорий. Дневной рацион делят на пять частей: завтрак, ланч, обед, полдник, ужин. В еде должно быть много белка, витаминов и микроэлементов. Рекомендуется напиток шиповника, он обладает комплексным оздоровительным действием, прекрасно пополняет рацион. Нужны молочные продукты, яйца разрешается в сыром виде, всмятку, можно омлеты.
Фитолечение основано на применении витаминных компонентов, мочегонных, желчегонных трав. Расторопша, Пол пала содержат вещества, используемые при производстве гепатопротекторов. Допустимы сборы с антисептическими противовоспалительными растительными средствами.
Самолечение народными средствами недопустимо, нужно принимать водные настойки, отвары, порошки только по рекомендации врача. Некоторые травы, используемые для лечения печеночных заболеваний, содержат яды. При некротической патологии их принимать не рекомендуют.
Состояние больного не позволяет ему полноценно трудиться, он оформляет группу инвалидности. Степень нетрудоспособности зависит от нескольких факторов:
- лечится ли цирроз печени при гепатите на стадии выявления или больного просто поддерживают медикаментозно;
- в каком объеме поражена паренхима;
- как быстро развивается процесс некротического перерождения;
- общее состояние организма;
- наличие осложнений и сопутствующих заболеваний.
На стадии компенсации делаются ограничения трудоспособности (III группа), больному противопоказаны:
- сидячая работа;
- большие физические нагрузки.
Ежегодно пациенты проходят обследование для подтверждения группы. Пожизненная дается только при серьезных осложнениях, когда нагрузка приводит к летальному исходу.
Тяжесть некротического перерождения печени зависит от разновидности штамма вируса. Чаще всего встречаются генотипы 2,3, они быстро поддаются лечению. Генотип 1в более устойчивый к противовирусным препаратам.
Гепатоциты быстрее восстанавливаются у людей, не имеющих хронических заболеваний. С возрастом патологию лечить труднее. Если поражено более 50% паренхимы, возможна трансплантация. В этом случае от цирроза, сопровождаемого вирусом, удается избавиться. Шансы на выздоровление при раннем выявлении патологии. Во всех других случаях перерождение печени необратимо.
Прогрессирующая патология сопровождается следующими осложнениями:
- кровотечением из варикозно расширенных вен пищевода;
- энцефалопатией – поражением головного мозга и центральной нервной системы;
- асцитом или водянкой, когда в животе скапливается жидкость.
- Все эти осложнения становятся причиной летального исхода в течение от года до трех лет. Шансы благоприятного прогноза продолжительности жизни для людей с патологией печени зависят:
- от возраста пациента;
- стадии развития заболевания;
- хронических заболеваний.
На 1 стадии при лечении живут минимум 10 лет. На второй пятилетний порог преодолевают не более 50% пациентов. На последней средняя продолжительность 1–3 года. При осложнения она уменьшается.
источник
Ретроспективное изучение хронического гепатита С (ХГ С) позволяет говорить, что в среднем у 20% больных в течение 20–30 лет развивается цирроз печени (ЦП). Скорость формирования цирроза зависит от ряда факторов.
Ретроспективное изучение хронического гепатита С (ХГ С) позволяет говорить, что в среднем у 20% больных в течение 20–30 лет развивается цирроз печени (ЦП). Скорость формирования цирроза зависит от ряда факторов. Медленное нарастание фиброза при ХГ С наблюдается у женщин молодого возраста в отсутствие таких факторов, как стеатоз печени, синдром перегрузки железом, злоупотребление алкоголем. Ряд причин обусловливает быстрое формирование ЦП: пожилой возраст при инфицировании, мужской пол, систематическое употребление алкоголя более 50 г/сут, наличие коинфекции вирусов гепатита В и/или ВИЧ, избыточная масса тела (> 28 кг/мІ), гетерогенность по гену гемохроматоза, полиморфизм генов ряда цитокинов, играющих ключевую роль в фиброгенезе. Среднее время развития ЦП у лиц, инфицированных в возрасте после 40 лет и злоупотребляющих алкоголем, составляет 13 лет, а у молодых женщин в отсутствие приема алкоголя ЦП формируется через 42 года. У 32% больных ХГ С протекает стабильно и не сопровождается прогрессированием болезни.
Важным фактором фиброгенеза является сохраняющаяся активность ХГ С по лабораторным данным и морфологическим признакам. У больных со стойко нормальным уровнем трансаминаз сыворотки риск развития ЦП С составляет 5%, в то время как наличие 3–5-кратного повышения АЛТ сыворотки ассоциируется с быстрым формированием ЦП С у 50% больных. Показано также, что факторами риска прогрессирования фиброза являются: наличие фиброза в ткани печени при первой биопсии, стеатоз печени и возраст больных. Быстрота прогрессирования фиброза определяется предшествующим фиброзом, стеатозом и лобулярным гепатитом [1]. При ХГ С низкой степени активности (ИГА по Knodell 4–8 баллов) риску развития ЦП С подвержены 7–10% больных, при ХГ С высокой степени активности (ИГА — более 13 баллов) у 71% больных цирроз может развиться уже через 7 лет. Проспективное изучение 404 больных компенсированным ЦП С показало, что за 85,7±36 мес наблюдения у 28% больных развивается хотя бы одно осложнение ЦП С, в том числе гепатоцеллюлярная карцинома (ГЦК) — у 19%, асцит — у 17%, кровотечение из варикозно расширенных вен пищевода (ВРВП) — у 5%, декомпенсация ЦП С (Чайлд В/С) — у 17%, энцефалопатия — у 2% [2].
Высокая частота развития ЦП С при хронической HCV-инфекции и риск серьезных осложнений в этой группе больных определяют задачи противовирусной терапии (ПВТ). Основная задача лечения — эрадикация вируса гепатита С и достижение стойкой ремиссии ХГ С, однако возможности достижения устойчивого вирусологического ответа (УВО) у больных ЦП С значительно ниже, чем при ХГ С. Исследования последних лет показали, что ПВТ способствует уменьшению выраженности фиброза, поэтому у больных ЦП С без вирусологического ответа целью противовирусного лечения является замедление прогрессирования болезни, снижение риска декомпенсации ЦП и развития его осложнений, в том числе ГЦК, В-клеточной лимфомы, криоглобулинемии, внепеченочных проявлений, портальной гипертензии и печеночно-клеточной недостаточности.
Представляют интерес исследования M. Curry и соавторов (2005), изучивших влияние длительной терапии пегинтерфероном α-2b в малых дозах на динамику портальной гипертензии у больных ХГ С со стадией фиброза F3 и ЦП С (F4). В исследование COPILOT были включены 267 больных, получавших колхицин 0,6 мг 2 раза в день, и 270 больных, которым проводится лечение пегинтроном 0,5 мкг/кг 1 раз в неделю в течение 4 лет. Обе группы были представлены больными, не ответившими на комбинированную терапию интерфероном и рибавирином. 83% больных в каждой группе имели ЦП С, у 40% из них имелись признаки портальной гипертензии, выявленные при эндоскопии (ВРВП или портальная гастропатия). ЭГДС проводилась с интервалом в 2 года. Опубликованы предварительные результаты исследования.
У 5 больных ЦП С, не получавших β-блокаторы с целью коррекции портальной гипертензии, до лечения пегинтроном провели измерение портального давления. Спустя 2 года лечения при повторной ЭГДС новые ВРВП появились у 11 из 66 больных, получавших колхицин, и сохранялись у 5 из 66 больных, получавших монотерапию пегинтроном. У всех 5 больных первоначальное портальное давление составляло 15 мм рт. ст., через 24 нед лечения составило в среднем 6 мм рт. ст. Кровотечение из ВРВП через 2 года отмечено у 11 (9%) больных, получавших колхицин, и у одного (1%) больного, получавшего пегинтрон. Асцит и печеночно-клеточная недостаточность также чаще выявлялись при лечении колхицином (20 больных), чем пегинтроном (13 больных). Таким образом, длительное лечение малыми дозами пегинтрона больных ЦП С может замедлить формирование ВРВП, снизить портальное давление, предотвратить кровотечение из ВРВП и другие осложнения портальной гипертензии у больных ЦП С, не достигших УВО на предшествующую комбинированную терапию интерфероном и рибавирином [3].
В последние годы ПВТ претерпела существенные изменения: с 2000 г. комбинированная терапия пегилированными интерферонами α-2a и 2b и рибавирином заняла ведущие позиции в лечении ХГ С и компенсированного ЦП С. Изучены прогностические факторы ответа на лечение, появились возможности коррекции ряда побочных эффектов ПВТ, что позволило достичь УВО у 56–63% больных ХГ С, включенных в лечение. Приверженность больных к лечению, адекватные дозы препаратов и длительность ПВТ позволяют повысить УВО до 72–75% [4, 5]. Наибольший эффект комбинированной терапии ХГ С отмечается у больных с генотипами 2 или 3 HCV: непродолжительный курс лечения (24 нед) при высокой приверженности к лечению пегилированными ИФН α и рибавирином позволяет достичь успеха в 84–94% случаев.
Повышению эффективности ПВТ способствуют обязательное назначение комбинированной ПВТ (ИФН α и рибавирин) первичным больным, выбор оптимальных доз препаратов и длительности лечения в зависимости от генотипа HCV и вирусной нагрузки. Кроме того, необходима коррекция факторов неблагоприятного ответа на лечение (стеатоз, холестаз, синдром перегрузки железом) и побочных эффектов ПВТ (депрессия, гемолитическая анемия при применении рибавирина, лейко- и тромбоцитопения при лечении ИФН α, дисфункция щитовидной железы). Субоптимальные дозы препаратов, используемых при проведении ПВТ, и недостаточная продолжительность лечения способствуют формированию группы резистентных к противовирусной терапии больных ХГ С, что делает необходимым проведение повторных курсов ПВТ. Так, было показано, что при 48-недельной комбинированной ПВТ УВО достигалось у 72% больных с генотипом 1b HCV и низкой вирусной нагрузкой. Последующее обострение ХГ С отмечалось у 3% пациентов. В то же время при 24-недельной ПВТ УВО отмечался только у 51% больных указанной категории, причем обострение ХГ С и возобновление виремии через 6–18 мес после окончания ПВТ наблюдались у 40% пациентов.
Несмотря на достижения последних лет, остаются категории трудных для лечения больных ХГ С, к которым относятся пациенты с генотипом 1 HCV и высокой вирусной нагрузкой и больные ЦП С.
Генотип 1 HCV и высокая вирусная нагрузка оказались независимыми прогностическими факторами слабого ответа на лечение. Причины этого до конца не ясны. Изучается значение мутаций в E2 и NS5A генах HCV (неструктурный регион NS5A определяет чувствительность к интерферону). Элиминация гепатоцитов, инфицированных генотипом 1 HCV, в процессе ПВТ происходит медленнее, чем при других генотипах. В первые 1–2 нед терапии вирусная нагрузка снижается на 1,6 log копий/мл при генотипе 1 HCV и на 2,9 log копий/мл при генотипе 2. Скорость гибели инфицированных гепатоцитов составляет 0,1 в день у больных с генотипом 1 и 0,26 в день при генотипе 2, что объясняется различиями в иммунном ответе у больных и дает основание для обсуждения необходимости более агрессивной и, возможно, более длительной ПВТ при генотипе 1 HCV [5].
Стратегия лечения больных ЦП и ХГ С, инфицированных генотипом 1 HCV и имеющих высокую вирусную нагрузку, тесно связана. УВО при лечении ИФН α в стандартном режиме больных ХГ С с генотипом 1 HCV не превышает 10% независимо от сроков лечения — 24 или 48 нед. При использовании комбинированной терапии (ИФН α/рибавирин) в течение 48 нед УВО у таких больных возрастает до 28–36%, оставаясь значительно ниже УВО при генотипах 2 и 3 HCV (64–79%). Лечение ХГ С с генотипом 1 HCV в течение 48 нед дает более высокие результаты (46–52%), чем 24 нед (29–42%). Таким образом, генотип вируса HCV определяет стратегию ПВТ ХГ С и ЦП С.
Уровень вирусной нагрузки, как и генотип вируса, не влияет на вариант и тяжесть течения ХГ C. Высокая вирусная нагрузка (более 2х10 6 копий/мл или более 800 000 МЕ/мл) может быть выявлена при хроническом гепатите низкой, умеренной, высокой степени активности, при минимальных изменениях в печени или при ЦП С. Однако уровень виремии отчетливо влияет на частоту достижения УВО: пегилированный ИФН α-2b 1,5 мкг/кг 1 раз в неделю в комбинации с рибавирином в дозе 800 мг/сут при высокой вирусной нагрузке обеспечивает УВО в 42% случаев, а при низкой — в 78%.
В последние годы разработан метод оценки успеха терапии на основании изучения вирусной кинетики на ранней стадии ПВТ. Ранний вирусологический ответ позволяет прогнозировать УВО. Высокая приверженность больных ХГ C к лечению и оценка прогноза ПВТ на основании данных раннего вирусологического ответа на 4-й или 12-й неделе позволили повысить результативность терапии в группе всех леченных больных ХГ С до 90%. Отказ от стандартных схем лечения ИФН α (3 млн МЕ 3 раза в нед) с переходом на комбинированную ПВТ также способствует повышению количества больных с ранним вирусологическим ответом.
Изучение раннего вирусологического ответа на основании количественного анализа HCV-РНК с помощью высокочувствительной ПЦР позволяет идентифицировать больных, которые не ответят на ПВТ. Если после 12-недельной ПВТ пегилированными ИФН α и рибавирином уровень HCV-РНК снизился на два и более десятичных логарифмов, но РНК вируса по-прежнему выявляется в крови, то целесообразно продолжить ПВТ еще в течение 12 нед, а затем провести повторное исследование HCV-РНК. При его отрицательном результате УВО колеблется от 42 до 78% в зависимости от вирусной нагрузки. Представляется целесообразным 72-недельный курс ПВТ, т. е. продление лечения до 1,5 лет, что позволяет значительно улучшить результаты лечения. При сохраняющейся виремии с падением ее уровня на 12-й неделе менее чем на два десятичных логарифма УВО составляет от 0 до 5%, что позволяет уже на ранних этапах либо отказаться от бесперспективной терапии при генотипе 1 HCV, либо модифицировать ее, либо перейти на поддерживающую терапию пегилированным ИФН α-2а (90 мкг) или ИФН α-2b (0,5 мкг/кг) с целью замедления прогрессирования ЦП С и профилактики развития ГЦК и лимфомы.
Таким образом, генотип 1b и высокая вирусная нагрузка определяют категорию «трудных» для лечения больных ХГ C. В отношении этой группы пациентов необходимо строго следовать правилу применения максимально эффективных доз пегилированных ИФН α-2b (1,5 мкг/кг) или ИФН α-2a (180 мкг) в сочетании с рибавирином в дозе выше 13 мг/кг при продолжительности лечения 48–52 нед. Известно, что пегилированные ИФН α-2a и 2b отличаются друг от друга по фармакокинетике и фармакодинамике. Была проведена независимая сравнительная оценка кинетики вирусологического ответа на пегилированные ИФН α-2a в дозе 180 мкг/нед и ИФН α-2b в дозе 1,5 мкг/кг/нед при их сочетании с рибавирином в дозе 15 мг/кг/сут у первичных больных ХГ C. В конце курса лечения вирусологический ответ на комбинированную терапию пегИФН α-2a/рибавирином и пегИФН α-2b/рибавирином у пациентов с генотипом 1 HCV составил 55% и 76% соответственно, что позволяет рекомендовать применение пегИФН α-2b в составе комбинированной ПВТ у данной категории больных [6]. В настоящее время ряд авторов предлагают оценивать ранний вирусологический ответ на 4-й неделе и при отсутствии вирусологического ответа модифицировать лечение. Используется индукционная терапия пегилированным ИФН α-2b в дозе 3 мкг/кг/нед в течение 4 неделе или 2 мкг/кг/нед в течение 8 нед с последующим применением препарата в дозе 1,5–1,0 мкг/кг/нед.
Тройная схема комбинированной ПВТ с включением помимо пегилированного ИФН α и рибавирина 200 мг амантадина не имеет преимуществ перед обычной схемой в лечении ХГ C генотипа 1b с высокой вирусной нагрузкой.
В 2004 г. опубликованы предварительные результаты лечения больных с генотипом 1 HCV и высокой вирусной нагрузкой, не ответивших на первый курс ПВТ ИФН α и рибавирином, комбинацией α-тимозина-1 (1,6 мг 2 раза в неделю подкожно), пегилированного ИФН α-2a (180 мкг в неделю) и рибавирина (1000–1200 мг/сут) в течение 24 недель. Ранний вирусологический ответ на 12-й неделе лечения достигнут у 47,8% больных, вирусологический ответ после 24 нед терапии сохранялся у 39,1% пациентов ХГ C, представляющих «трудную» для лечения группу. Дополнительный препарат (α-тимозин-1) не добавлял новых побочных эффектов и хорошо переносился больными.
Новые стратегии в лечении «трудных» больных с генотипом 1 HCV и высокой вирусной нагрузкой включают продление сроков комбинированной ПВТ до 72 нед у пациентов, не достигших раннего вирусологического ответа на 4-й неделе, что позволяет повысить УВО с 22% (при 48-недельной терапии) до 51% и снизить частоту обострений [7].
Обоснованием для лечения ХГ C с продвинутой стадией фиброза или сформировавшимся ЦП С стали данные о снижении риска декомпенсации ЦП и развития ГЦК, а также регрессе фиброза у 60% больных, получающих ПВТ. Наличие портального фиброза или ЦП С считается независимым фактором низкой частоты УВО у HCV-инфицированных больных. Пациенты с ЦП C обычно плохо отвечают на стандартную монотерапию ИФН α: УВО составляет от 5 до 20%. Эффективность комбинированной терапии ИФН α и рибавирином составила в этой группе 5–29%. Применение пегилированных ИФН α в составе комбинированной терапии компенсированного ЦП C или ХГ С с мостовидным фиброзом позволило повысить УВО до 44–50%.
Следует отметить, что даже при монотерапии пегилированным ИФН α можно достигнуть гистологического улучшения у 54% больных компенсированным ЦП С. В сравнительном исследовании эффективности пегилированных ИФН α-2a и 2b у больных ЦП C наличие мостовидного фиброза являлось отрицательным прогностическим фактором достижения раннего вирусологического ответа. В конце 24-недельной ПВТ вирусологический ответ в 1-й группе больных ЦП C составил 83%, во 2-й — 60%. Таким образом, пегилированный ИФН α-2a может быть препаратом выбора в комбинированной терапии ЦП C [8]. Даже при отсутствии вирусологического ответа на комбинированную ПВТ при ЦП C отмечается улучшение гистологической картины в печени (снижение ИГА и ГИС).
Наиболее значимое улучшение морфологических данных имеет место при достижении УВО, что сопровождается улучшением качества жизни больных ЦП С, несмотря на наличие продвинутой стадии болезни. Интерес представляют данные Poynard и соавторов (2000), наблюдавших 3010 больных ХГ С с повторной биопсией печени (до начала ПВТ и спустя 6–12 мес после ее окончания) при использовании различных режимов лечения: монотерапии ИФН α-2b, комбинированной ПВТ ИФН α или пегилированным ИФН α-2b и рибавирином в течение 48 нед. Более чем у трети больных, у которых был достигнут УВО, улучшилась гистологическая картина (ГИС и ИГА) в печени, морфологическая динамика отмечена также у трети больных без вирусологического ответа [9]. Анализ биопсий печени у больных ХГ С, участвовавших в четырех многоцентровых исследованиях, показал, что у 75 (49%) из 153 пациентов ЦП С после окончания терапии ГИС (уровень фиброза) снизился на 1–3 балла, что позволяет говорить о возможности регресса фиброза при ЦП С под влиянием настойчивой целенаправленной ПВТ [10].
В последние годы предпринимаются попытки противовирусного лечения декомпенсированного ЦП С (Чайлд В и С). Известно, что 40% всех ортотопических трансплантаций печени проводится в связи с ЦП С. Больные с сохраняющейся виремией имеют высокий риск реакций отторжения трансплантата и инфицирования донорской печени вирусом гепатита С с быстрым развитием (в течение 5–7 лет) ЦП С и/или ГЦК в пересаженной печени. В 2003–2004 гг. появились первые публикации использования ПВТ малыми дозами интерферона и рибавирина при декомпенсированном ЦП С у кандидатов на трансплантацию печени. Предлагается начинать лечение ИФН α 3 млн МЕ ежедневно и рибавирином 800 мг/сут за 4 мес до предполагаемой операции. Режим ежедневного введения интерферона позволяет уменьшить частоту гриппоподобного синдрома, лечение в течение 4 мес позволяет добиться максимального снижения виремии (до операции). У 9 (30%) из 30 больных декомпенсированным ЦП С (Чайлд В или С) удалось достичь вирусологического ответа на 12-й неделе, у 6 из них (20%) авиремия сохранялась после трансплантации печени [11]. Аналогичные данные о возможности развития УВО в 18–20% случаев декомпенсированного ЦП С опубликованы рядом авторов, длительность наблюдения за такими больными продолжается более 3,9 лет.
Известно, что употребление алкоголя значительно повышает смертность при вирусных ЦП: пятилетняя выживаемость больных достигает лишь 43%, значительно отличаясь в группах ЦП Чайлд А (66%), Чайлд В (50%) и Чайлд С (25%). При продолжающемся приеме алкоголя риск смерти у больных ЦП С повышается в случае наличия таких факторов, как пожилой возраст, печеночно-клеточная дисфункция (Чайлд В или С), желудочно-кишечное кровотечение, коинфекция (HBV, HCV), курение и отсутствие признаков острого алкогольного гепатита при биопсии печени. Среди механизмов влияния алкоголя на прогрессирование HCV-инфекции отмечают активацию репликации, повышение разнообразия квазивидов и мутаций вируса, усиление апоптоза гепатоцитов, подавление иммунного ответа хозяина, нарастание стеатоза и уровня железа в печени. Все это ведет к быстрому развитию болезни, высокой частоте формирования ЦП С и ГЦК и низкой эффективности интерферонотерапии. Эффективность ПВТ при ХГ С у лиц, употребляющих алкоголь, в 3 раза ниже стандартных показателей УВО: при монотерапии ИФН УВО снижается до 7–8% по сравнению с 25% у больных, не употребляющих алкоголь; при комбинированной терапии — до 12–4% по сравнению с 41%. Не существует безопасных доз алкоголя для больных ХГ С. Рекомендуется полный отказ от его приема за 6 мес до предполагаемой ПВТ, что улучшает результаты противовирусного лечения, однако УВО не достигает показателей, свойственных больным, не употреблявшим алкоголь в прошлом. Возврат к приему алкоголя после окончания ПВТ повышает риск обострения ХГ С и возврата виремии.
У больных ХГ С на стадии цирроза или при наличии мостовидного фиброза (F3) риск развития побочных эффектов интерферонотерапии выше, чем при менее продвинутых стадиях фиброза. Показано, однако, что частота их выявления и необходимость прекращения ПВТ существенно не отличаются в группах больных, леченных пегилированным ИФН α или ИФН α в стандартном режиме. Пегилированный ИФН α-2а обладает более выраженным миелосупрессивным действием, чем ИФН α-2b. Гематологическая токсичность при применении пегилированных ИФН α проявляется в первые 4 нед лечения, затем достигается устойчивый уровень лейкоцитов и тромбоцитов. Особенно быстро их число снижается после первой дозы препаратов. ПВТ назначают больным компенсированным ЦП С с уровнем лейкоцитов 3000/ммЁ и тромбоцитов 50 000/ммЁ. При снижении уровня нейтрофилов до 600/ммЁ, а уровня тромбоцитов до 20 000/ммЁ ИФН α отменяют.
Модификация дозы пегилированного ИФН α или рибавирина (снижение дозы или отмена препарата) в связи с побочными эффектами отмечена у 50% больных ЦП С. В зависимости от достижения раннего вирусологического ответа на 12-й неделе лечения предложены различные варианты лечения ЦП С: продолжение комбинированной терапии в максимально эффективных дозах в течение 36 нед при достижении раннего вирусологического ответа; лечение небольшими дозами пегилированного ИФН α-2b (0,5 мкг/кг) в течение 5 лет при отсутствии такого ответа на 4-й нед (EPIC3) или малыми дозами пегилированного ИФН α-2а (90 мкг) в течение 4 лет (HALT-С).
Определены показания к повторным курсам ПВТ: наличие генотипов 2 или 3 НСV; частичный ответ при предшествующем курсе ПВТ, F3- и F4-стадии фиброза. Противопоказаниями к повторным курсам лечения являются: пожилой возраст, генотип 1, ЦП С с гипербилирубинемией, высокая вирусная нагрузка, высокий индекс массы тела, минимальные изменения в печени при биопсии (ИГА менее 4 баллов) и продолжающееся употребление алкоголя или наркотиков.
Таким образом, ПВТ компенсированного и декомпенсированного ЦП при ХГ С решает ряд следующих задач: замедление декомпенсации цирроза, снижение смертности от его осложнений (кровотечение из варикозно расширенных вен, печеночно-клеточная недостаточность и т. д.), предотвращение развития ГЦК и профилактику реактивации инфекции после трансплантации печени, а также улучшение качества жизни больных и обеспечение их социальной реабилитации. Несомненно, что на ранних стадиях HCV-инфекции ПВТ дает лучшие результаты: частота УВО при лечении острого гепатита С достигает 90%, ХГ С — 60–70%, что превышает эффективность лечения ЦП С пегилированными ИФН α и рибавирином (30–50%). Наш опыт ПВТ ХГ С низкой степени активности позволяет говорить о высокой эффективности лечения данной категории больных. Используя пегилированный ИФН α-2b (1,5 мкг/кг) и рибаверин (более 10,6 мг/кг) при лечении первичных больных с небольшим сроком заболевания (5,9±5,7 лет), преимущественно низкой степени активности и слабым фиброзом (F1), а также низкой вирусной нагрузкой, мы получили устойчивый вирусологический ответ в 86 % случаев, в том числе у 77% пациентов с генотипом 1 HCV, включая 5 больных на стадии ЦП С [12].
- Collier J. D., Woodall T., Wight D. G. D. et al. Predictiv of progressive hepatic fibrosis stage on sabsequent liver biopsy in chronic hepatitis C virus infection. J. Viral Hepatitis, 2005; 12: 74-80.
- Niederau C., Lange S., Heintgest T. et al. Prognosis of chronic Hepatitis C: Results of a Large, Prospective Cohort Study. Hepatology, 1998; 28: 1687-1695.
- Curry M., Cardenas A., Afdhal N. H. Effect of maintenance Peg-Intron therapy on portal hypertension and its complications: results from the COPILOT study. J. Hepatol., 2005; 42 (2): 95.
- Fried M. W., Shiffman M., Reddy R. et al. Peginterferon alfa-2a plus ribavirin for chronic hepatitis C virus infection. N Engl J. Med., 2002; 347: 975-982.
- Manns M., McHutchison J., Gordon S. et al. Peginterferon alfa-2b plus ribavirin compared with interferon alfa-2b plus ribavirin for initial treatment of chronic hepatitis C: a randomized trial. Lancet, 2001; 358: 958-965.
- Luise S., Bernardinello E., Cavalletto L. et al. Kinetic of Virolological Response Duning Peg-IFNS in Chronic Hepatitis C. J. Hepatol 2004; 40 (1): A 490.
- Berg T., von Wagner M., Hinrichsen H. et al. Comparison of 48 or 72 weeks of treatment with pegiterferon alfa-2a (40 KD) (Pegasys) plus ribavirin (Copegus) in treatment-naive patients with chronic hepatitis C infected with HCV genotype 1 [Abstract]. Hepatology 2003; 38 (1): 317A.
- Hadziyannis S. J., Papatheodoridis G. V. Peginterferon-(2a (40 kDa) for chronic hepatitis C. Expert Opin. Pharmacother. 2003; 4:541-551.
- Poynard T., Marcellin P., Lee S. S. et al. Randomised trial of interferon alpha 2b plus ribavirin for 48 weeks or for 24 weeks versus interferon alpha 2b plus placebo for 48 weeks for treatment of chronic infection with hepatitis C virus. Lancet 1998; 352:1426-1432.
- Poynard T., McHutchison J., Manns M. et al. Impact of Pegylated Interferon Alpha-2b and Ribavirin on Liver Fibrosis in Patients with Chronic Hepatitis C. Gastroenterol. 2002; 122: 1303-1313.
- Forns X., Navasa M., Rodes J. Treatment of HCV Infection in Patients With Advanced Cirrhosis. Hepatology, 2004; 40: 498.
- Никулкина Е. Н., Крель П. Е., Лопаткина Т. Н. и др. Комбинированная терапия пегинтерфероном альфа-2b (пегинтроном) и рибавирином (Ребетолом) у первичных больных хроническим гепатитом C // Клиническая фармакология и терапия. — 2004. — № 13 (2). — С. 48-52.
Т. Н. Лопаткина, кандидат медицинских наук, доцент
источник
Болезни органов пищеварения играют весомую роль в медицинской практике. Отдельно выделено направление, которое занимаются непосредственно их изучением и лечением – гастроэнтерология.
Гепатит и цирроз печени, являются основной частью диагнозов у пациентов гастроэнтерологического отделения. Чем отличаются эти две, казалось бы одинаковые, патологии друг от друга расскажет данная статья.
Гепатит – воспаление ткани печени, которое носит как инфекционный, так и неинфекционный характер, а также острое и хроническое течение. Причинами воспаления могут быть:
- вирусы А, В, С, В, Е, F, G;
- алкоголизм (алкоголь индуцированный);
- токсические гепатотропные вещества (мышьяк, сулема, яд бледной поганки, суррогаты алкоголя);
- аутоиммунные процессы;
- неправильное питание;
- медикаменты (противотуберкулезные препараты, седативные средства, тетрациклины);
- застой желчи (холестаз);
- наследственные генные причины;
- невыясненная этиология (идеопатический).
Цирроз – это хронический процесс, при котором нормальные или измененные клетки печени (гепатоциты) погибают и заменятся соединительной тканью. Заболевание является часто осложнением вирусного или хронического гепатита. Приводит к развитию цирроза систематическая алкогольная интоксикация и отравление медикаментами.
Эти два заболевания печени весьма схожи друг с другом и по сути своей одно и то же. Цирроз печени – это следствие неизлеченного гепатита. До появления современных методов диагностики, лапароскопии и прицельной биопсии, проводилась дифференциальную диагностика между этими патологиями.
- Инфекционные и неинфекционные фактор
- Перенесенный острый, а чаще хронический гепатит.
- Токсические провокаторы.
- Развивается неполноценность (недостаточность) гепатоцитов
- Происходит некротическое изменение печеночной клетки, а вместо нее разрастается соединительная ткань, которая неспособна выполнять нужные функции.
- Сохраняется дольковая структура печени с атрофией (изменением) паренхимы.
- Отсутствует дольковое строение органа, замена их ложными дольками, полная перестройка органа.
- Астено-вегетативный синдром (нарушена память, апатия, сонливость), что вызвано нарушением выведения токсических продуктов распада.
- Симптомы расстройства пищеварения (диспептические нарушения) – нарушен аппетит, непереносимость алкоголя, чувство горького во рту, частая рвота, дискомфорт в области печени, живот умерено вздут.
- Синдром застоя желчи (холестаз) – кал теряет окраску, моча становится похожей на темное пиво, кожа и слизистые желтеют.
- Синдром недостаточности функции печени, которой проявляется нарушением выработки важных белков крови (кровоподтеки, отеки тканей).
- Увеличена печень (гепатомегалия), селезенка (спленомегалия).
- Характерны те же признаки, что и для гепатита.
- Синдром портальной гипертензии – это повышение давления в воротной вене, приносящей кровь на очистку в печени из всего желудочно-кишечного тракта. Его проявления:
- Асцит (большой живот, вследствие скопления в ней пропотевшей жидкости, до 10 литров);
- Расширенные вен на животе, которые просвечивают, становятся видными невооруженным глазом («голова медузы»);
- Дилятированы вены желудка, пищевода и прямой кишки, что провоцирует соответственно желудочное, пищеводное, геморроидальное кровотечение.
- Токсическая энцефалопатия (слабоумие).
Из написанного выше, делаем вывод о том, что четкой разницы в клинике двух болезней нет, а признаки цирроза печени наслаиваются на симптоматику гепатита.
Острое воспаление редко, а вот формы хронического гепатита в разном процентом соотношении довольно часто ведут к циррозу печени.
- Острые формы вирусных гепатитов С и В с наибольшей частотой способны к хронизации процесса и в районе 10% к формированию цирротических изменений.
- Агрессивная форма хронического воспаления любой этиологии является злокачественной и в 30 – 60% кинических случаев запускает цирроз.
- Холестатическая форма невирусного воспаления печеночной ткани практически в 100 % случаев порождает цирроз.
Пациенты, которым поставлен диагноз печеночное воспаление той или иной этиологии, часто задают врачам и сами себе этот вопрос, так как он на самом деле щепетильный. Ответ на него прост – нет, не всегда воспалительный процесс в печеночной ткани заканчивается циррозом.
Вирусный гепатит А – доброкачественный вариант болезни, который никогда не приводит к развитию цирроза, а гепатит В только в 1% случаев.
Если вовремя начать лечение, по возможности устранить провоцирующие факторы, то и цирротического перерождения печени не произойдет.
Процесс лечения развившегося цирроза очень сложный, требует грамотного подхода и комплексной терапии.
- Если это возможно – устранить те факторы, которые привели к развитию вначале гепатита, а потом и цирроза (оставить алкоголь, прекратить прием медикаментозных средств и иное).
- Диетотерапия преследует цель облегчения работы печени:
- убрать из рациона жирную еду, а также копчености;
- ограничить белок и поваренную соль;
- увеличить потребление витаминов (на первом месте группа В), овощей и фруктов;
- соблюдать кратность и порционность – небольшое количество 4-5 раз в сутки;
- термический способ обработки – варка, готовка на пару (жарить не рекомендуется).
- Этиотропная терапия (направленная на причину болезни):
| Причина цирроза печени | Лекарственный препарат |
| Гепатиты В, С, D | – противовирусные лекарственные средства: ПЕГ-ИНФ альфа-2а, ПЕГ-ИНФ альф-2b, Рибавирин, Тенофовир, Ламивудин, Симепревир, Омбитасвир, Дасабувир |
| Воспаление печени аутоиммунного характера | – глюкокортикотероидные гормоны: Преднизолон, Метилпреднизолон, Дексаметазон; – цитостатические средства (иммуномодуляторы): Мофетиламикофенолат, Метотрексат, Азатиоприн. |
| Алкогольное воспаление | – витамины группы В (Тиамин (В1, Пиридоксин (В6), Цианокобаламин (В12); – глюкокортикотероидные гормоны: Преднизолон, Метилпреднизолон, Дексаметазон; – вазодилататоры (Пентоксифиллин, Трентал). |
| Воспаление неалкогольного генеза (стеатогепатит) | – ингибиторы липазы (Орлистат) – гипогликемические лекарства (Метформин, Эксенатид); – гиполипидемические средства (Аторвастатин, Розувостатин) |
- Симптоматическая терапия:
- лечение асцита – мочегонные (Спиронолактон, Лазикс, Фуросемид), лапароцентез (пункция живота) по мере накопления жидкости;
- восстановление недостатка белка (Альбумин, Протеин, свежезамороженная плазма);
- терапия геморрагического синдрома (Терлипрессин, Лиоктреотид);
- борьба с сопутствующей инфекцией – назначают антибиотики (Цефатоксим, Цефтриаксон, Ципрофлоксацин, Офлоксацин);
- устранение симптомов печеночной энцефалопатии – L-Орнитин, L-аспартат.
При всех разновидностях цирроза прогноз продолжительности жизни для людей неутешительный и зависит от сложности морфологических изменений, настроенности пациента соблюдать все назначения и совершенства методов терапии. В среднем живут люди от трех до шести, редко до десяти, лет. Большое количество пациентов умирает от осложнения – кровотечения из варикозно-расширенных вен пищевода.
С развитием трансплантологии, у больных циррозом появился шанс получить ворую жизнь – пересадка печени.
Прогнозы у пациентов с гепатитом весьма благоприятные. Можно добиться полного излечения или периода стойкой ремиссии.
Избежать этих заболеваний можно и нужно. Для этого необходимо всего лишь вести здоровый образ жизни, разбираться в половых связях, чтобы не заразится парентеральными гепатитами, правильно питаться и следить за своим здоровьем.
источник