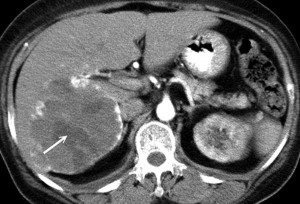
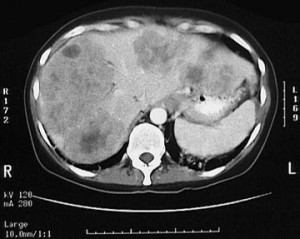
Очаговыми образованиями (или очагами) печени называют единичные или множественные участки изменения ее структуры, которые бывают самого разного происхождения – как доброкачественного, так и злокачественного.
Чаще всего очаги выявляются при УЗИ, но иногда являются случайной находкой при компьютерной томографии или МРТ, когда исследование выполнялось по какой-то иной причине. При этом КТ используется для уточнения размеров, количества, расположения и структуры очагов. При этом по результатам КТ врач, как правило, должен ответить на вопросы о характере изменений: имеем ли мы дело с доброкачественным процессом (например, кистой или гемангиомой), либо злокачественным процессом (рак, метастазы, и т.п.). В ряде случаев после выполнения КТ диагноз остается сомнительным. В таких случаях рекомендуется получить второе медицинское мнение по результатам исследования.
Иногда патологическое образование печени выявляется при сцинтиграфии или ПЭТ (очаг гиперфиксации РФП).
Все объемные образования печени, выявленные при компьютерной томографии, можно разделить в зависимости от следующих параметров:
1) Плотность – характеристика любой ткани организма, которая измеряется на компьютерных томограммах в т.н. единицах Хаунсфилда. В зависимости от рентгеновской плотности очаги бывают гипо-, гипер- и изоденсными по отношению к окружающей нормальной паренхиме. По плотности можно предположить, что находится в структуре очага: кровь, другая жидкость, мягкотканный компонент. Более достоверно выявляются участки обызвествления – кальцинаты.
2) Структура. Кистозные образования подразделяются на одно- и многокамерные; они могут иметь хорошо видимую стенку или не иметь таковой; содержать включения кальция, геморрагическую – гиперденсную – жидкость, гиподенсную жидкость, например, желчь. Внутри можно обнаружить инородное тело или паразита, кистозный или мягкотканный компонент. Также структура может быть однородная или неоднородная, последняя часто объясняется участками некроза. Выявление извести и кальцинатов свидетельствует о длительности процесса.
3) Форма может быть приближенной к шару, вытянутая, неправильная (иррегулярная) и т. д.
4) Контуры. Ровные или неровные, четкие или нечеткие, видимые на всем протяжении или на ограниченном участке.
5) Размеры. Измеряются линейные размеры очага (длинник и поперечник) на аксиальном срезе либо все три размера (когда это возможно, указывается также объем). Если планируется контрольное исследование через определенное время, выбирается т. н. «маркерный» очаг, изменение размеров которого будет оцениваться во времени.
6) Расположение необходимо указывать в описании КТ-исследования: локализуется ли патологический участок непосредственно в глубине органа, под капсулой, рядом с крупными сосудами, с желчными протоками, с желчным пузырем и т. д. Это может быть навести на мысли о его природе: например, билиарные кисты локализованы чаще всего вблизи желчных протоков, вблизи желчного пузыря.
7) Количество. Солитарный очаг в печени означает одиночный. Число патологических участков (например, метастазов при раке желудка или других органов системы пищеварения) может варьировать. Выявление одного метастаза уже позволяет выставить стадию M1 по системе TNM. Однако следует учитывать, что множественные очаговые образования в печени – это не всегда метастазы, и врач-рентгенолог обязан провести их дифференциальную диагностику, сопоставив многочисленные КТ-признаки.
8) Особенности накопления контраста. Чем меньше накопление контраста в очаге, тем меньше он кровоснабжается. Наоборот, чем быстрее накапливается контраст, тем более развита сосудистая сеть. Чем быстрее снижается плотность после окончания введения контраста, тем интенсивнее кровоток в очаге.
Так, гемангиома печени на КТ без контраста выглядит как гиподенсный участок, природу которого установить затруднительно. В артериальную фазу контрастирования наблюдается значительное увеличение плотностных характеристик гемангиомы (из-за накопления контрастированной крови в сосудистых лакунах), но затем ее плотность снижается и постепенно приходит к прежним значениям, что позволяет отличить гемангиому печени от рака, так как злокачественные новообразования, например, рак кишечника с метастазами в печень при КТ с контрастированием проявляется иначе: для метастазов наиболее характерно усиление плотности в виде «кольца» («ободка»), которое отображает активную (васкуляризованную) часть опухоли.
Гемангиома печени или рак? КТ брюшной полости с контрастным усилением: типичное накопление контраста в виде лакун помогает дифференцировать гемангиому от рака и установить правильный диагноз: кавернозная гемангиома.
Гиподенсные образования имеют плотность ниже нормальной паренхимы (в норме ее плотность составляет +50…+70 единиц Хаунсфилда – без контрастирования) и представляют собой следующие морфологические варианты:
1) Жировые образования имеют плотность от -100 до -10 единиц Хаунсфилда. Это может быть липома, фибролипома, ангиолипома, ангиофибролипома, аденома, липосаркома и некоторые другие опухоли из жировой ткани (а также участок с отрицательной плотностью может быть обусловлен локальным участком жировой инфильтрации, или жирового гепатоза).
2) Гиподенсный очаг плотностью 0…+20 единиц Хаунсфилда чаще всего содержит жидкость. Это может быть простая или паразитарная киста, билома – скопление желчи после операций на желчном пузыре и протоках, а также кистозные метастазы.
3) Гиподенсный очаг плотностью +20…+40 единиц Хаунсфилда бывает обусловлен как жидкостным содержимым, так и мягкотканным. Здесь гораздо больше вариантов, при составлении дифференциального ряда нужно учитывать размеры, форму, характер накопления контрастного вещества.
Капиллярная гемангиома правой доли печени: КТ с контрастным усилением в артериальную фазу выявляет гиперденсный участок.
Гиперденсные очаги имеют рентгеновскую плотнтость выше нормальной паренхимы (>70 единиц Хаунсфилда) и могут быть обусловлены кистами, содержащими плотную жидкость (с примесями белка или крови), либо их субстратом является опухоль или кальцинат.
1) Очаг плотностью +200…+400 единиц Хаунсфилда обусловлен наличием кальция в структуре. Это может быть обызвествленная киста, фиброма, фиброаденома (либо другая опухоль), обызвествленная гематома.
2) Локальный участок повышения плотности паренхимы зачастую бывает обусловлен отложениями металлов – солей алюминия, железа и т.д.
3) Опухоли бывают как гиперденсными, так и гиподенсными.
Кистозный характер при КТ имеют следующие образования:
1) Простая киста печени — что это? Простая киста возникает в результате эмбриогенеза и представляет собой ограниченное капуслой скопление жидкости. На КТ она имеют ровные края, четкие контуры, обычно правильную форму; плотностные характеристики жидкости +5…+20 единиц Хаунсфилда, не содержит каких-либо включений (кровь, кальций и т. д.), в их структуре нет перегородок, стенка ровная, без локальных утолщений. Контраст такие кисты не накапливают. Часто возникает вопрос, может ли киста печени перерасти в рак. Если киста имеет типичные КТ-характеристики, тревоги она вызывать не должна, озлокачествления кисты не бывает. Но важно отличить простую кисту от эхинококковой, от кистозной формы метастаза или кистозного рака.
2) Кистозные метастазы в печень при раке молочной железы, желудка, других органов обычно множественные, имеют неправильную форму, неоднородную структуру, размеры от 0,5 см до нескольких десятков см. Характеризуются накоплением контраста в виде «кольца». Обладают инфильтративным ростом. Подозрение на mts в печени возникает при КТ нередко, в таких случаях может помочь второе мнение по снимкам. В наше время множественные метастазы нередко успешно лечатся в крупных онкологических клиниках, где применяются различные методики (хирургическое удаление, химиоэмболизация, радиочастотная абляция и т.п.).
3) Кистозная форма гепатоцеллюлярного рака: форма неправильная, может выявляться солидный компонент (при кистозной форме он выражен минимально), опухоль единичная, оказывает объемное воздействие на рядом расположенные сосуды и желчные протоки.
4) Паразитарные кисты. Чаще всего эти кисты представлены эхинококком, реже – альвеококком. Бывают множественными или единичными, имеют хорошо видимую стенку, усиливающуюся при контрастировании. Бывают однокамерные и многокамерные паразитарные кисты. Внутри таких кист можно обнаружить паразита.
5) Гемангиома правой доли печени, либо левой доли. Гемангиома печени на КТ выглядит как типичный гиподенсный очаг, при контрастировании в артериальную фазу резко усиливается, в результате чего становятся видимыми сосудистые лакуны, а затем медленно теряет контраст. Атипичные гемангиомы на КТ имеют несколько другие характеристики, и отличить их от злокачественного поражения помогает взгляд опытного рентгенолога, имеющего опыт в диагностике заболеваний брюшной полости.
Вторичные (секундарные) изменения в печени на КТ. Рак кишечника с метастазами. Прогноз неблагоприятный, учитывая размеры и количество метастазов.
«Солидный» означает мягкотканный, состоящий из живой ткани. Какие бывают солидные образрования?
1) Объемное образование с включениями жира: липома, липофиброма, ангиолипома, липосаркома и др. Имеют характерную структуру и плотностные характеристики, соответствующие жировой ткани.
2) Фокальная нодулярная гиперплазия (ФНГ) имеет неправильную форму (в виде узла), при нативном исследовании – гиперденсный (незначительно выше нормальной плотности), при контрастировании неравномерно усиливается.
3) Регенераторный узел, локальный участок фиброза либо жировой инфильтрации – признак перерождения печеночной ткани под влиянием различного характера интоксикацией или травм, признак цирроза. Выглядит как локальный гипо- (жировая инфильтрация) или гиперденсный (фиброз) участок.
4) Гепатоцеллюлярный рак (ГЦР). Выглядит как объемное образование неправильной формы, различных размеров (иногда несколько десятков сантиметров в поперечнике), структура его неоднородна – при КТ могут быть выявлены участки некроза, полости (не усиливающиеся при контрастировании). Ткань опухоли за счет хорошего кровоснабжения повышает плотность при контрастировании.
Не все специалисты способны достоверно определить изменения в печени, выявленные при компьютерной томографии. Это во многом зависит от опыта рентгенолога, от качества выполнения исследования. К сожалению, при выполнении компьютерной томографии и других лучевых исследований (особенно в отдаленных периферийных клиниках) изменения иногда бывают пропущены, либо неверно истолкованы. Можно ли перепутать метастазы в печени? Увы, нередко обычные доброкачественные гемангиомы трактуются как метастазы, либо наоборот. В ряде случаев кистозные метастазы в печень трактуются как простые кисты, если к тому же не использовать контрастирование. В целом нужно отметить, что диагноз «mts печени» достаточно сложный в плане дифференцировки с другими множественными очаговыми изменениями.
Второе консультативное мнение врача, обладающего опытом в анализе КТ-исследований брюшной полости, всегда полезно – заключение по исследованию даст специалист, имеющий высшую врачебную категорию или научное звание, после подробного ознакомления с историей заболевания, с результатами лабораторных тестов и т. д. В результате точность диагностики становится выше, что позволяет определиться с дальнейшим направлением лечения (либо назначить дополнительные инструментальные и иные диагностические исследования).
Чтобы получить Второе мнение по результатам КТ или МРТ, можно обратиться в Национальную телерадиологическую сеть. Сделать это можно удаленно, не выходя из дома. Достаточно иметь результаты исследования на диске. В течение 24 часов с момента отправки снимков вы получите квалифицированный пересмотр КТ или МРТ с подробным описанием в виде заключения с подписью высококвалифицированного диагноста.
источник
После внедрения МРТ в клиническую практику ведущих европейских клиник врачи получи множество полезной информации относительно использования магнитно-резонансной томографии для диагностики заболеваний органа. Клинические исследования показали высокую ценность использования МРТ сканирования для верификации кист, гемангиом, рака ворот печени, фиброзных изменений, метастатического поражения печеночных тканей.
МРТ печени хорошо показывает гемангиомы – доброкачественные сосудистые опухоли. Образования имеют четкие контуры, по мере нарастания спиновых эхо-последовательностей во всех взвешенных изображениях прослеживается падение интенсивности сигнала. Во всех случаях на T1-взвшенных изображениях гипоинтенсивность сигнала падает.
Фото МРТ печени при гигантской кисте
Повышенная интенсивность сигнала на T2-взвешенных снимках позволяет провести дифференциальную диагностику гемангиом от кист. Дополнительным диагностическим признаком является однородность структуры. Неоднородные образования с гипо- и гиперинтенсивными включениями встречаются в 28% случаев.
МРТ печени при раке сопровождается высоким полиморфизмом симптомов. На T1-взвешенном снимке злокачественное новообразование характеризуется сигналом низкой интенсивности. Повышение прослеживается при кровотечениях, наличии жировой ткани внутри очага. На T2-взвешенной рентгенограмме прослеживается очаг с неоднородной структурой. На долю образований с мелкими гипоинтенсивными ободками приходится около 7% случаев.
Наличие объемного образования с масс-эффектом, гипоинтенсивный сигнал на T1-режиме встречается в 80% случаев. На долю монофокальных поражений приходится 76% случаев.
На практике установлена специфичность МРТ при диагностике болезней печени со специфичностью в 64%.
Затруднение вызывает дифференциальная диагностика метастазов в печень с полиморфизмом проявлений. Типичные признаки патологии – T1-взвешенное изображение (95%), перифокальный отек (68%), неоднородность структуры (81%).
Средняя чувствительность магнитно-резонансной томографии составляет около 89%. В данный показатель включена вероятность гипердиагностики. После верификации образования биопсией ошибочная диагностика метастазов встречается у 4% пациентов при первичной многоузловой форме рака. В любом случае при использовании магнитно-резонансной томографии нельзя пропустить небольшое образование более 5мм диаметров в печеночных тканях.
Есть практические наблюдения относительно принятия за метастаз крупной кисты (более 15 мм диаметром). Метастазы лейомиосаркомы и рака желудка ошибочно трактуются врачами лучевой диагностики, как гемангиомы. Для дифференциальной диагностики в данном случае достаточно провести T2-релаксометрию.
Информативность диагностики при верификации кист печени достаточно высока. МРТ диагностика показывает высокую чувствительность и специфичность при этих нозологических формах (свыше 90%). Дифференциальная диагностика гемангиом на основе T1 и T2-взвешенных снимков при гидрографии позволяет получить качественную картинку узла с гипоинтенсивным ободком.
Для отличия жировой дистрофии от печеночной аденомы требуется оценка гиперинтенсивного сигнала на t1-взвешенном изображении. Способ подавления сигнала от жира в импульсной последовательности определяется градиентным эхо, представляющим подбор определенных импульсов от воды и жира. Противофаза приводит к уменьшению импульсной последовательности от жировой ткани.
Узловая гиперплазия предполагает использование рутинных способов диагностики, позволяющих провести дифференциальную диагностику между гепатоцеллюлярными образованиями.
Сложности при мрт диагностики печени возникают при необходимости верификации первичного печеночного рака из фиброзной ткани и аденоматозной гиперплазии. Специалисты встречаются с формами злокачественных новообразований, возникающих у пациентов с фиброзом печени. Гипоинтенсивный сигнал от паренхимы, различные очаговые образования печеночных клеток составляют трудности при верификации мелких очагов.
Первичный рак появляется также при циррозе. При таком образовании МРТ печени показывает цирроз, при котором гиперинтенсивный сигнал на T2-режиме является дифференциальным признаком, так как очаги восстановления ткани характеризуются низкоинтенсивной последовательностью.
Анализируя описанную информацию, удается визуализировать изменения интенсивности сигнала паренхимы печени, очаги печеночной ткани, обусловленные разностью изображения между патологической и нормальной тканью. Специфические изменения на снимках, построенных на основе релаксации между T1 и T2 режимами, позволяют более тщательно верифицировать характер патологии. На томограммах врачи лучевой диагностики определяют следующие изменения:
1. Гипо- и гиперинтенсивность в T1-T2-взвешенных режимах;
2. Однородность, неоднородностью структуры образования;
3. Наличие, отсутствие капсулы;
4. Дополнительные включения.
Определенное сочетание описанных признаков позволяет предположить диагноз. На основе первичной томограммы удается определить патологические образования при злокачественных опухолях. Для верификации изменений требуется изучение дополнительных признаков. Есть практические результаты оценки T2 печеночной ткани, которые в норме равны 74 мс, при гемангиомах – 298 мс, при злокачественных опухолях – 181 мс. Время релаксации – это важная характеристика, помогающая верифицировать диагноз.
МРТ печени и желчного пузыря показывает разное время релаксации при злокачественных опухолях и гемангиомах с большими диапазонами перекрытия. Научные исследования выявили погрешности при дифференциальной диагностике на магнитно-резонансных томограммах печени и желчного пузыря при большой выборке пациентов. Искажения t2 определяются следующими особенностями:
• Разная васкуляризация;
• Очаги некроза в ткани;
• Кровоизлияния;
• Включения жира;
• Дополнительные артефакты.
Есть случаи времени релаксации при гемангиомах около 87 мс, а при раке – 95 мс. Такие расхождения специалисты объясняют изменениями печеночной ткани на фоне патологического процесса.
На МРТ желчного пузыря искажение T2 определяется также при поражении путей опухолью, холестазе, обтурационном гепатите (закупорка желчного пузыря и протоков).
Более достоверно провести дифференциальную диагностику позволяет введение коэффициента релаксации, отражающего пропорции между временем релаксации печеночной ткани и аналогичного значения от патологического образования – Т2 образования/T2 паренхимы печени.
При гемангиомах коэффициент имеет значение 2,8-3,4. При злокачественных опухолях значение более низкое – меньше 2,0.
Эхинококковая киста в печения на магнитно-резонансной томограмме
Для МРТ-диагностики образований печени и желчного пузыря важное значение имеет правильный подбор импульсных последовательностей. К примеру, верификация гемангиом при T2-взвешенном сканировании позволяет выявить важный признак – повышение сигнала с увеличением спинового эхо. Для верификации доброкачественных сосудистых образований не рационально использование быстрых методик.
При подозрении на аденому или первичный рак рекомендуется применение T1 и T2 режимов. Подход позволяет определить неоднородность структуры образования. Подавление сигнала от жировой ткани позволяет верифицировать образования с содержанием жира. Информативность исследования не позволяет использовать качественные методы верификации патологи. Комбинирование последовательностей помогает определить неоднородность строения, обнаружить капсулу, кровоизлияния.
Информативность релаксометрии при однородности опухолей структуры позволяет получить нужно заключение.
При подозрении на кисты печени эффективность метода гидрографии не вызывает сомнений. Режим позволяет четко отслеживать жидкость.
Метастазы лучше визуализировать при подавлении артефактов дыхания. Сочетание режима с гидрографией позволяет провести дифференциальную диагностику печеночных кист.
МРТ печени с контрастом позволяет верифицировать васкуляризацию патологических образований. Способ дополняет диагностическую информацию, полученную при гемангиомах, злокачественных новообразованиях. Периферическое очаговое контрастирование направлено от периферии к центральной части. Обследование позволяет изучить гепатоциты в портальную и аортальную фазу.
Динамическая контрастная магнитно-резонансная томография – это современный метод, нивелирующий недостатки традиционного исследования. Обследование показывает следующие результаты:
1. Отсутствие васкуляризации при гемангиомах;
2. Периферический рак печени характеризуется гипо- или гиперваскуляризацией. При васкулярном типе контраст поступает в интерстиций, поэтому хорошо прослеживается капсула. При гиперваскуляризации может прослеживаться отсутствие контраста при некрозе, стартовое контрастирование в артериальную фазу, вымывание;
3. При метастазах динамическое контрастирование позволяет заполнить образование полностью или частично. Эффект вымывания прослеживается примерно у 70% пациентов, стартовое контрастирование в артериальную фазу возникает из-за уникального кровоснабжения метастазов.
Подводя итог, о роли МРТ печени с контрастом для верификации патологических очагов следует заметить специфические признаки диагностики. При гемангиомах полость постепенно или быстро заполняется полностью. Для раков характерно «вымывание». При гиперваскулярных формах опухоли прослеживается попадание контрастного вещества в раннюю фазу внутрь патологического очага.
Динамическая контрастная магнитно-резонансная томография – это обследование, позволяющее отличить узловую гиперплазию от фиброза печени.
При кистах контрастирование очага не возникает. При абсцессе в единичных случаях возникает засвечивание капсулы.
Подведем итог описанной информации:
• Исследования указывают на то, что томография при использовании описанных алгоритмов, применении релаксометрии является качественным диагностическим методом, превосходящим другие способы обследования;
• Специфичность магнитно-резонансной томографии при диагностике печеночных очагов установлена в 82% при выявлении гемангиом, метастазах – 81%, кистах – 90%;
• Использование времени релаксации с коэффициентом соотношения между здоровой тканью и патологическим очагом повышает вероятность дифференцировки заболевания;
• Коэффициент релаксации эффективен при верификации злокачественных опухолей и гемангиом;
• Динамическое МР-контрастирование позволяет использовать быстрые импульсные последовательности для оценки артериальной, интерстициальной и портальной фазы;
• Динамическая магнитно-резонансная томография увеличивает специфичность исследования до 96%. Выделение дополнительных признаков при контрастировании позволяет верифицировать патологические опухоли;
• Пункционная биопсия помогает справиться с метастазами, помогает при узловой гиперплазии печени;
• Комплексная лучевая диагностика пациентов с дополнением магнитно-резонансной томографии КТ и УЗИ повышает качество диагностики.
При подозрении на патологию печени настоятельно рекомендуем использовать коэффициент релаксации, позволяющий предварительно предположить характер инородного узла.
При комплексной диагностике требуется изучение возможностей разных методов диагностики и сопоставление их результатов получению необходимой диагностической информации.
Пришлите данные Вашего исследования и получите квалифицированную помощь от наших специалистов
источник
1 ГБУЗ «Научно-практический центр медицинской радиологии Департамента здравоохранения города Москвы» ФГБНУ «Российский Научный Центр Хирургии им. акад. Б.В. Петровского» Дифференциальная диагностика очаговых образований печени методами КТ и МРТ Москва 2017 Ким Станислав Юрьевич к.м.н. Заместитель директора по научной работе
2 Основная роль методов диагностики очаговых образований печени *Выявление чувствительность *Дифференциальная характеристика специфичность Определение задач лечения наблюдение, биопсия, хирургия Планирование лечения абляция, резекция, регионарная или системная терапия Контроль за результатами лечения прогрессирование, степень ответа на терапию Дополнительно оценка состояния паренхимы, объем неизмененной паренхимы, оценка состояния сосудистого русла, желчных протоков, функции печени.
3 Методы диагностики очаговых образований печени УЗИ МСКТ Сцинтиграфия ПЭТ-КТ МРТ T2-ВИ Т1-ВИ с внеклеточным КВ с внутриклеточным КВ
4 Два источника кровоснабжения печени 70-80% за счет воротной вены 20-30% за счет печеночной артерии! Наилучшее контрастирование печени происходит в портально-венозную фазу исследования!
5 Стандарты качества при КТ брюшной полости Выбор протокола по весовой группе пациента Толщина среза 6 Протокол МСКТ исследования (томографы 64 slice и более) ТРЕБУЕТСЯ КАК МИНИМУМ 2-х ФАЗНЫЙ ПРОТОКОЛ!! Фаза Задержка Анализ Бесконтрастная фаза АРТЕРИАЛЬНАЯ ФАЗА 0-20 с Камни, кальцинаты, оценка плотности печени (гепатоз), определение границ сканирования артерии гиперваскулярные образования Фаза воротной вены с воротная вена гиповаскулярные образования ВЕНОЗНАЯ ФАЗА с воротная вена, собственные вены нижняя полая вена гиповаскулярные образования Wash-out Отсроченная фаза 300 сек Wash-out
7 Протокол МРТ-исследования Стандартный протокол: T2-ВИ T1-ВИ Fat saturation DWI MRCP (по запросу) + CM
8 КВ при МРТ печени неспецифичные (внеклеточные) гепатоцит-специфичные, гепатотропные (внутриклеточные) Gd-EOB
9 МРТ с контрастированием 0 сек сек T1-FS (быстрое динамическое исследование с задержкой дыхания)
10 T2 FS МРТ с гепатотропным КВ T1 FS + Gd-EOB 20 min 1 min 10 min
11 Накопление контраста МРТ с контрастированием Gd-EOB Высокодиф. ГЦК и гиперваскулярные метастазы Фокальнонодулярная гиперплазия Гепатоцелюллярная аденома Гемангиома Низкодиф. ГЦК Гиповаскулярные метастазы Нормальная паренхима печени время By Agris and Menist
12 Применение последовательности диффузионновзвешенных изображений (DWI) Диффузионно-взвешенная МРТ регистрирует диффузию молекул воды в биологических тканях Злокачественные образования имеют более высокую плотность опухолевых клеток и малый объём межклеточной жидкости по сравнению с доброкачественными образованиями, что снижает скорость диффузии молекул воды
13 Применение DWI T2 T2 FS+ контраст B500
14 DWI Timm Denecke, Klinik für Radiologie Charité — Universitätsmedizin Berlin, 2011
15 Область обсуждения Метастазы колоректального рака печени Киста Цистаденома Эхинококкоз Альвеококкоз Гемангиома ФНГ Аденома ГЦК Холангиокарцинома Абсцесс Очаги фокального стеатоза
16 Алгоритм диагностического поиска: плотность Плотность образования ЖИДКОСТНАЯ Киста Простая Паразитарная Цистаденома Абсцесс МЯГКОТКАННАЯ Вторичное поражение Холангиоцеллюлярный рак Альвеококкоз ГЦА ГЦК НИЗКАЯ ПЛОТНОСТЬ Гемангиома ФНГ 16
17 Алгоритм диагностического поиска: васкуляризация НАКОПЛЕНИЕ КОНТРАСТА АВАСКУЛЯРНЫЕ, СЛАБОВАСКУЛЯРНЫЕ Киста Простая Паразитарная Цистаденома Абсцесс Вторичное поражение Холангиоцеллюлярный рак Альвеококкоз ГИПЕРВАСКУЛЯРНЫЕ Гемангиома Фокальнонодулярная гиперплазия Гепатоцелелюллярная аденома Гепатоцелюллярная карцинома 17
18 Метастазы КРР на КТ гиповаскулярные образования Гиподенсные очаги, которые отчётливо определяются в портально-венозной фазе Периферический «ободок» в портально-венозной фазе контрастирования
19 Фазы распределения контрастного вещества в печени и метастатическом узле Timm Denecke, Klinik für Radiologie Charité — Universitätsmedizin Berlin, 2011
20 Метастазы КРР (МРТ) на Т1-ВИ гипоинтенсивные на Т2-ВИ гиперинтенсивные На Т2-ВИ FS гиперинтенсивные МРТ с в/в контрастированием. Кольцевидное накопление КВ по контуру образования с наличием п е р и о п у х о л е в о г о о т е к а.
21 Киста Билиарные кисты печени имеют различные размеры, тонкие стенки, однородное содержимое с плотностью, характерной для жидкости При КТ — денситометрическая плотность При МРТ — гипоинтенсивная на Т1 и однородно гиперинтенсивная на Т2 взвешенных Контрастирование в диагностике кист печени чаще всего проводить нет необходимости (при МРТ) КТ: простая киста МРТ: мелкие кисты левой доли печени
22 Билиарная цистаденома Это многокамерное кистозное образование На КТ и МРТ определяются стенки образования и внутренние септы (перегородки), отличающие цистаденому от простой кисты Могут присутствовать и внутрикистозные мягкотканые включения При КУ накопление (незначительное) стенками и перегородками
23 Эхинококкоз печени кистозное образование с дочерними кистами с многослойной капсулой с различной степенью кальцинации при КУ накопление контраста септами
24 Артериальная фаза Альвеококкоз Наличие обызвествленных включений Венозная фаза Нативная фаза Множественные кисты Нечеткие контуры из-за инфильтративного роста с воспалительной инфильтрацией и некрозом по периферии кист При КУ неравномерно накапливает КВ по периферии
25 Гемангиома на КТ На КТ чётко отграниченное изоденсное или гиподенсное к сосудам образование При КУ- начинающее с периферии контрастирование «языки пламени» или быть узловым «лакуны» В отсроченную фазу большинство гемангиом полностью заполняются КВ
26 MTS Мелкие гемангиомы Нативная артериальная Фаза воротной вены Поздняя (2 мин) Мелкие гемангиомы могут быстро гомогенно накапливать КВ в виде «вспышек», большие гемангиомы могут выглядеть атипично, так как полному заполнению иногда препятствует центральный фиброзный рубец.
27 Гемангиома на МРТ Т2 ВИ на T1 гипоинтенсивная на T2 гиперинтенсивная На Т2FS характерно очень яркое изображение опухоли на фоне темной паренхимы печени. При КУ аналогично накоплению контраста на КТ Т1 с контрастированием
28 ФНГ(КТ) ФНГ это сосудистая опухоль Гиперваскулярная в артериальную фазу, за исключением зоны центрального рубца (симптом «колеса со спицами»). При КУ с визуализаций в артериальную фазу приносящего артериального сосуда Симптом «колеса со спицами» в артериальную фазу
29 ФНГ (МРТ) На Т1 ВИ гиперинтенсивная (слабо-гиперинтенсивная) На Т2 ВИ рубец типично гиперинтенсивен в 80% случаев. Контрастное усиление гадолиний-содержащими препаратами дает схожие результаты о характере васкуляризации образования в сравнении с постконтрастными КТ изображениями. Диагноз ФНГ ставится на основании наличия центрального рубца и гомогенного контрастирования, однако типичный центральный рубец может не визуализироваться в 20% наблюдений.
30 Аденома (КТ и МРТ) Отграниченная инкапсулированная опухоль Аденомы склонны к центральному некрозу и кровоизлияниям Большинство аденом на КТ представлены гомогенно контрастирующимися в артериальную фазу очагами. Наличие жира в аденомах обнаружено у около 7% пациентов на КТ и лучше визуализируется на МР-изображениях. Псевдокапсула низкой плотности, контрастируемая в отсроченные фазы, встречается в 30% случаев.
31 ГЦК Мозаичная структура (участки кровоизлияний и фиброза) Наличие внутриопухолевых перегородок, некротических или кистозных участков Наличие капсулы и дочерних узлов. Гиперваскулярный характер опухоли, что характеризуется её особенностью кровоснабжения и наличием артерио-венозных шунтов. Анализ всех данных исследования может подтвердить признак «вымывания» в венозную фазу контрастирования, а так же наличие хорошо видимой псевдокапсулы опухоли.
32 ГЦК (МРТ) T1 Art phase 1min 5min Т1- гипоинтенсивный сигнал (иногда может быть с гиперинтенсивным окружением за счет отека прилежащей ткани) Т2- гиперинтенсивный сигнал Т2FS- гиперинтенсивный сигнал ДВИ- гиперинтенсивный сигнал на В1000
33 Холангиокарцинома Гиподенсная в артериальную и портально-венозную фазу, с некоторым периферическим усилением Гиперденсная в отсроченную фазу, что говорит о плотной фиброзной ткани Гиповаскулярна, отмечается отсроченное стойкое накопление КВ Ретракция капсулы печени Выраженное расширение внутрипеченочных желчных протоков выше места их обструкции опухолью и контрастирование ткани самого образования.
34 Абсцесс Жидкостной плотности образование с четкими контурами, толстой капсулой, которая накапливает контрастное вещество к отсроченной фазе сканирования (фиброз) Перфузия смежной паренхимы снижена ( двойная мишень ) Клинико-лабораторная картина* LiverAtlas. 34
35 Очаг стеатоза Очаги фокальной формы стеатоза могут имитировать метастазы, однако на нативных изображениях эти участки жировых изменений имеют неправильную географическую форму без массэффекта и изменения локальных сосудов.
36 Чувствительность МРТ с гепатотропным КВ в сравнении с МСКТ Динамическая МСКТ Фаза воротной вены МРТ Т1 ВИ (Т1WI FS VIBE) через 15 мин после введения
37 Алгоритм описания 1. Локализация по сегментам печени 2. Размеры образования a.передне-задний b.медио-латеральный c.кранио-каудальный 3. Края и контуры 4. Плотность и структура 5. Характер накопления контрастного препарата 6. Статус смежных анатомических структур 37
38 Шаблон описания БРЮШНАЯ ПОЛОСТЬ ИССЛЕДОВАНИЕ: Первичное / Повторное, сравнение с исследованием от г. ПЕЧЕНЬ: не увеличена, однородной структуры. Внутри- и внепеченочные протоки не расширены. ЖЕЛЧНЫЙ ПУЗЫРЬ: не изменен, рентгеноконтрастных конкрементов не выявлено. ПОДЖЕЛУДОЧНАЯ ЖЕЛЕЗА: не увеличена, структура не изменена, Вирсунгов проток не расширен. СЕЛЕЗЕНКА: не увеличена, структура не изменена. НАДПОЧЕЧНИКИ: не увеличены, структурно не изменены. ПОЧКИ И МОЧЕВЫВОДЯЩАЯ СИСТЕМА: почки обычно расположены, не увеличены, структура и плотность паренхимы не изменены. Чашечно-лоханочные системы не расширены. Мочеточники не расширены. Конкрементов по ходу мочевыводящих путей не выявлено. ОРГАНЫ МАЛОГО ТАЗА: без патологических изменений. СОСУДЫ: без особенностей. ЛИМФАТИЧЕСКИЕ УЗЛЫ: не увеличены. ПРОЧИЕ ОРГАНЫ: свободной жидкости в брюшной полости нет. В мягких тканях патологические изменения не выявлены. КОСТНЫЕ СТРУКТУРЫ: без патологических изменений. ЗАКЛЮЧЕНИЕ: Патологических изменений органов брюшной полости не выявлено. 38
39 Шаблон описания МР-ХОЛАНГИОГРАФИЯ ИССЛЕДОВАНИЕ: Первичное / Повторное, сравнение с исследованием от г. ПРАВЫЙ ПЕЧЁНОЧНЫЙ ПРОТОК — до х мм в диаметре, ЛЕВЫЙ ПЕЧЁНОЧНЫЙ ПРОТОК — до х мм в диаметре. Протоки формируют ОБЩИЙ ПЕЧЁНОЧНЫЙ ПРОТОК обычно. ХОЛЕДОХ до х мм. Визуализируется (не визуализируется) ПУЗЫРНЫЙ ПРОТОК до х мм в диаметре. Просвет всех протоков однородный, дефектов наполнения не выявлено. ХОЛЕДОХ и ВИРСУНГОВ ПРОТОК визуализируются до места впадения в 12- ти перстную кишку, просвет их однороден, препятствий оттоку не выявлено. Вирсунгов проток визуализируется на всём протяжении, до х мм в диаметре. 39
40 ГБУЗ «Научно-практический центр медицинской радиологии Департамента здравоохранения города Москвы» ФГБНУ «Российский Научный Центр Хирургии им. акад. Б.В. Петровского» Спасибо за внимание! Москва 2017 Ким Станислав Юрьевич
источник
Среди других паренхиматозных органов человеческого организма печень занимает главенствующую роль, выполняя множество жизненно необходимых функций. Современный образ жизни человека, а также состояние окружающей среды способствуют огромным нагрузкам, возлагаемым на данный орган. Это зачастую приводит к возникновению различных заболеваний и патологических процессов в печени.
С целью диагностирования заболеваний печени в настоящий момент существует большое количество разнообразных лабораторных и инструментальных методов исследования. Одним из наиболее современных, высокоточных и абсолютно безвредных среди них является метод МРТ диагностики, обладающий большим числом преимуществ.
Патологические изменения печени условно разделяют на диффузные и очаговые.
Рассмотрим несколько примеров выявления заболеваний обеих групп методом МРТ:
Жировая дистрофия печени — патологический процесс, связанный с накоплением липидов в клетках печени. Встречается и как самостоятельное заболевание, и как синдром, сопровождающий ряд заболеваний (гепатит, алкоголизм, интоксикация, ятрогенный генез).
Клинически жировая дистрофия может протекать бессимптомно или в стертой малопрогрессирующей форме. Со временем могут появляться тупые боли в правом подреберье, диспептические расстройства, нарушение стула, слабость, утомляемость.
Т1-ВИ, диффузное повышение интенсивности МР-сигнала.
Очаговая жировая дистрофия печени, Т1-ВИ. При применении программы FS, неоднородное очаговое снижение интенсивности МР-сигнала в правой доле печени за счет жироподавления.
Цирроз печени – заболевание, являющееся в большинстве случаев следствием алкоголизма, гепатита В, билиарного цирроза, гемохроматоза и некоторых др.
Подобные процессы способствуют гибели и значительному уменьшению количества гепатоцитов с замещением их соединительной тканью (фиброзом), что приводит к уменьшению размеров печени, развитию печеночной недостаточности, спленомегалии и портальной гипертензии.
Пациентов беспокоят слабость, нарушение аппетита, снижение работоспособности, диспептические расстройства, чувство тяжести в правом подреберье, различные нарушения сознания и поведения.
Выявляются также «печеночные знаки» — сосудистые «звездочки» и покраснение ладоней.
Цирротическая трансформация печени.
Гемохроматоз – представляет собой патологию печени, связанную с избыточным накоплением железа в клетках ретикулоэндотелиальной системы. Данное заболевание может быть первичным (наследственным) или вторичным – при повышенном поступлении железа в организм (посттрансфузионный, алиментарный и др.).
Большинство выявляемых мелких очагов в печени у пациентов являются доброкачественными (кисты, гемангиомы и прочие).
Образования небольших размеров (менее 1.5 см) при многих методах исследования зачастую не дают возможности достоверно высказаться об их характере. В таких случаях требуется обследование с использованием наиболее высокоточных методов, таких как МРТ.
В случаях, когда при ультразвуковом исследовании не удается получить все требуемые характеристики кисты или исследование является недостаточно информативным, может быть рекомендовано МРТ исследование.
1. простые — характеризуются тонкими стенками, без перегородок, с однородным жидкостным содержимым.
Единичная простая киста печени
Множественные эхинококковые кисты печени и единичная киста в селезенке
Возникает в результате инфекционных процессов, развивающихся после травм печени, операций, при флебите портальной вены, сепсисе.
Проявляется выраженной гипертермией, тахикардией, диспептическими расстройствами, а также болями и чувством распирания типичной локализации.
Достаточно часто встречающаяся при МРТ обследовании печени доброкачественная опухоль. В подавляющем числе случаев гемангиомы бессимптомны и обнаруживаются случайно. Очень редко гигантские (> 5 см) гемангиомы сопровождаются клинической симптоматикой из-за сдавления окружающих структур, тромбоза сосудов или кровотечений.
Наличие гемангиомы печени при МРТ не вызывает никаких сомнений даже при размерах гемангиомы менее 1,0 см по причине высокой интенсивности сигнала по Т2 ВИ и характерных волнистых четких контуров.
Нативные и постконтрастные МР-изображения гемангиомы с диффузным типом усиления.
Очаговая гиперплазия печени (ОГП)
Вторая по частоте доброкачественная опухоль печени. Включает в себя гепатоциты, купферовские клетки и желчные протоки. В центральной части располагается рубец, от которого отходят перегородки – септы. Встречается чаще у взрослых женщин. Протекает бессимптомно и обнаруживается зачастую случайно. Не малигнизируется и обычно не создает проблем для здоровья (чрезвычайно редко кровоточит).
МРТ визуализация ОГП при нативном исследовании и динамическом контрастировании. МРТ-исследование с динамическим контрастированием достоверно выявляет и позволяет однозначно характеризовать образование печени как узловую нодулярную гиперплазию.
Узловая гиперплазия печени
Доброкачественная опухоль печени, происходящая из гепатоцитов.
Гетерогенна по структуре (некроз, кровоизлияния, жировая инфильтрация, инкапсуляция, развитие крупных внутриопухолевых сосудов).
Встречаются как одиночные, так и множественные аденомы.
Диагностика данной опухоли очень важна в силу высокого риска осложнений в виде кровотечения, разрыва, малигнизации. Методом выбора в случае подозрения на аденому является МРТ печени с в/венным динамическим усилением.
МРТ визуализация гепатоцеллюлярной аденомы печени
Первичная опухоль печени, наиболее часто встречающаяся среди злокачественных новообразований данного паренхиматозного органа.
Риск развития гепатоцеллюлярного рака высок у лиц с циррозом печени, гепатитом В и гемохроматозом.
Различают узловую, многоузловую и диффузную формы.
Характерна инвазия в портальную и печеночную вены.
Клинически проявляется тупой болью в правом подреберье, лихорадкой, общей слабостью и на поздних стадиях — желтухой.
Гепатоцеллюлярный рак (по данным УЗИ – гемангиома).
Гепатоцеллюлярный рак (инфильтративная форма), вторичная лимфоаденопатия.
Холангиоцеллюлярный рак (холангиокарцинома).
Представляет собой злокачественную опухоль, исходящую из внутрипеченочных желчных протоков. Встречается достаточно редко. В клинической картине преобладающим симптомом является желтуха.
По причине особенностей кровообращения человеческого организма, наличия системы воротной вены, метастазирование различных опухолей в печень весьма закономерно. Наиболее часто в печень метастазируют опухоли желудка, кишечника, поджелудочной железы, рак легкого и молочной железы.
Множественные метастазы печени.
Единичные мелкие метастазы печени; схожесть при нативном исследовании с гемангиомами.
Тот же пациент. Постконтрастные томограммы. Единичные мелкие метастазы печени в отличие от гемангиом на томограммах в ранней и поздней паренхиматозных фазах становятся гипоинтенсивными, как при нативном исследовании (критерий быстрого сброса контраста в течение 1 минуты).
источник
НЕКОТОРЫЕ АСПЕКТЫ ДИАГНОСТИКИ ОЧАГОВОЙ ПАТОЛОГИИ ПЕЧЕНИ
SOME DIAGNOSTIC ASPECTS OF FOCAL LIVER PATHOLOGY
С. В. Шахиджанова, Т. С. Пустовитова
Shakhidzhanova S. V., Pustovitova Т. S.
Институт клинической кардиологии им. А. Л.Мясникова Российского кардиологического научно-производственного комплекса, Москва
A. L. Myasnikov Institute of Clinical Cardiology, Cardiology Research Complex, RF Ministry of Public Health, Moscow
В статье представлены данные о применении различных визуализирующих методик в диагностике очаговых поражений печени: гемангиом, кист, абсцессов, аденом, очаговой узловой гиперплазии, злокачественных опухолей. Рассматривается также вопрос о сложности выявления злокачественных поражений на фоне цирротически измененной печени. Проведен анализ данных литературы для определения предпочтительных методик в диагностике различных очаговых образований печени, что позволит сократить путь к установлению диагноза.
This paper reviews the data on the use of different visualization techniques in the diagnosis of focal liver pathology such as hemangiomas, cysts, abscesses, adenomas, focal nodular hyperplasia and malignant tumors. The problem of the difficulties which may be encountered in the diagnosis of malignancies in the presence of cirrhotic lesions of the liver is also under consideration. Analysis is made of the reported data in order to delineate the preferable modalities to be employed in the diagnosis of different focal liver pathology, which will allow for shortening the way to the diagnosis establishment.
(«Визуализация в клинике», 2001, 19: 31-41)
| Ключевые слова: печень, очаговая патология, ультразвуковое исследование, магнитно-резонансная томография, компьютерная томография. |