Глюкоза является главным энергетическим материалом для функционирования человеческого тела. В организм она поступает с пищей в виде углеводов. На протяжении многих тысячелетий человек претерпевал массу эволюционных изменений.
Одним из важных приобретенных умений стала способность организма впрок запасать энергетические материалы на случай голода и синтезировать их из других соединений.
Избытки углеводов аккумулируются в организме при участии печени и сложных биохимических реакций. Все процессы накопления, синтеза и использования глюкозы регулируются гормонами.
Существуют следующие пути для использования глюкозы печенью:
- Гликолиз. Сложный многоступенчатый механизм окисления глюкозы без участия кислорода, в результате которого образуется универсальные источники энергии: АТФ и НАДФ — соединения, обеспечивающие энергией протекание всех биохимических и обменных процессов в организме;
- Запасание в виде гликогена при участии гормона инсулина. Гликоген – неактивная форма глюкозы, которая может накапливаться и сберегаться в организме;
- Липогенез. Если глюкозы поступает больше, чем необходимо даже для образования гликогена, начинается синтез липидов.
Роль печени в углеводном обмене огромна, благодаря ей в организме постоянно присутствует запас углеводов, жизненно необходимых организму.
Основная роль печени — регуляция углеводного обмена и глюкозы с последующим депонированием гликогена в гепатоцитах человека. Особенностью является превращение сахара под воздействием узкоспециальных ферментов и гормонов в особую его форму, этот процесс происходит исключительно в печени (необходимое условие потребления её клетками). Эти преобразования ускоряются ферментами гексо- и глюкокиназой при понижении уровня содержания сахара.
В процессе пищеварения (а углеводы начинают расщепляться сразу после попадания еды в ротовую полость) содержание глюкозы в крови повышается, вследствие чего происходит ускорение реакций, направленных на депонирование излишков. Тем самым предупреждается возникновение гипергликемии во время приёма пищи.
Сахар из крови с помощью ряда биохимических реакций в печени преобразуется в неактивное его соединение – гликоген и накапливается в гепатоцитах и мышцах. При наступлении энергетического голода с помощью гормонов организм способен высвобождать гликоген из депо и синтезировать из него глюкозу — это основной путь получения энергии.
Излишки глюкозы в печени используются в производстве гликогена под воздействием гормона поджелудочной железы — инсулина. Гликоген (животный крахмал) — это полисахарид, особенностью строения которого является древообразная структура. Запасают его гепатоциты в форме гранул. Содержание гликогена в печени человека может увеличиваться до 8% от массы клетки после принятия углеводистой еды. Распад нужен, как правило, для удержания уровня глюкозы в процессе пищеварения. При длительном голодании содержание гликогена понижается почти до нуля и снова синтезируется во время пищеварения.
Если у организма повышается потребность в глюкозе — гликоген начинает распадаться. Механизм преобразования происходит, как правило, между приемами пищи, и ускоряется при мышечных нагрузках. Голодание (отсутствие приема пищи в течение не менее 24 часов) приводит к практически полному распаду гликогена в печени. Но при регулярном питании его запасы полностью восстанавливаются. Подобное аккумулирование сахара может существовать очень долго, до возникновения потребности в распаде.
Глюконеогенез – процесс синтеза глюкозы из неуглеводных соединений. Его главная задача — удержание стабильного содержания углеводов в крови при недостатке гликогена или тяжёлой физической работе. Глюконеогенез обеспечивает продукцию сахара до 100 грамм в сутки. В состоянии углеводного голода организм способен синтезировать энергию с альтернативных соединений.
Для использования пути гликогенолиза при необходимости получения энергии нужны следующие вещества:
- Лактат (молочная кислота) – синтезируется при распаде глюкозы. После физических нагрузок возвращается в печень, где снова преобразуется в углеводы. Благодаря этому молочная кислота постоянно участвует в образовании глюкозы;
- Глицерин – результат распада липидов;
- Аминокислоты – синтезируются при распаде мышечных белков и начинают участвовать в образовании глюкозы при истощении запасов гликогена.
Основное количество глюкозы производится в печени (более 70 грамм в сутки). Главной задачей глюконеогенеза является снабжение сахаром мозга.
В организм попадают углеводы не только в виде глюкозы — это может быть и манноза, содержащаяся в цитрусовых. Манноза в результате каскада биохимических процессов преобразуется в соединение, подобное глюкозе. В этом состоянии она вступает в реакции гликолиза.
Путь синтеза и распада гликогена регулируется такими гормонами:
- Инсулин – гормон поджелудочной железы белковой природы. Он понижает содержание сахара в крови. В целом особенностью гормона инсулина является влияние на обмен гликогена, в противоположность глюкагону. Инсулин регулирует дальнейший путь преобразования глюкозы. Под его влиянием происходит транспортировка углеводов в клетки организма, а из их избытков — образование гликогена;
- Глюкагон – гормон голода – вырабатывается поджелудочной железой. Имеет белковую природу. В противоположность инсулину, ускоряет распад гликогена, и способствует стабилизации уровня глюкозы в крови;
- Адреналин – гормон стресса и страха. Его выработка и выделение происходят в надпочечниках. Стимулирует выброс избытка сахара из печени в кровь, для снабжения тканей «питанием» в стрессовой ситуации. Так же, как и глюкагон, в отличие от инсулина, ускоряет катаболизм гликогена в печени.
Перепад количества углеводов в крови активирует производство гормонов инсулина и глюкагона, смену их концентрации, что переключает распад и образование гликогена в печени.
Одной из важных задач печени является регулирование пути синтеза липидов. Липидный обмен в печени включает производство разных жиров (холестерина, триацилглицеридов, фосфолипидов, и др.). Эти липиды поступают в кровь, их присутствие обеспечивает энергией ткани организма.
Печень непосредственно участвует в поддержании энергетического баланса в организме. Ее заболевания способны привести к нарушению важных биохимических процессов, в результате чего будут страдать все органы и системы. Необходимо тщательно следить за своим здоровьем и при необходимости не откладывать визит к врачу.
источник

Кость Широкая решила рассказать вам все самое важное и нужное о гликогене, чтобы больше не верили в миф о том, что «сжигание жиров начинается только после 20 минуты бега». Заинтриговали?
Итак, из этой статьи вы узнаете: что такое гликоген, строение и биологическую роль, его свойства, а также формулу и структуру строения, где и для чего содержится гликоген, как происходит синтез и распад вещества, как происходит обмен, а также, какие продукты являются источником гликогена.
Нашему телу еда в первую очередь нужна как источник энергии, а уже потом, как источник удовольствия, антистрессовый щит или возможность «побаловать» себя. Как известно, энергию мы получаем из макронутриентов: жиров, белков и углеводов.
Жиры дают 9 ккал, а белки и углеводы — 4 ккал. Но не смотря на большую энергетическую ценность жиров и важную роль незаменимых аминокислот из белков важнейшими «поставщиками» энергии в наш организм являются углеводы.
Почему? Ответ прост: жиры и белки являются «медленной» формой энергии, т.к. на их ферментацию требуется определенное время, а углеводы — относительно «быстрой». Все углеводы (будь то конфета или хлеб с отрубями) в конце концов расщепляются до глюкозы, которая необходима для питания всех клеток организма.

Гликоген — это своеобразный «консервант» углеводов, другими словами, энергетические резервы организма — сохраненная про запас для последующих энергетических нужд глюкоза. Она хранится в связанном с водой состоянии. Т.е. гликоген — это «сироп» калорийностью 1-1.3 ккал/гр (при калорийности углеводов 4 ккал/г).
По сути, молекула гликогена состоит из остатков глюкозы, это запасное вещество на случай нехватки энергии в организме!
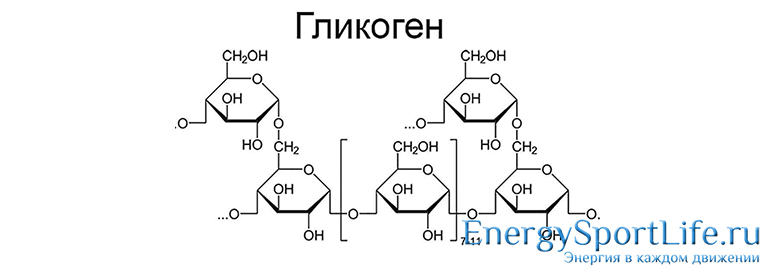
Структурная формула строения фрагмента макромолекулы гликогена (C6H10O5) выглядит схематично так:
Вообще, гликоген — это полисахарид, а значит, относится к классу «сложных» углеводов:
В гликоген может пойти только углевод. Поэтому крайне важно держать в своем рационе планку углеводов не ниже 50 % от общей калорийности. Употребляя нормальный уровень углеводов (около 60% от суточного рациона) вы по максимуму сохраняете собственный гликоген и заставляете организм очень хорошо окислять углеводы.
Важно иметь в рационе хлебобулочные изделия, каши, злаки, разные фрукты и овощи.
Лучшими источниками гликогена являются: сахар, мед, шоколад, мармелад, варенье, финики, изюм, инжир, бананы, арбуз, хурма, сладкая выпечка.
Осторожно к подобной пище стоит отнестись лицам с дисфункцией печени и недостатком ферментов.
Как же происходит создание и процесс распад гликогена?
Как организм запасает гликоген? Процесс образования гликогена (гликогенез) проходит по 2 сценариям. Первый — это процесс запаса гликогена. После углеводосодержащей еды уровень глюкозы в крови повышается. В ответ инсулин попадает в кровоток, чтобы впоследствии облегчить доставку глюкозы в клетки и помочь синтезу гликогена.
Благодаря ферменту (амилазе) происходит расщепление углеводов (крахмала, фруктозы, мальтозы, сахарозы) на более мелкие молекулы.
Затем под воздействием ферментов тонкого кишечника осуществляется распад глюкозы на моносахариды. Значительная часть моносахаридов (самая простая форма сахара) поступает в печень и мышцы, где гликоген откладывается в «резерв». Всего синтезируется 300-400 гр гликогена.
Т.е. само превращение глюкозы в гликоген (запасной углевод) происходит в печени, т.к. мембраны клеток печени в отличие от мембраны клеток жировой ткани и мышечных волокон свободно проницаемы для глюкозы и в отсутствие инсулина.
Второй механизм под названием мобилизация (или распад) запускается в периоды голода или активной физической деятельности. По мере необходимости гликоген мобилизуется из депо и превращается в глюкозу, которая поступает к тканям и используется ими в процессе жизнедеятельности.
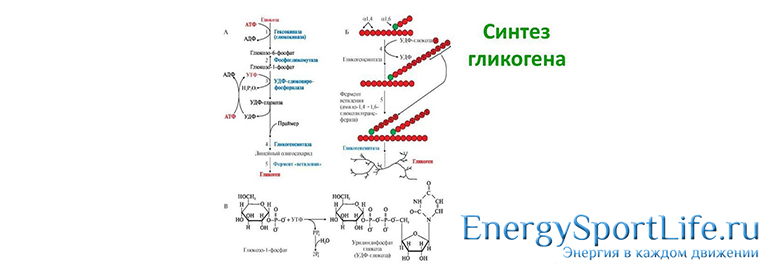
Когда организм истощает запас гликогена в клетках, то мозг подает сигналы о необходимости «дозаправки». Схема синтеза и мобилизации гликогена:
Кстати, при распаде гликогена происходит торможение его синтеза, и наоборот: при активном образовании гликогена его мобилизация тормозится. Гормоны, отвечающие за мобилизацию данного вещества, т.е., гормоны, стимулирующие распад гликогена — это адреналин и глюкагон.
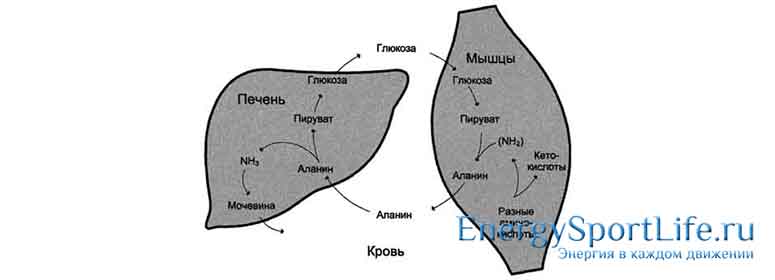
Где накапливается гликоген для последующего использования:
Основные запасы гликогена находятся в печени и мышцах. Количество гликогена в печени может достигать у взрослого человека 150 — 200 гр. Клетки печени являются лидерами по накоплению гликогена: они могут на 8 % состоять из этого вещества.
Основная функция гликогена печени — поддержать уровень сахара в крови на постоянном, здоровом уровне.
Печень сама себе является одним из важнейших органов организма (если вообще стоит проводить «хит парад» среди органов, которые нам все необходимы), а хранение и использование гликогена делает ее функции еще ответственнее: качественное функционирование головного мозга возможно только благодаря нормальному уровню сахара в организме.
Если же уровень сахара в крови снижается, то возникает дефицит энергии, из-за которого в организме начинается сбой. Нехватка питания для мозга сказывается на центральной нервной системе, которая истощается. Тут то и происходит расщепление гликогена. Потом глюкоза поступает в кровь, благодаря чему организм получает необходимое количество энергии.
Запомним также, что в печени происходит не только синтез гликогена из глюкозы, но и обратный процесс — гидролиз гликогена до глюкозы. Этот процесс вызывается понижением концентрации сахара в крови в результате усвоения глюкозы различными тканями и органами.
Гликоген откладывается также в мышцах. Общее количество гликогена в организме составляет 300 — 400 граммов. Как мы знаем, около 100-120 граммов вещества накапливается в клетках печени, а вот остальная часть (200-280 гр) сохраняется в мышцах и составляет максимум 1 — 2% от общей массы этих тканей.
Хотя если говорить максимально точно, то следует отметить, что гликоген хранится не в мышечных волокнах, а в саркоплазме — питательной жидкости, окружающей мышцы.
Количество гликогена в мышцах увеличивается в случае обильного питания и уменьшается во время голодания, а снижается только во время физической нагрузки – длительной и/или напряженной.
При работе мышц под влиянием специального фермента фосфорилазы, которая активируется в начале мышечного сокращения, происходит усиленное распад гликогена в мышцах, который используется для обеспечения глюкозой работы самих мышц (мышечных сокращений). Таким образом, мышцы используют гликоген только для собственных нужд.
Интенсивная мышечная деятельность замедляет всасывание углеводов, а легкая и непродолжительная работа усиливает всасывание глюкозы.
Гликоген печени и мышц используется для разных нужд, однако говорить о том, что какой-то из них важнее — абсолютнейший вздор и демонстрирует только вашу дикую неграмотность.

Все, что написано на данном скрине, полная ересь. Если вы боитесь фруктов и думаете, что они прямиком запасаются в жир, то никому не говорите этой чуши и срочно читайте статью Фруктоза: можно ли есть фрукты и худеть?
Важно знать, почему работают низкоуглеводные высокобелковые диеты. В организме взрослого может находиться около 400 граммов гликогена, а как мы помним, на каждый грамм резервной глюкозы приходится примерно 4 грамма воды.
Т.е. около 2 кг вашего веса — это масса гликогенного водного раствора. Кстати, поэтому мы активно потеем в процессе тренировок — организм расщепляет гликоген и при этом теряет в 4 раза больше жидкости.
Этим свойством гликогена объясняется и быстрый результат экспресс-диет для похудения. Безуглеводные диеты провоцируют интенсивное израсходование гликогена, а с ним – жидкости из организма. Но как только человек возвращается к обычному рациону с содержанием углеводов, запасы животного крахмала восстанавливаются, а с ними и потерянная за период диеты жидкость. В этом и кроется причина недолгосрочности результата экспресс-похудения.
Для любых активных физических нагрузок (силовые упражнения в тренажерном зале, бокс, бег, аэробика, плавание и все, что заставляет вас потеть и напрягаться) организму нужно 100-150 граммов гликогена в каждый час активности. Потратив запасы гликогена, тело начинает разрушать сперва мышцы, затем жировую ткань.
Обратите внимание: если речь идет не о длительном полном голодании, запасы гликогена не истощаются полностью, потому что имеют жизненно важное значение. Без запасов в печени мозг может остаться без снабжения глюкозой, а это смертельно опасно, ведь мозг самый главный орган (а не попа, как некоторые думают).
Без запасов в мышцах сложно совершить интенсивную физическую работу, что в природе воспринимается как повышенный шанс быть съеденным/без потомства/замерзшим и т.д.
Тренировки истощают запасы гликогена, но не по схеме «первые 20 минут работаем на гликогене, потом переходим на жиры и худеем».
Для примера возьмем исследование, в котором тренированные атлеты выполняли 20 сетов упражнений на ноги (4 упражнения, 5 сетов каждого; каждый сет выполнялся до отказа и составлял 6-12 повторений; отдых был коротким; общее время тренировки составило 30 минут).
Кто знаком с силовыми тренировками, понимает, что было отнюдь не легко. До и после упражнения у них брали биопсию и смотрели содержание гликогена. Оказалось, что количество гликогена снизилось с 160 до 118 ммоль/кг, т. е. менее, чем на 30%.
Вот так походя мы развеяли еще один миф — вряд ли за тренировку вы успеете исчерпать все запасы гликогена, так что не стоит набрасываться на еду прямо в раздевалке среди потных кроссовок и посторонних тел, вы явно не помрете от «неминуемого» катаболизма.
Кстати, пополнять запасы гликогена стоит не в течении 30 минут после тренировки ( увы, белково-углеводное окно – миф ), а в течении 24 часов.
Люди крайне преувеличивают скорость истощения гликогена (как и многие другие вещи)! Любят сразу на тренировке закинуться «углями» после первого разминочного подхода с грифом пустым, а то ж «истощение мышечного гликогена и КАТАБОЛИЗМ». Прилег на час днем и усе, печеночного гликогена как не бывало.
Мы уж молчим про катастрофические энергозатраты от 20минутного черепашьего бега. Да и вообще, мышцы жрут чуть не 40 ккал на 1 кг, белок гниет, образует слизь в жкт и провоцирует рак, молочка заливает так, что аж 5 лишних кило на весах (не жира, ага), жиры вызывают ожирение, углеводы смертельно опасны (боюсь-боюсь) и от глютена вы точно помрете.
Странно только, что мы вообще ухитрились выжить в доисторические времена и не вымерли, хотя питались явно не амброзией и спортпитом.
Помните, пожалуйста, что природа умнее нас и давно все при помощи эволюции отрегулировала. Человек один из самых адаптированных и приспосабливаемых организмов, который способен существовать, размножаться, выживать. Так что без психозов, господа и дамы.
Однако тренироваться на пустой желудок более чем бессмысленно.»Что же делать?» подумаете вы. Ответ вы узнаете в статье «Кардио: когда и зачем?» , которая расскажет вам о последствиях голодных тренировок.
Гликоген печени расщепляется при снижении концентрации глюкозы в крови, прежде всего между приемами пищи. Через 48-60 часов полного голодания запасы гликогена в печени полностью истощаются.
Гликоген мышц расходует во время физической активности. И тут мы опять вернемся к мифу: «Чтобы сжечь жир, нужно бегать не менее 30 минут, поскольку только на 20-й минуте в организме истощаются запасы гликогена и в качестве топлива начинает использоваться подкожный жир», только с чисто математической стороны. Откуда это пошло? А пес его знает!
Действительно, организму проще использовать гликоген, чем окислять жир для энергии, поэтому в первую очередь расходуется он. Отсюда и миф: надо сначала израсходовать ВЕСЬ гликоген, и потом жир начнет гореть, а произойдет это примерно через 20 минут после начала аэробной тренировки. Почему 20? Понятия не имеем.
НО: никто не учитывает, что использовать весь гликоген не так-то просто и 20-ю минутами тут дело не ограничится.
Как мы знаем, общее количество гликогена в организме составляет 300 — 400 граммов, а в некоторых источниках говорится о 500 граммах, что дает нам от 1200 до 2000 ккал! Вы вообще представляете, сколько нужно бегать, чтобы истощить такую прорву калорий? Человек весом в 60 кг должен будет пробежать в среднем темпе от 22 до З5 километров. Ну как, готовы?

источник
Гликоген — полисахарид на основе глюкозы, выполняющий в организме функцию энергетического резерва. Формально соединение относится к сложным углеводам, встречается только в живых организмах и предназначено для восполнения затрат энергии при физических нагрузках.
Из статьи вы узнаете о функциях гликогена, особенностях его синтеза, роли, которую играет это вещество в спорте и диетическом питании.
Говоря простым языком, гликоген (в особенности для спортсмена) – это альтернатива жирным кислотам, которая используется в качестве запасающего вещества. В чем суть? Все просто: мышечных клетках есть специальные энергетические структуры — «гликогеновые депо». В них хранится гликоген, который в случае необходимости быстро распадается на простейшую глюкозу и питает организм дополнительной энергией.
Фактически, гликоген – это основные батарейки, которые используются исключительно для совершения движений в стрессовых условиях.
Прежде чем рассматривать пользу гликогена как сложного углевода, разберемся, почему вообще в организме возникает такая альтернатива — гликоген в мышцах или жировые ткани. Для этого рассмотрим структуру вещества. Гликоген – это соединение из сотен молекул глюкозы. Фактически это чистый сахар, который нейтрализован и не попадает в кровь, пока организм сам его не запросит.
Синтезируется гликоген в печени, которая перерабатывает поступающий сахар и жирные кислоты по своему усмотрению.
Что же такое жирная кислота, которая получается из углеводов? Фактически – это более сложная структура, в которой участвуют не только углеводы но и транспортирующие белки. Последние связывают и уплотняют глюкозу до более трудно расщепляемого состояния. Это позволяет в свою очередь увеличить энергетическую ценность жиров (с 300 до 700 ккал) и уменьшить вероятность случайного распада.
Все это делается исключительно для создания резерва энергии в случае серьезного дефицита калорий. Гликоген же накапливается в клетках, и распадается на глюкозу при малейшем стрессе. Но и синтез его значительно проще.
Сколько гликогена может содержать организм? Здесь все зависит от тренировки собственных энергетических систем. Изначально размер гликогенового депо нетренированного человека минимален, что обусловлено его двигательными потребностями.
В дальнейшем, через 3-4 месяца интенсивных высокообъемных тренировок, гликогеновое депо под воздействием пампинга, насыщения крови и принципа супервосстановления постепенно увеличивается.
При интенсивном и продолжительном тренинге запасы гликогена увеличиваются в организме в несколько раз.
Что в свою очередь приводит к таким результатам:
- возрастает выносливость;
- объём мышечной ткани увеличивается;
- наблюдаются значительные колебания в весе во время тренировочного процесса
Гликоген не влияет напрямую на силовые показатели спортсмена. Кроме того, чтобы увеличивать размер гликогенового депо, нужны специальные тренировки. Так, например, пауэрлифтеры лишены серьезных запасов гликогена в виду и особенностей тренировочного процесса.
Обмен гликогена происходит в печени. Её основная функция — не превращение сахара в полезные нутриенты, а фильтрация и защита организма. Фактически, печень негативно реагирует на повышение сахара в крови, появление насыщенных жирных кислот и физические нагрузки.
Все это физически разрушает клетки печени, которые, к счастью, регенерируют. Чрезмерное потребление сладкого (и жирного), в совокупности с интенсивными физическими нагрузками чревато не только дисфункцией поджелудочной железы и проблемами с печенью, но и серьёзными нарушениями обмена веществ со стороны печени.
Организм всегда пытается адаптироваться к изменяющимся условиям с минимальной энергопотерей. Если создать ситуацию, при которой печень (способная переработать не более 100 грамм глюкозы за раз), будет хронически испытывать переизбыток сахара, то новые восстановленные клетки будут превращать сахар напрямую в жирные кислоты, минуя стадию гликогена.
Этот процесс называется «жировое перерождение печени». При полном жировом перерождении наступает гепатит. Но частичное перерождение считается нормой для многих тяжелоатлетов: такое изменение роли печени в синтезе гликогена приводит к замедлению обмена веществ и появлению избыточной жировой прослойки.
Гликоген в организме выполняет задачу главного энергоносителя. Он накапливается в печени и мышцах, откуда напрямую попадает в кровеносную систему, обеспечивая нас необходимой энергией.
Рассмотрим, как напрямую влияет гликоген на работу спортсмена:
- Гликоген быстро истощается благодаря нагрузкам. Фактически за одну интенсивную тренировку можно растратить до 80% всего гликогена.
- Это в свою очередь вызывает «углеводное окно», когда организм требует быстрых углеводов, для восстановления.
- Под воздействием наполнения мышц кровью, гликогеновое депо растягивается, увеличивается размер клеток, которые могут хранить его.
- Гликоген поступает в кровь только до тех пор, пока пульс не пересечет отметку в 80% от максимального ЧСС. В случае превышения этого порога, недостаток кислорода приводит к стремительному окислению жирных кислот. На этом принципе основана «сушка организма».
- Гликоген не влияет на силовые показатели – только на выносливость.
Интересный факт: в углеводное окно можно безболезненно употреблять любое количество сладкого и вредного, так как организм в первую очередь восстанавливает гликогеновое депо.
Взаимосвязь гликогена и спортивных результатов предельно проста. Чем больше повторений – больше истощения, больше гликогена в дальнейшем, а значит, больше повторений в итоге.
Увы, но накопление гликогена не способствует похудению. Тем не менее, не стоит бросать тренировки и переходить на диеты. Рассмотрим ситуацию подробнее. Регулярные тренировки приводят к увеличению гликогенового депо. Суммарно за год оно способно увеличится на 300-600%, что выражается в 7-12% повышения общего веса. Да, это те самые килограммы от которых стремятся бежать многие женщины. Но с другой стороны, эти килограммы оседают не на боках, а остаются в мышечных тканях, что приводит к увеличению самих мышц. Например, ягодичных.
В свою очередь, наличие и опустошение гликогенового депо позволяет спортсмену корректировать свой вес в короткие сроки. Например, если нужно похудеть на дополнительные 5-7 килограмм за несколько дней, истощение гликогенового депо серьезными аэробными нагрузками поможет быстро войти в весовую категорию.
Другая важная особенность расщепления и накопления гликогена — перераспределение функций печени. В частности, при увеличенном размере депо избыток калорий связывается в углеводные цепочки без превращения их в жирные кислоты. А что это значит? Все просто – тренированный спортсмен меньше склонен к набору жировой ткани. Так, даже у маститых бодибилдеров, вес которых в межсезонье касается отметок в 140-150 кг, процент жировой прослойки редко достигает 25-27%.
Важно понимать, что не только тренировки влияют на количество гликогена в печени. Этому способствует и основная регуляция гормонов инсулина и глюкагона, которая происходит благодаря потреблению определенного типа пищи. Так, быстрые углеводы при общем насыщении организма скорее всего превратятся в жировую ткань, а медленные углеводы полностью превратятся в энергию, минуя гликогеновые цепочки. Так как же правильно определить, как распределится съеденная пища?
Для этого необходимо учитывать следующие факторы:
- Гликемический индекс. Высокие показатели способствуют росту сахара в крови, который нужно в срочном порядке законсервировать в жиры. Низкие показатели,стимулируют постепенное повышение глюкозы в крови, что способствует полному её расщеплению. И только средние показатели (от 30 до 60) способствуют превращению сахара в гликоген.
- Гликемическая нагрузка. Зависимость обратно пропорциональная. Чем ниже нагрузка, тем больше шансов превращения углеводов в гликоген.
- Тип самого углевода. Всё зависит от того, насколько просто углеводное соединение расщепляется на простые моносахариды. Так, например мальтодекстрин с большей вероятностью превратится в гликоген, хотя имеет высокий гликемический индекс. Этот полисахарид попадает напрямую в печень, минуя пищеварительный процесс, и в этом случае его проще расщепить на гликоген, чем превратить в глюкозу и снова пересобрать молекулу.
- Количество углеводов. Если правильно дозировать количество углеводов в один прием пищи, то даже питаясь шоколадками и кексами вам удастся избежать жирового отложения.
Итак, углеводы неравноценны по своей способности превращения в гликоген или в жирные полинасыщенные кислоты. Во что превратится поступающая глюкоза, зависит только от того, в каком количестве она выделится при расщеплении продукта. Так, например, очень медленные углеводы с большой вероятностью вообще не превратятся ни в жирные кислоты, ни в гликоген. В то же время чистый сахар уйдет в жировую прослойку практически целиком.
Примечание редакции: приведённый ниже список продуктов нельзя рассматривать как истину в последней инстанции. Метаболические процессы зависят от индивидуальных особенностей конкретно взятого человека. Мы указываем лишь процентную вероятность, что этот продукт будет более полезным или более вредным для вас.
| Наименование | Гликемический индекс | Процент вероятности полного сжигания | Процент вероятности превращения в жир | Процент вероятности превращения в гликоген |
| Финики сушёные | 204 | 3.7% | 62.4% | Итог |
Гликоген в мышцах и печени особенно важен для атлетов, практикующих кроссфит. Механизмы накопления гликогена предполагают стабильное увеличение базового веса. Тренировка энергетических систем поможет не только достичь высоких спортивных результатов, но и увеличит общий запас дневной энергии. Вы будете меньше уставать и лучше себя чувствовать.
Для спортсмена наращивание гликогеновых запасов — не только необходимость, но и профилактика ожирения. Сложные углеводы могут храниться в мышцах сколь угодно долго, не окисляясь и не распадаясь. При этом любая нагрузка приводит к их растрате и регуляции общего состояния организма.
И напоследок один интересный факт: именно распад гликогена ведет к тому, что большая часть глюкозы попадает через кровь напрямую в ЦНС, стимулируя выброс эндорфинов и улучшая мозговую деятельность.
источник
Гликоген – большая разветвленная молекула с молекулярной массой 10 3 -10 4 кДа (до120 000 остатков глюкозы в молекуле), образует в цитозоле клеток гранулы диаметром до 40 нм. Линейные участки молекулы гликогена построены из молекул глюкозы, соединенных α(1→4)-гликозидными связями, точки ветвления в молекуле образуются α(1→6)- гликозидными связями.
Синтез гликогена (гликогенез) осуществляется почти во всех клетках, но в больших количествах гликоген образуется и накапливается в печени (до 10 % массы органа) и мышечной ткани (1,5-2,0%) Содержание гликогена в других органах значительно меньше.
Рис. 5.3. Схема синтеза гликогена
Образовавшийся в клетке глюкозо-6-фосфат (рис.5.3) вступает на путь синтеза гликогена под действием фосфоглюкомутазы, которая катализирует его превращение в глюкозо-1-фосфат. Эта реакция проходит через стадию образования глюкозо-1,6-дифосфата в активном центре фермента. Глюкоза-1-фосфат взаимодействует с УТФ, в результате чего образуется еще одна активная форма глюкозы – УДФ-глюкоза. Реакция катализируется ферментом УДФ-глюкозо-пирофосфорилазой.
Гликогенсинтаза – фермент, катализирующий образование гликогена, нуждается в затравке (праймере). Функцию праймера выполняет специальный самогликозилирующийся белок – гликогенин.
Гликогенин, используя УДФ-глюкозу в качестве субстрата, образует октосахарид, присоединяя первую молекулу глюкозы к тирозину (Тир-194) при помощи фермента тирозил-гликозилтрансферазы. Этот процесс происходит в комплексе с гликогенсинтазой, которая после формирования октосахарида продолжает наращивать цепь, образуя α(1→4)-гликозидные связи.
Образование мест ветвления обеспечивает фермент ветвления – амило-(1,4→1,6)-трансглюкозидаза. Он образует (1→6)- гликозидную связь, переносит семь остатков глюкозы с одной из длинных боковых цепей гликогена и формирует новую ветвь (рис. 5.4). Образование новой ветви происходит на расстоянии не менее четырех остатков глюкозы от соседней цепи.
Рис.5.4. Функционирование фермента ветвления:
а–место действия фермента ветвления;б– место присоединения цепи из семи остатков глюкозы и создание дополнительного участка ветвления в структуре гликогена
Ветвление повышает гидрофильность молекулы гликогена, при этом в нем увеличивается также количество нередуцирующих концевых остатков – мест действия гликогенсинтазы и фосфорилазы, иными словами, ветвление увеличивает скорость синтеза и распада гликогена.
Пусковым механизмом гликогенолиза является начинающаяся гипогликемия. Голодание в течение суток приводит практически к полному исчерпанию запасов гликогена в печени; очень быстро он расходуется при интенсивной физической нагрузке и стрессовых ситуациях.
Распад гликогена осуществляется двумя путями: 1) гидролитически с участием α-амилазы; 2) фосфоролитически с участием гликогенфосфорилазы. Основным в клетках является второй путь.
Гликогенфосфорилаза при участии фосфорной кислоты последовательно расщепляет линейные α(1→4)- гликозидные связи с освобождением глюкоза-1-фосфата (рис.5.5.).
Рис.5.5. Схема мобилизации гликогена в печени и мышцах
В результате действия гликогенфосфорилазы из гликогена образуется полисахарид с боковыми короткими олигосахаридными цепями – “лимит декстрин”, который становится субстратом специального деветвящего фермента — амило-(1→6)-гликозидазы (рис. 5.6).
Рис.5.6. Функционирование деветвящего фермента:
а– трансферазная активность деветвящего фермента;б–амило-1,6-глюкозидазная активность;с–места действия фосфорилазы или-амилазы
Этот фермент катализирует две реакции. Вначале он переносит 3 остатка глюкозы на другую ветвь гликогена (трансферазная активность), а затем гидролизует α(1→6)-гликозидную связь и освобождает молекулу глюкозы у точки ветвления (глюкозидазная активность).
Вслед за действием деветвящего фермента, включается вновь гликогенфосфорилаза. Отщепившийся под влиянием гликогенфосфорилазы глюкоза-1-фосфат превращается в глюкозо-6-фосфат (фермент – фосфоглюкомутаза).
В мышцах глюкозо-6-фосфат не переходит в свободную глюкозу и используется как основной иточник энергии. В печени (а также в почках) имеется фермент глюкозо-6-фосфатаза, под действием которого образуется свободная глюкоза. Поскольку последняя способна проходить через плазматическую мембрану клеток в межклеточное пространство, печень является основным органом, поддерживающим нормальный уровень глюкозы в крови.
NB! Регуляция обмена гликогена органоспецифична
Гликоген находится в цитозоле вместе с ферментами, его синтезирующими и разрушающими, поэтому существует большая вероятность возникновения замкнутого круга метаболизма, при котором продукты распада гликогена тотчас же будут использоваться на его синтез и требуется тонкая регуляция взаимоотношений участников этих процессов. Основными регулируемыми ферментами являются гликогенсинтаза и фосфорилаза. Каждый их этих ферментов может находиться в двух конформационных состояних: активном (R, расслабленном) и неактивном (Т, напряженном) и регуляторы поддерживают эти состояние реципрокно. Если один из ферментов находится в R-конформации, то другой – в Т и наоборот. У каждого из ферментов имеются свои аллостерические регуляторы, а также важное место в их регуляции принадлежит ковалентной модификации структуры.
Гликогенфофорилаза представляет гомодимер с молекулярной массой 97 кДа. В образовании активного центра участвуют обе субъединицы. Важную роль в катализе фосфоролиза гликогена играет фосфопиридоксаль, который ковалентно связан с лизином активного центра.
Гликоген в печени и мышцах используется по-разному, и это сказывается на принципах регуляции активности фосфорилазы в этих органах. Мышечная фосфорилаза может находиться в двух формах фосфорилированной (R-форма, фосфорилаза а) и дефосфорилированной (Т-форма, фосфорилаза b). Переход одной формы в другую катализируется ферментом киназой фосфорилазы, которая фосфорилирует серин фосфорилазы. В покоящейся мышце преобладает фосфорилаза b.
Аллостерические регуляторы мышечной фосфорилазы АМФ и АТФ. Они связываются со специальным нуклеотидсвязывающим центром. Связывание с АМФ переводит фосфорилазу b в активную R-конформацию, а с АТФ – в Т-конформацию. Глюкозо-6-фосфат также стабилизирует Т-конформацию. Печеночная фосфорилаза не чувствительна к действию АМФ, но активность фосфорилазы а ингибируется глюкозой, что важно при регуляции уровня сахара в крови, источником которой служит гликоген печени.
Гликогенсинтаза также может находится в двух конформационных состояниях: гликогенсинтаза b –неактивная, ингибируется по аллостерическому механизму АТФ,АДФ, и гликогенсинтаза а –активная, активируется глюкозо-6-фосфатом.
Ковалентная модификация ведущих ферментов обмена гликогена выражается в цикле “фосфорилирование-дефосфориилрование”. Эти процессы катализируются специальными протеинкиназами, которые составляют часть каскадных механизмов действия гормонов на клетки.
Фосфорилирование гликогенфосфорилазы происходит при участии киназы фосфорилазы. Это сложный фермент с молекулярной массой 1200 кДа, состоящий из четырех типов субъединиц:
4 субъединицы — каталитические субъединицы;
4 субъединицы – регуляторные субъединицы, фосфорилируются протеинкиназой А и при этом активируются;
4субъединицы представлены кальмодулином – белком, связывающим Ca 2+ и активирующим данную киназу.
Такое строение фермента показывает, что киназа фосфорилазы является ферментом, активность которого изменяется под влиянием вторичных посредников, образующихся в каскадных механизмах усиления нескольких гормонов (инсулина, адреналина и глюкагона).
Дефосфорилирование гликогенфосфорилазы и киназы фосфорилазы катализируется фосфопротеинфосфатазой 1, которая переводит эти ферменты в неактивное (напряженное) состяние. Фосфопротеинфосфатаза 1 состоит из трех субъединиц:
G1-субъединицы, которая связывает гликоген и
ингибитора 1, который в фосфорилированной форме тормозит активность протеинфосфатазы.
Фосфорилирование гликогенсинтазы вызывает ее ингибирование и катализируется рядом протеинкиназ, связанных с каскадами действия гормонов: кальмодулинзависимой протеинкиназой, протеинкиназой С, киназой-3 гликогенсинтазы.
Рис. 5.7. Гормональный контроль гликогенолиза и гликогенеза
Адреналин и глюкагон, активируя аденилатциклазу, способствуют образованию цАМФ, который запускает “каскадный” механизм фосфорилирования ферментов распада и синтеза гликогена. В результате фосфорилирования образуется фосфорилированная, т.е. активная гликогенфосфорилаза и фосфорилированная, т.е. неактивная гликогенсинтаза. В этих условиях будет осуществляться распад гликогена (рис .5.7).
Напротив, под действием инсулина, включающего механизм дефосфорилирования ключевых ферментов, появятся дефосфорилированная, т.е. неактивная гликогенфосфорилаза, и дефосфорилированная, т.е. активная, гликогенсинтаза. В этих условиях будет происходить синтез гликогена.
Активность обоих ключевых ферментов синтеза и распада гликогена в печени регулируется также Са ++ – выход кальция из внутриклеточных депо в цитозоль клетки контролируется инозитолтрифосфатом, который освобождается фосфолипазой С при распаде входящего в состав мембраны фосфатидилинозитол пирофосфата.
источник
Гликоген – это запасной углевод животных, состоящий из большого количества остатков глюкозы. Запас гликогена позволяет быстро восполнять недостаток содержания в крови глюкозы, как только её уровень понижается, происходит расщепление гликогена, и в кровь поступает свободная глюкоза. В организме человека глюкоза в основном хранится в виде гликогена. Запасать отдельные молекулы глюкозы клеткам не выгодно, так как это значительно повышало бы осмотическое давление внутри клетки. По своей структуре гликоген напоминает крахмал, то есть полисахарид, который в основном запасают растения. Крахмал тоже состоит из остатков глюкозы, соединённых между собой, однако в молекулах гликогена гораздо больше разветвлений. Качественная реакция на гликоген – реакция с йодом – даёт бурое окрашивание, в отличие от реакции йода с крахмалом, которая позволяет получить фиолетовое окрашивание.
Образование и расщепление гликогена регулируют несколько гормонов, а именно :
1) инсулин
2) глюкагон
3) адреналин
Образование гликогена происходит после того, как концентрация глюкозы в крови повышается: раз глюкозы много, то её необходимо запасти впрок. Поглощение глюкозы клетками в основном регулируется двумя гормонами-антагонистами, то есть гормонами с противоположным действием: инсулином и глюкагоном. Оба гормона выделяются клетками поджелудочной железы.
Обратите внимание: слова «глюкагон» и «гликоген» очень похожи, но глюкагон – это гормон, а гликоген – запасной полисахарид.
Инсулин синтезируется, если глюкозы в крови много. Это обычно бывает после того, как человек поел, в особенности если еда — это богатая углеводами пища (например, если съесть мучное или сладкое). Все углеводы, которые содержатся в пище, расщепляются до моносахаридов, и уже в таком виде через стенку кишечника всасываются в кровь. Соответственно, уровень глюкозы повышается.
Когда рецепторы клеток реагируют на инсулин, клетки поглощают глюкозу из крови, и её уровень вновь снижается. Кстати, именно поэтому диабет – недостаток инсулина – образно называют «голод среди изобилия», ведь в крови после употребления пищи, которая богата углеводами, появляется очень много сахара, но без инсулина клетки не могут его поглотить. Часть глюкозы клетки используют для получения энергии, а оставшуюся превращают в жир. Клетки печени используют поглощённую глюкозу для синтеза гликогена. Если же в крови мало глюкозы, то происходит обратный процесс: поджелудочная железа выделяет гормон глюкагон, и клетки печени начинают расщеплять гликоген, выделяя глюкозу в кровь, или синтезировать глюкозу заново из более простых молекул, таких как молочная кислота.
Адреналин также приводит к распаду гликогена, потому что всё действие этого гормона направлено на то, чтобы мобилизовать организм, подготовить его к реакции по типу «бей или беги». А для этого необходимо, чтобы концентрация глюкозы стала выше. Тогда мышцы смогут использовать её для получения энергии.
Таким образом, поглощение пищи приводит к выделению в кровь гормона инсулина и синтезу гликогена, а голодание – к выделению гормона глюкагона и распаду гликогена. Выделение адреналина, происходящее в стрессовых ситуациях, также приводит к распаду гликогена.
Субстратом для синтеза гликогена, или гликогеногенеза, как его по-другому называют, служит глюкозо-6-фосфат. Это молекула, которая получается из глюкозы после присоединения к шестому атому углерода остатка фосфорной кислоты. Глюкоза, образующая глюкозо-6-фосфат, попадает в печень из крови, а в кровь – из кишечника.
Возможен и другой вариант: глюкоза может быть заново синтезирована из более простых предшественников (молочной кислоты). В таком случае из крови глюкоза попадает, например, в мышцы, где расщепляется до молочной кислоты с выделением энергии, а потом накопленная молочная кислота транспортируется в печень, и клетки печени заново синтезируют из неё глюкозу. Потом эту глюкозу можно превратить в глюкозо-6-фосфот и далее на его основе синтезировать гликоген.
Итак, что же происходит в процессе синтеза гликогена из глюкозы?
1. Глюкоза после присоединения остатка фосфорной кислоты становится глюкозо-6-фосфатом. Это происходит благодаря ферменту гексокиназе. Этот фермент имеет несколько разных форм. Гексокиназа в мышцах немного отличается от гексокиназы в печени. Та форма этого фермента, которая присутствует в печени, хуже связывается с глюкозой, а продукт, образующийся в ходе реакции, не ингибирует протекание реакции. Благодаря этому клетки печени способны поглощать глюкозу только тогда, когда её много, и могу сразу превратить в глюкозо-6-фосфат очень много субстрата, даже если не успевают его переработать.
2. Фермент фосфоглюкомутаза катализирует превращение глюкозо-6-фосфата в его изомер — глюкозо-1-фосфат.
3. Полученный глюкозо-1-фосфат потом соединяется с уридинтрифосфатом, образуя УДФ-глюкозу. Катализирует этот процесс фермент УДФ-глюкозопирофосфорилаза. Эта реакция не может протекать в обратную сторону, то есть является необратимой в тех условиях, которые присутствуют в клетке.
4. Фермент гликогенсинтаза переносит остаток глюкозы на формирующуюся молекулу гликогена.
5. Гликогенразветвляющий фермент добавляет точки ветвления, создавая новые «веточки» на молекуле гликогена. Позже на конец этого ответвления добавляются новые остатки глюкозы с помощью гликогенсинтазы.
Гликоген – это необходимый для жизни запасной полисахарид, и хранится он в виде небольших гранул, находящихся в цитоплазме некоторых клеток.
Гликоген запасают следующие органы :
1. Печень. В печени гликогена довольно много, и это единственный орган, который использует запас гликогена для регуляции концентрации сахара в крови. До 5-6 % может составлять гликоген от массы печени, что примерно соответствует 100-120 граммам.
2. Мышцы. В мышцах запас гликогена меньше в процентном соотношении (до 1 %), однако суммарно по весу может превосходить весь гликоген, запасённый в печени. Мышцы не выделяют ту глюкозу, которая образовалась после распада гликогена, в кровь, они используют её только для своих собственных нужд.
3. Почки. В них обнаружено незначительное количество гликогена. Ещё меньшие количества были найдены в глиальных клетках и в лейкоцитах, то есть белых кровяных клетках.
В процессе жизнедеятельности организма гликоген синтезируется довольно часто, практически каждый раз после еды. Организму нет смысла запасать огромные количества гликогена, ведь основная его функция – это не служить донором питательных веществ как можно дольше, а регулировать количество сахара в крови. Запасов гликогена хватает на срок около 12 часов.
Для сравнения, запасённые жиры :
— во-первых, обычно имеют массу гораздо большую, чем масса запасённого гликогена,
— во-вторых, их может хватить на месяц существования.
К тому же стоит отметить, что организм человека может превращать углеводы в жиры, но не наоборот, то есть запасённый жир превратить в гликоген никак не получится, только напрямую использовать для получения энергии. А вот расщепить гликоген до глюкозы, потом разрушить саму глюкозу и использовать получившийся продукт для синтеза жиров организм человека вполне в состоянии.
источник
Одним из наиболее важных влияний инсулина является депонирование в печени всасываемой после приема пищи глюкозы в виде гликогена. В промежутках между приемами пищи, когда нет поступлений питательных веществ и концентрация глюкозы в крови начинает снижаться, параллельно быстро снижается секреция инсулина. Гликоген в печени начинает распадаться до глюкозы, которая высвобождается в кровь и препятствует падению концентрации глюкозы до слишком низкого уровня.
Механизм, с помощью которого инсулин обеспечивает поступление и депонирование глюкозы в печени, включает несколько почти одновременных этапов.
1. Инсулин инактивирует фосфорилазу печени— основной фермент, способствующий распаду гликогена печени до глюкозы. Это предупреждает распад гликогена, который в таком случае запасается в клетках печени.
2. Инсулин обеспечивает усиление поступления глюкозы из крови в клетки печени. Это достигается увеличением активности фермента глюкокиназы, являющейся одним из ферментов, инициирующих фосфорилирование глюкозы после ее диффузии в клетки печени. После фосфорилирования глюкоза временно остается как бы в ловушке в клетке печени, т.к. в такой форме она не может диффундировать обратно через клеточную мембрану.
3. Инсулин также увеличивает активность ферментов, обеспечивающих синтез гликогена, особенно гликогенсинтетазы, ответственной за полимеризацию моносахаридов — единиц, из которых образуется молекула гликогена.
Значение всех этих изменений заключается в увеличении содержания гликогена в печени. В целом содержание гликогена в печени при увеличении его синтеза может составить 5-6% массы печени, что соответствует приблизительно 100 г гликогена, составляющего депо гликогена в печени.
Глюкоза высвобождается из печени в промежутках между приемами пищи. Если уровень глюкозы в крови начинает снижаться до нижнего предела в промежутках между приемами пищи, это приведен к ряду изменений и послужит поводом для высвобождения глюкозы из печени в кровоток.
1. Снижение уровня глюкозы приводит к снижению секреции инсулина поджелудочной железой.
2. Отсутствие инсулина приведет к изменению направления реакций, нацеленных на создание запаса гликогена, главным образом к остановке дальнейшего синтеза гликогена в печени и предупреждению поступления глюкозы в печень из крови.
3. Отсутствие инсулина (параллельно с увеличением глюкагона, что будет рассмотрено далее) активирует фермент фосфорилазу, расщепляющую гликоген до глюкозофосфата.
4. Фермент глюкофосфатаза, ингибируемый инсулином, при отсутствии инсулина активируется и приводит к отщеплению фосфатного радикала от глюкозы, что позволяет свободной глюкозе вернуться в кровь.
Таким образом, печень забирает глюкозу из крови, когда в крови возникает ее избыток в связи с приемом пищи, и возвращает ее в кровь, когда концентрация глюкозы снижается в промежутках между приемами пищи. Обычно около 60% глюкозы пищи запасается таким способом в печени и в последующем возвращается в кровь.
Инсулин обеспечивает превращение избытка глюкозы в жирные кислоты и ингибирует глюконеогенез в печени.
Если поступление глюкозы превышает возможности запасания ее в виде гликогена или возможности ее локальных метаболических превращений в гепатоцитах, инсулин обеспечивает превращение избытка глюкозы в жирные кислоты. Жирные кислоты впоследствии в виде триглицеридов переводятся в липопротеины очень низкой плотности и в таком виде транспортируются кровью в жировую ткань, где депонируются в виде жира.
Инсулин также тормозит глюконеогенез. Это достигается снижением как количества, так и активности ферментов, необходимых для глюконеогенеза. Однако эти эффекты частично вызваны снижением высвобождения аминокислот из мышц и других внепеченочных тканей и вследствие этого — снижением необходимого для глюконеогенеза сырья. Это будет обсуждаться далее в связи с влиянием инсулина на обмен белка.
источник