Часто после проведения обследования пациенты буквально впадают в панику, обнаруживая непонятные им специфические медицинские термины, например, «гипоэхогенное образование в печени». В этом случае пугаться не стоит, так как этот термин не означает заболевание, а лишь является характеристикой обнаруженного в печени образования.
Гипоэхогенное образование в печени
При проведении ультразвукового обследования могут обнаруживаться особые участки, которые отличаются от других тканей органа более низкой плотностью. Аппарат УЗИ посылает в орган звуковые волны высокой частоты.
Структуры органа, имеющие разную плотность и строение, по-разному отражают эти волны, которые возвращаются обратно, фиксируются особыми датчиками аппарата УЗИ и формируют картину состояния органа. Если в структуре органа имеется образование или участок с более низкой плотностью, чем другие части или ткани, оно будут выглядеть на экране УЗИ как гипоэхогенное образование в печени.
Обследование на УЗИ позволяет не просто определить наличие таких образований, но и узнать их месторасположение, количество и размеры. На экране гипоэхогенная зона выглядит как темное пятно. Чаще всего в роли таких образований выступает участок ткани в виде полости, заполненной жидкостью. Она обычно бывает окружена тонкими стенками, отделяющими ее от соседних тканей. У нее могут быть гладкие ровные края или же неровные очертания.
Наличие гипоэхогенных зон свидетельствует о патологии в печени, однако она может быть как доброкачественной, так и злокачественной природы.
Четкие ровные контуры структуры могут указывать на ее паразитарное происхождение, например, на лямблии или эхинококки в печени, окруженные плотной капсулой, или же на наличие обычной кисты. Криволинейные или расплывчатые образования также могут оказаться кистами, опухолями различного происхождения или фиброаденомами.
Выявление таких участков в печени потребуют дополнительных исследований и взятия анализов. Если существует онкологическая настороженность, может возникнуть необходимость при возможности взятия биопсии образования, чтобы исключить раковую опухоль или же метастаз.
Симптомы гипоэхогенного образования в печени
Больной обращается за медицинской помощью и обследованием, если ощущает постоянный дискомфорт в области печени. Это может выражаться:
- Болями в правом боку и эпигастральной области – рвущими, ноющими или колющими.
- Часто боли сопровождаются изжогой и тошнотой после приема пищи, чувством горечи во рту, особенно хорошо ощутимым с утра, увеличением печени, отсутствием аппетита или искажением вкуса.
- Некоторые больные жалуются на необъяснимое и достаточно резкое снижение веса
- Появление желтых пятен или пожелтению кожных покровов и белков глаз, зуду кожи.
Все эти симптомы могут относиться к разнообразным патологиям печени и желчного пузыря. Так как они очень субъективны, то четко указывать на конкретное заболевание не могут.
Само наличие участков затемнения на эхограмме не означает обязательной патологии, однако сочетания субъективных жалоб и показания УЗИ – это повод для углубленного исследования с целью исключения опасных для жизни заболеваний, таких как цирроз и рак печени, метастазы в этот орган или глистная инвазия.
Ультразвуковое исследование печени
Проведение УЗИ-диагностики поможет выявить наличие разнообразных образований и дать возможность разобраться в причинах недомогания больного.
Иногда по внешнему облику, которое имеет гипоэхогенное образование в печени, можно сделать первичные выводы об имеющейся проблеме:
- Аденомы проявляются затененными участками с однородной структурой, возможно, с единичными включениями материала другой плотности и гладким краем.
- На абсцессы печени могут указывать многочисленные очаги инфицирования с неровными контурами, возможно, с включениями пузырей внутри, при этом внешняя оболочка плотная и хорошо отражающая сигналя УЗИ.
- Ровные контуры темного пятна с имеющимися внутри него отраженными сигналами ультразвуковых волн могут указывать на кисту с внутренними одиночными или множественными кровоизлияниями.
- Круглые с бугристым краем образования могут свидетельствовать о наличии цирроза печени.
- Если образования имеют форму овала и/или треугольника, локализуются возле воротной вены или желчного пузыря, а у пациента имеются признаки жирового перерождения печени, логично предположить, что это оставшиеся нетронутыми части здоровой печеночной ткани.
- Если на экране возникает неравномерное образование с фрагментами кальцификатов, кровоизлияниями, это дает возможность заподозрить смертельно опасное заболевание – рак печени.
- Метастазы из других органов также имеют неравномерные очертания без четких контуров, при этом основные ткани печени без изменений.
- Глистные капсулы читаются как четкие образования, обычно округлой или овальной формы, с плотным гладким краем и полостью, заполненной жидкостью. Внутри капсулы имеются участки уплотнений, заметные на экране.
Диагностика при помощи УЗИ позволяет «вычислить» наличие патологий и несколько сузить круг возможных заболеваний. Эта несложная для пациента процедура помогает лечащему врачу в проведении дальнейших исследований и точной постановке диагноза.

Каждое из выявленных при помощи УЗИ заболеваний печени имеет свое специфическое лечение. Например, лечение цирроза зависит от степени заболевания и включает в себя как медикаментозное лечение, так и полное изменение больным образа жизни. Иногда для спасения жизни пациента приходится прибегать к оперативному вмешательству с целью удаления очага заболевания или же полной пересадки всего органа.
При лечении абсцессов активно используются антибиотики, которые назначаются лечащим врачом с учетом всех имеющихся у пациента заболеваний, его возраста и стадии болезни. Обязательно принимается во внимание возможная индивидуальная реакция на лекарства и склонность к аллергиям.
Если УЗИ дает основание заподозрить рак или метастазы, обследования должны проводиться глубже и тщательнее для выявления очага заболевания и подтверждения (или опровержения) диагноза.
Если данные находят свое подтверждение, больного передают онкологам, ему назначают специфическое противоопухолевое лечение , которое зависит от типа опухоли, а если это метастаз, то лечение должно быть направлено против основного очага и способствовать уменьшению и исчезновению метастазов. Не все обнаруженные участки пониженной плотности требуют лечения, по крайней мере, медикаментозного. В некоторых случаях достаточно соблюдения диеты, похудения и смены образа жизни, поэтому пугаться заключения УЗИ совершенно не стоит.
Больше информации о подготовке к УЗИ печени можно узнать из видео.
источник
Первичный рак печени по гистогенезу разделяют на гепатоцеллюлярный рак, исходящий из гепатоцитов, холангиоцеллюлярный рак или холангиокарцинома), исходящий из эпителия желчных протоков, и смешанный гепатохолангиоцеллюлярный рак. Основная доля поражений приходится на гепатоцеллюлярный рак, в то время как холангиоцеллюлярный рак считается относительно редким заболеванием и составляет около 10% всех злокачественных опухолей печени [Parkin et al., 1993].
Ультразвуковая картина при первичном раке печени весьма разнообразна. Обычно первичный рак печени характеризуется наличием объемных образований в печени, одиночных или множественных (узловая форма). Вместе с тем существует диффузная форма первичного рака печени, эхографическое изображение которой в ряде случаев напоминает цирротические изменения органа (надежные критерии дифференциальной диагностики этих заболеваний отсутствуют до настоящего времени).
Выделяют несколько типов ультразвукового изображения узловой формы первичного рака печени [Догра, Рубенс, 2005]:
1) гиперэхогенный, наиболее часто встречающийся;
Наиболее часто первичный рак печени локализуется в правой доле, в толще паренхимы. Поверхностное субкапсульное расположение встречается значительно реже. Размеры и форма первичного рака печени вариабельны. При выявлении достаточно крупных образований (более 4-5 см в диаметре) определяется увеличение размеров печени, сопровождающееся неровностью контуров в месте поражения. Отмечается аномальный ход сосудов и желчных протоков в проекции опухоли, ампутация крупных сосудистых стволов, а в ряде случаев сегментарное либо генерализованное расширение желчных протоков.
Прорастание первичного рака печени в магистральные сосуды органа в итоге приводит к нарушению печеночной гемодинамики: поражение системы воротной вены в 30-68% случаев заканчивается формированием опухоли или тромба в полости сосуда; вовлечение в неопластический процесс печеночных вен и реже нижней полой вены вызывает развитие синдрома Бадда—Киари. Злокачественные новообразования обильно кровоснабжаются. В цветовом, особенно энергетическом, допплеровском режиме может визуализироваться хаотический рисунок сосудистой сети опухоли [Митьков В.В. и др., 1999].
Ультразвуковые признаки узловой формы первичного рака печени отличаются вариабельностью и не являются патогномоничными в дифференциальной диагностике гепатоцеллюлярного рака с холангиоцеллюлярным раком.
Около половины очаговых образований при гепатоцеллюлярном раке (53%) имеют изоэхогенное изображение относительно печеночной паренхимы, при холангиоцеллюлярном раке этот признак наблюдается только у 30% больных. Гиперэхогенная картина опухоли выявлена у 40% больных с холангиокарциномами и только в 13% случаев при печеночноклеточном раке. Эхонегативные участки внутри объемных образований чаще наблюдают при гепатоцеллюлярном раке.
Нечеткость и неровность контуров более характерна для холангиоцеллюлярного рака. Вероятность диагноза холангиоцеллюлярного рака повышается, если наличие опухоли сопровождается внутрипеченочной сегментарной или генерализованной билиарной гипертензией.
Дифференциально-диагностическим признаком первичного рака печени относительно других солидных образований печени может быть эхонегативная окантовка изображений опухоли или отдельных узлов в ней (встречается одинаково часто при гепатоцеллюлярном и холангиоцеллюлярном раках: в 60-70% случаев).
Диффузная форма первичного рака печени при ультразвуковом исследовании может быть представлена 2 вариантами изображений: множественные узлы различного размера и эхогенности во всех отделах печени и крупноочаговая неоднородность печеночной паренхимы смешанной эхогенности, при которой отдельные узлы практически не дифференцируются.
В обоих вариантах печень обычно увеличена, часто с бугристыми контурами. Структура паренхимы неоднородна, по типу множественного очагового либо крупноочагового диффузного поражения. Наблюдаются выраженные нарушения сосудистого рисунка печени. При многоузловом варианте диффузной формы первичного рака печени отмечается деформация и сдавление венозных сосудов органа. Для крупноочагового диффузного поражения печени характерно обеднение сосудистого рисунка, включая крупные ветви воротной и печеночных вен, деформация и ампутация сосудов.
Изменения сосудистой архитектоники печени и хаотический рисунок сосудистой сети опухоли лучше выявляются в цветовом и особенно энергетическом допплеровском режимах. При диффузной форме первичного рака печени часто наблюдается быстрое развитие портальной и билиарной гипертензии, обусловленных выраженными нарушениями структуры печени и ее анатомических образований.
При ультразвуковом исследовании возникают сложности в дифференциальной диагностике злокачественных и доброкачественных опухолей, первичного и вторичного рака, а также злокачественных опухолей и других очаговых поражений печени (абсцесс, альвеококк).
Метастазы — наиболее часто встречаемые злокачественные опухоли печени. Могут быть одиночными и множественными (в 90% случаев). При метастатическом поражении наблюдается деформация контуров, локальное или генерализованное увеличение, очаговая неоднородность структуры печени. Одиночные метастазы приводят к локальному сдавлению и смещению сосудистого рисунка печени. Массивное очаговое поражение вызывает выраженное изменение ангиоархитектоники органа с обеднением сосудистого рисунка. Ультразвуковая картина вторичных опухолей весьма разнообразна и может быть представлена несколькими вариантами.
• Гиперэхогенный (образования с четкими контурами, повышенной эхогенности, чаще неоднородные).
Дифференциальная диагностика с гемангиомами печени, очаговой жировой инфильтрацией и очаговым фиброзом печени, первичным раком печени. Осложненными формами этого варианта эхоскопической картины вторичных опухолей, по мнению В. Догра и Д.Дж. Рубенса (2005), являются метастазы типа «бычий глаз» (гипоэхогенный центр и гиперэхогенная периферия) и «мишень» (гиперэхогенная центральная часть и гипоэхогенная периферия). В ряде публикаций эта разновидность вторичных опухолей выделяется в отдельный вариант ультразвуковой картины [Митьков В.В., Брюховецкий Ю.А, 1996). Дифференциальная диагностика практически со всеми известными очаговыми поражениями печени.
• Изоэхогенный (образования по структуре и эхогенности практически неотличимы от печеночной паренхимы). Дифференциальная диагностика с очаговой узловой гиперплазией печени, ПРП.
Имеют ряд черт, присущих опухолям: отсутствие капсулы, неоднородная внутренняя структура при полипозиционном исследовании с применением соответствующей частоты датчика в режиме двойной гармоники, отсутствие эффекта дистального псевдоусиления тканей, увеличение размеров и количества образований при динамическом исследовании в относительно короткие промежутки времени.
Дифференциальная диагностика с простыми, нагноившимися и малигнизированными кистами, некротизированным первичным раком печени, абсцессами печени, кавернозными гемангиомами, эхинококкозом.
• Смешанной эхогенности или диффузный (образования с неоднородной внутренней структурой, часто плохо дифференцируемые на фоне паренхимы печени, особенно при наличии диффузных изменений органа).
Такие осложнения описторхоза, как кисты, абсцессы и холангиогенные опухоли печени требуют динамического наблюдения либо оперативного лечения.
Существование описторхозных кист, как самостоятельного поражения печени, доказано патоморфологическими исследованиями. Описторхозные кисты развиваются у лиц с массивной и супермассивной степенью инвазии в результате длительной желчной гипертензии. Они представляют собой резко расширенные желчные ходы с сохраненной или частично разрушенной стенкой, окруженной фиброзной тканью. Содержат желчь, слизь, экссудат, яйца описторхов или самих паразитов.
Описторхозные кисты вариабельны по форме, как правило, небольших или средних размеров, чаще множественные. Обычно они расположены в периферических отделах печени, субкапсульно или по ходу портальных трактов с преимущественной локализацией в левой доле, что связано с худшими условиями желчеоттока.
Ультразвуковая картина описторхозных печеночных кист соответствует признакам простых кист: в 95,5% наблюдений это жидкостные образования с однородным анэхогенным содержимым, тонкостенные, с неровными, чаще фестончатыми контурами. В 4,1% случаев в просвете кист отмечались хлопьевидные включения, а в 2,7% наблюдений — единичные внутренние перегородки [Толкаева М.В., 1999].
В дифференциальной диагностике помогают дополнительные ультразвуковые признаки описторхозного поражения, наблюдаемые у 83% пациентов с кистами печени: повышение эхогенности стенок внутрипеченочных желчных протоков и перипортальных тканей, наличие холангиоэктазов в периферических отделах печени, увеличение желчного пузыря с внутриполостными осадочными и хлопьевидными включениями.
Описторхозные абсцессы печени относятся к редким, но наиболее тяжелым по течению и трудным для диагностики осложнениям описторхоза.
По данным Н.А. Бражниковой (1989), в общей структуре хирургических осложнений описторхоза абсцессы составляют 2,56%.
Описторхозные абсцессы обычно развиваются на фоне гнойного холангита, но в ряде случаев возникают как следствие нагноения кист печени или тромбоза сосудов портальной системы.
Существует два типа ультразвукового изображения гнойников при описторхозе [Толкаева М.В., 1999].
• Абсцессы I типа. Располагаются в задних сегментах правой доли печени (S6-S7) и являются следствием локального нарушения дренирования сегмента или субсегмента органа. Представляют собой крупные неоднородные фрагменты печеночной паренхимы повышенной эхогенности без четких границ, от 6,5 до 9,0 см в диаметре, соответствующие зоне воспалительной инфильтрации. Участки деструкции внутри инфильтрата определяются в виде небольших очагов пониженной плотности или жидкостных включений неправильной, иногда древовидной формы с размытыми контурами.
Описторхозные абсцессы I типа при адекватной консервативной терапии не нуждаются в оперативном лечении. Дифференциальная диагностика с пиогенными абсцессами может вызывать затруднения.
• Абсцессы II типа. Имеют холангиогенное происхождение, развиваются на почве холангиоэктазов вследствие желчной гипертензии и гнойного холангита. Представляют собой множественные локально расширенные внутрипеченочные желчные протоки с утолщенными и уплотненными стенками на фоне общего повышения эхогенности ткани печени вследствие ее воспалительной инфильтрации. В просвете холангиоэктазов определяется слабоэхогенное содержимое, обусловленное гноем и детритом.
Для абсцессов II типа характерна множественная локализация в обеих долях печени, небольшие размеры, быстрое развитие печеночной недостаточности. Холангиогенные абсцессы требуют экстренного хирургического вмешательства. Отсутствие своевременного лечения (причиной чего может быть трудность диагностики) приводит к перфорации абсцессов с развитием гнойного перитонита, поддиафрагмальных и подпеченочных абсцессов, забрюшинных флегмон. Описторхозные абсцессы II типа эхоскопически не имеют существенных отличий от холангитических абсцессов непаразитарной этиологии.
Наиболее серьезное осложнение длительно существующего описторхоза — первичный рак печени. В регионах, эндемичных по описторхозу, частота первичного рака печени в 3—9 раз выше, чем на остальных территориях [Шайн А.А., 1972]. Преобладающей формой первичного рака печени при описторхозе является холангиоцеллюлярный рак. Развитие холангиоцеллюлярного рака — многофакторный процесс, при котором паразиты играют роль стимуляторов злокачественного роста.
В зависимости от уровня поражения желчных протоков у больных описторхозом, существует 3 типа эхоскопической картины холангиоцеллюлярного рака печени [Толкаева М.В., 1999].
• Опухоли внутрипеченочной локализации. Развиваются из мелких внутрипеченочных желчных протоков и характеризуются диффузно-инфильтративными изменениями паренхимы периферических отделов печени. Визуализируются в виде фрагментов гиперэхогенной ткани сглаженной структуры, без четких границ, с внутренними мелкими очагами пониженной или повышенной плотности и кальцинатами.
Часто сопровождаются мелкими холангиоэктазами в периферических отделах печени в зоне поражения. Дополнительный признак описторхозной инвазии — выраженные перидуктальные фиброзноинфильтративные изменения тканей, местами с элементами обызвествления. Опухоли внутрипеченочной локализации при описторхозе наиболее трудны для ультразвуковой диагностики в связи с диффузно-инфильтративным характером роста и невозможностью определения истинных границ поражения.
• Опухоли с поражением ворот печени (центральная локализация). Характеризуются наличием в области портальных ворот печени объемного образования небольших размеров (до 3—5 см), без четких контуров, гипер-, изо- или гипоэхогенного относительно печеночной паренхимы. Сопровождаются обструкцией желчных протоков в зоне поражения и расширением проксимальной части внутрипеченочных желчных протоков.
• Опухоли с поражением дистальных желчных протоков. Для холангиоцеллюлярного рака характерно длительное бессимптомное течение заболевания. Сложности визуализации опухолей при ультразвуковом исследовании определяют позднюю диагностику. К моменту постановки диагноза у 85,7% больных имеется метастатическое поражение печени и лимфатических узлов.
Ультразвуковое исследование благодаря своей неинвазивности, информативности и точности получаемой информации является ценнейшим диагностическим методом, дающим возможности в большинстве случаев верифицировать диагноз очагового поражения печени до такой степени достоверности, что использование других диагностических методов становится необязательным. Сочетание ультразвукового метода исследования с допплерографией позволяет выяснить взаимоотношения патологического очага с сосудисто-протоковыми структурами печени и достаточно точно планировать объем и характер предстоящего оперативного вмешательства.
источник
Очаговыми образованиями (или очагами) печени называют единичные или множественные участки изменения ее структуры, которые бывают самого разного происхождения – как доброкачественного, так и злокачественного.
Чаще всего очаги выявляются при УЗИ, но иногда являются случайной находкой при компьютерной томографии или МРТ, когда исследование выполнялось по какой-то иной причине. При этом КТ используется для уточнения размеров, количества, расположения и структуры очагов. При этом по результатам КТ врач, как правило, должен ответить на вопросы о характере изменений: имеем ли мы дело с доброкачественным процессом (например, кистой или гемангиомой), либо злокачественным процессом (рак, метастазы, и т.п.). В ряде случаев после выполнения КТ диагноз остается сомнительным. В таких случаях рекомендуется получить второе медицинское мнение по результатам исследования.
Иногда патологическое образование печени выявляется при сцинтиграфии или ПЭТ (очаг гиперфиксации РФП).
Все объемные образования печени, выявленные при компьютерной томографии, можно разделить в зависимости от следующих параметров:
1) Плотность – характеристика любой ткани организма, которая измеряется на компьютерных томограммах в т.н. единицах Хаунсфилда. В зависимости от рентгеновской плотности очаги бывают гипо-, гипер- и изоденсными по отношению к окружающей нормальной паренхиме. По плотности можно предположить, что находится в структуре очага: кровь, другая жидкость, мягкотканный компонент. Более достоверно выявляются участки обызвествления – кальцинаты.
2) Структура. Кистозные образования подразделяются на одно- и многокамерные; они могут иметь хорошо видимую стенку или не иметь таковой; содержать включения кальция, геморрагическую – гиперденсную – жидкость, гиподенсную жидкость, например, желчь. Внутри можно обнаружить инородное тело или паразита, кистозный или мягкотканный компонент. Также структура может быть однородная или неоднородная, последняя часто объясняется участками некроза. Выявление извести и кальцинатов свидетельствует о длительности процесса.
3) Форма может быть приближенной к шару, вытянутая, неправильная (иррегулярная) и т. д.
4) Контуры. Ровные или неровные, четкие или нечеткие, видимые на всем протяжении или на ограниченном участке.
5) Размеры. Измеряются линейные размеры очага (длинник и поперечник) на аксиальном срезе либо все три размера (когда это возможно, указывается также объем). Если планируется контрольное исследование через определенное время, выбирается т. н. «маркерный» очаг, изменение размеров которого будет оцениваться во времени.
6) Расположение необходимо указывать в описании КТ-исследования: локализуется ли патологический участок непосредственно в глубине органа, под капсулой, рядом с крупными сосудами, с желчными протоками, с желчным пузырем и т. д. Это может быть навести на мысли о его природе: например, билиарные кисты локализованы чаще всего вблизи желчных протоков, вблизи желчного пузыря.
7) Количество. Солитарный очаг в печени означает одиночный. Число патологических участков (например, метастазов при раке желудка или других органов системы пищеварения) может варьировать. Выявление одного метастаза уже позволяет выставить стадию M1 по системе TNM. Однако следует учитывать, что множественные очаговые образования в печени – это не всегда метастазы, и врач-рентгенолог обязан провести их дифференциальную диагностику, сопоставив многочисленные КТ-признаки.
8) Особенности накопления контраста. Чем меньше накопление контраста в очаге, тем меньше он кровоснабжается. Наоборот, чем быстрее накапливается контраст, тем более развита сосудистая сеть. Чем быстрее снижается плотность после окончания введения контраста, тем интенсивнее кровоток в очаге.
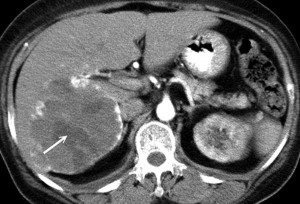
Так, гемангиома печени на КТ без контраста выглядит как гиподенсный участок, природу которого установить затруднительно. В артериальную фазу контрастирования наблюдается значительное увеличение плотностных характеристик гемангиомы (из-за накопления контрастированной крови в сосудистых лакунах), но затем ее плотность снижается и постепенно приходит к прежним значениям, что позволяет отличить гемангиому печени от рака, так как злокачественные новообразования, например, рак кишечника с метастазами в печень при КТ с контрастированием проявляется иначе: для метастазов наиболее характерно усиление плотности в виде «кольца» («ободка»), которое отображает активную (васкуляризованную) часть опухоли.
Гемангиома печени или рак? КТ брюшной полости с контрастным усилением: типичное накопление контраста в виде лакун помогает дифференцировать гемангиому от рака и установить правильный диагноз: кавернозная гемангиома.
Гиподенсные образования имеют плотность ниже нормальной паренхимы (в норме ее плотность составляет +50…+70 единиц Хаунсфилда – без контрастирования) и представляют собой следующие морфологические варианты:
1) Жировые образования имеют плотность от -100 до -10 единиц Хаунсфилда. Это может быть липома, фибролипома, ангиолипома, ангиофибролипома, аденома, липосаркома и некоторые другие опухоли из жировой ткани (а также участок с отрицательной плотностью может быть обусловлен локальным участком жировой инфильтрации, или жирового гепатоза).
2) Гиподенсный очаг плотностью 0…+20 единиц Хаунсфилда чаще всего содержит жидкость. Это может быть простая или паразитарная киста, билома – скопление желчи после операций на желчном пузыре и протоках, а также кистозные метастазы.
3) Гиподенсный очаг плотностью +20…+40 единиц Хаунсфилда бывает обусловлен как жидкостным содержимым, так и мягкотканным. Здесь гораздо больше вариантов, при составлении дифференциального ряда нужно учитывать размеры, форму, характер накопления контрастного вещества.
Капиллярная гемангиома правой доли печени: КТ с контрастным усилением в артериальную фазу выявляет гиперденсный участок.
Гиперденсные очаги имеют рентгеновскую плотнтость выше нормальной паренхимы (>70 единиц Хаунсфилда) и могут быть обусловлены кистами, содержащими плотную жидкость (с примесями белка или крови), либо их субстратом является опухоль или кальцинат.
1) Очаг плотностью +200…+400 единиц Хаунсфилда обусловлен наличием кальция в структуре. Это может быть обызвествленная киста, фиброма, фиброаденома (либо другая опухоль), обызвествленная гематома.
2) Локальный участок повышения плотности паренхимы зачастую бывает обусловлен отложениями металлов – солей алюминия, железа и т.д.
3) Опухоли бывают как гиперденсными, так и гиподенсными.
Кистозный характер при КТ имеют следующие образования:
1) Простая киста печени — что это? Простая киста возникает в результате эмбриогенеза и представляет собой ограниченное капуслой скопление жидкости. На КТ она имеют ровные края, четкие контуры, обычно правильную форму; плотностные характеристики жидкости +5…+20 единиц Хаунсфилда, не содержит каких-либо включений (кровь, кальций и т. д.), в их структуре нет перегородок, стенка ровная, без локальных утолщений. Контраст такие кисты не накапливают. Часто возникает вопрос, может ли киста печени перерасти в рак. Если киста имеет типичные КТ-характеристики, тревоги она вызывать не должна, озлокачествления кисты не бывает. Но важно отличить простую кисту от эхинококковой, от кистозной формы метастаза или кистозного рака.
2) Кистозные метастазы в печень при раке молочной железы, желудка, других органов обычно множественные, имеют неправильную форму, неоднородную структуру, размеры от 0,5 см до нескольких десятков см. Характеризуются накоплением контраста в виде «кольца». Обладают инфильтративным ростом. Подозрение на mts в печени возникает при КТ нередко, в таких случаях может помочь второе мнение по снимкам. В наше время множественные метастазы нередко успешно лечатся в крупных онкологических клиниках, где применяются различные методики (хирургическое удаление, химиоэмболизация, радиочастотная абляция и т.п.).
3) Кистозная форма гепатоцеллюлярного рака: форма неправильная, может выявляться солидный компонент (при кистозной форме он выражен минимально), опухоль единичная, оказывает объемное воздействие на рядом расположенные сосуды и желчные протоки.
4) Паразитарные кисты. Чаще всего эти кисты представлены эхинококком, реже – альвеококком. Бывают множественными или единичными, имеют хорошо видимую стенку, усиливающуюся при контрастировании. Бывают однокамерные и многокамерные паразитарные кисты. Внутри таких кист можно обнаружить паразита.
5) Гемангиома правой доли печени, либо левой доли. Гемангиома печени на КТ выглядит как типичный гиподенсный очаг, при контрастировании в артериальную фазу резко усиливается, в результате чего становятся видимыми сосудистые лакуны, а затем медленно теряет контраст. Атипичные гемангиомы на КТ имеют несколько другие характеристики, и отличить их от злокачественного поражения помогает взгляд опытного рентгенолога, имеющего опыт в диагностике заболеваний брюшной полости.
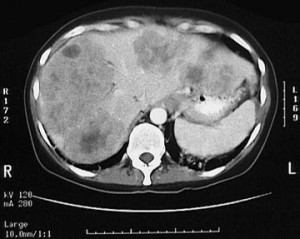
Вторичные (секундарные) изменения в печени на КТ. Рак кишечника с метастазами. Прогноз неблагоприятный, учитывая размеры и количество метастазов.
«Солидный» означает мягкотканный, состоящий из живой ткани. Какие бывают солидные образрования?
1) Объемное образование с включениями жира: липома, липофиброма, ангиолипома, липосаркома и др. Имеют характерную структуру и плотностные характеристики, соответствующие жировой ткани.
2) Фокальная нодулярная гиперплазия (ФНГ) имеет неправильную форму (в виде узла), при нативном исследовании – гиперденсный (незначительно выше нормальной плотности), при контрастировании неравномерно усиливается.
3) Регенераторный узел, локальный участок фиброза либо жировой инфильтрации – признак перерождения печеночной ткани под влиянием различного характера интоксикацией или травм, признак цирроза. Выглядит как локальный гипо- (жировая инфильтрация) или гиперденсный (фиброз) участок.
4) Гепатоцеллюлярный рак (ГЦР). Выглядит как объемное образование неправильной формы, различных размеров (иногда несколько десятков сантиметров в поперечнике), структура его неоднородна – при КТ могут быть выявлены участки некроза, полости (не усиливающиеся при контрастировании). Ткань опухоли за счет хорошего кровоснабжения повышает плотность при контрастировании.
Не все специалисты способны достоверно определить изменения в печени, выявленные при компьютерной томографии. Это во многом зависит от опыта рентгенолога, от качества выполнения исследования. К сожалению, при выполнении компьютерной томографии и других лучевых исследований (особенно в отдаленных периферийных клиниках) изменения иногда бывают пропущены, либо неверно истолкованы. Можно ли перепутать метастазы в печени? Увы, нередко обычные доброкачественные гемангиомы трактуются как метастазы, либо наоборот. В ряде случаев кистозные метастазы в печень трактуются как простые кисты, если к тому же не использовать контрастирование. В целом нужно отметить, что диагноз «mts печени» достаточно сложный в плане дифференцировки с другими множественными очаговыми изменениями.
Второе консультативное мнение врача, обладающего опытом в анализе КТ-исследований брюшной полости, всегда полезно – заключение по исследованию даст специалист, имеющий высшую врачебную категорию или научное звание, после подробного ознакомления с историей заболевания, с результатами лабораторных тестов и т. д. В результате точность диагностики становится выше, что позволяет определиться с дальнейшим направлением лечения (либо назначить дополнительные инструментальные и иные диагностические исследования).
Чтобы получить Второе мнение по результатам КТ или МРТ, можно обратиться в Национальную телерадиологическую сеть. Сделать это можно удаленно, не выходя из дома. Достаточно иметь результаты исследования на диске. В течение 24 часов с момента отправки снимков вы получите квалифицированный пересмотр КТ или МРТ с подробным описанием в виде заключения с подписью высококвалифицированного диагноста.
источник
Первичный рак печени по гистогенезу разделяют на гепатоцеллюлярный рак, исходящий из гепатоцитов, холангиоцеллюлярный рак или холангиокарцинома), исходящий из эпителия желчных протоков, и смешанный гепатохолангиоцеллюлярный рак. Основная доля поражений приходится на гепатоцеллюлярный рак, в то время как холангиоцеллюлярный рак считается относительно редким заболеванием и составляет около 10% всех злокачественных опухолей печени [Parkin et al., 1993].
Ультразвуковая картина при первичном раке печени весьма разнообразна. Обычно первичный рак печени характеризуется наличием объемных образований в печени, одиночных или множественных (узловая форма). Вместе с тем существует диффузная форма первичного рака печени, эхографическое изображение которой в ряде случаев напоминает цирротические изменения органа (надежные критерии дифференциальной диагностики этих заболеваний отсутствуют до настоящего времени).
Выделяют несколько типов ультразвукового изображения узловой формы первичного рака печени [Догра, Рубенс, 2005]:
1) гиперэхогенный, наиболее часто встречающийся;
Наиболее часто первичный рак печени локализуется в правой доле, в толще паренхимы. Поверхностное субкапсульное расположение встречается значительно реже. Размеры и форма первичного рака печени вариабельны. При выявлении достаточно крупных образований (более 4-5 см в диаметре) определяется увеличение размеров печени, сопровождающееся неровностью контуров в месте поражения. Отмечается аномальный ход сосудов и желчных протоков в проекции опухоли, ампутация крупных сосудистых стволов, а в ряде случаев сегментарное либо генерализованное расширение желчных протоков.
Прорастание первичного рака печени в магистральные сосуды органа в итоге приводит к нарушению печеночной гемодинамики: поражение системы воротной вены в 30-68% случаев заканчивается формированием опухоли или тромба в полости сосуда; вовлечение в неопластический процесс печеночных вен и реже нижней полой вены вызывает развитие синдрома Бадда—Киари. Злокачественные новообразования обильно кровоснабжаются. В цветовом, особенно энергетическом, допплеровском режиме может визуализироваться хаотический рисунок сосудистой сети опухоли [Митьков В.В. и др., 1999].
Ультразвуковые признаки узловой формы первичного рака печени отличаются вариабельностью и не являются патогномоничными в дифференциальной диагностике гепатоцеллюлярного рака с холангиоцеллюлярным раком.
Около половины очаговых образований при гепатоцеллюлярном раке (53%) имеют изоэхогенное изображение относительно печеночной паренхимы, при холангиоцеллюлярном раке этот признак наблюдается только у 30% больных. Гиперэхогенная картина опухоли выявлена у 40% больных с холангиокарциномами и только в 13% случаев при печеночноклеточном раке. Эхонегативные участки внутри объемных образований чаще наблюдают при гепатоцеллюлярном раке.
Нечеткость и неровность контуров более характерна для холангиоцеллюлярного рака. Вероятность диагноза холангиоцеллюлярного рака повышается, если наличие опухоли сопровождается внутрипеченочной сегментарной или генерализованной билиарной гипертензией.
Дифференциально-диагностическим признаком первичного рака печени относительно других солидных образований печени может быть эхонегативная окантовка изображений опухоли или отдельных узлов в ней (встречается одинаково часто при гепатоцеллюлярном и холангиоцеллюлярном раках: в 60-70% случаев).
Диффузная форма первичного рака печени при ультразвуковом исследовании может быть представлена 2 вариантами изображений: множественные узлы различного размера и эхогенности во всех отделах печени и крупноочаговая неоднородность печеночной паренхимы смешанной эхогенности, при которой отдельные узлы практически не дифференцируются.
В обоих вариантах печень обычно увеличена, часто с бугристыми контурами. Структура паренхимы неоднородна, по типу множественного очагового либо крупноочагового диффузного поражения. Наблюдаются выраженные нарушения сосудистого рисунка печени. При многоузловом варианте диффузной формы первичного рака печени отмечается деформация и сдавление венозных сосудов органа. Для крупноочагового диффузного поражения печени характерно обеднение сосудистого рисунка, включая крупные ветви воротной и печеночных вен, деформация и ампутация сосудов.
Изменения сосудистой архитектоники печени и хаотический рисунок сосудистой сети опухоли лучше выявляются в цветовом и особенно энергетическом допплеровском режимах. При диффузной форме первичного рака печени часто наблюдается быстрое развитие портальной и билиарной гипертензии, обусловленных выраженными нарушениями структуры печени и ее анатомических образований.
При ультразвуковом исследовании возникают сложности в дифференциальной диагностике злокачественных и доброкачественных опухолей, первичного и вторичного рака, а также злокачественных опухолей и других очаговых поражений печени (абсцесс, альвеококк).
Метастазы — наиболее часто встречаемые злокачественные опухоли печени. Могут быть одиночными и множественными (в 90% случаев). При метастатическом поражении наблюдается деформация контуров, локальное или генерализованное увеличение, очаговая неоднородность структуры печени. Одиночные метастазы приводят к локальному сдавлению и смещению сосудистого рисунка печени. Массивное очаговое поражение вызывает выраженное изменение ангиоархитектоники органа с обеднением сосудистого рисунка. Ультразвуковая картина вторичных опухолей весьма разнообразна и может быть представлена несколькими вариантами.
• Гиперэхогенный (образования с четкими контурами, повышенной эхогенности, чаще неоднородные).
Дифференциальная диагностика с гемангиомами печени, очаговой жировой инфильтрацией и очаговым фиброзом печени, первичным раком печени. Осложненными формами этого варианта эхоскопической картины вторичных опухолей, по мнению В. Догра и Д.Дж. Рубенса (2005), являются метастазы типа «бычий глаз» (гипоэхогенный центр и гиперэхогенная периферия) и «мишень» (гиперэхогенная центральная часть и гипоэхогенная периферия). В ряде публикаций эта разновидность вторичных опухолей выделяется в отдельный вариант ультразвуковой картины [Митьков В.В., Брюховецкий Ю.А, 1996). Дифференциальная диагностика практически со всеми известными очаговыми поражениями печени.
• Изоэхогенный (образования по структуре и эхогенности практически неотличимы от печеночной паренхимы). Дифференциальная диагностика с очаговой узловой гиперплазией печени, ПРП.
Имеют ряд черт, присущих опухолям: отсутствие капсулы, неоднородная внутренняя структура при полипозиционном исследовании с применением соответствующей частоты датчика в режиме двойной гармоники, отсутствие эффекта дистального псевдоусиления тканей, увеличение размеров и количества образований при динамическом исследовании в относительно короткие промежутки времени.
Дифференциальная диагностика с простыми, нагноившимися и малигнизированными кистами, некротизированным первичным раком печени, абсцессами печени, кавернозными гемангиомами, эхинококкозом.
• Смешанной эхогенности или диффузный (образования с неоднородной внутренней структурой, часто плохо дифференцируемые на фоне паренхимы печени, особенно при наличии диффузных изменений органа).
Такие осложнения описторхоза, как кисты, абсцессы и холангиогенные опухоли печени требуют динамического наблюдения либо оперативного лечения.
Существование описторхозных кист, как самостоятельного поражения печени, доказано патоморфологическими исследованиями. Описторхозные кисты развиваются у лиц с массивной и супермассивной степенью инвазии в результате длительной желчной гипертензии. Они представляют собой резко расширенные желчные ходы с сохраненной или частично разрушенной стенкой, окруженной фиброзной тканью. Содержат желчь, слизь, экссудат, яйца описторхов или самих паразитов.
Описторхозные кисты вариабельны по форме, как правило, небольших или средних размеров, чаще множественные. Обычно они расположены в периферических отделах печени, субкапсульно или по ходу портальных трактов с преимущественной локализацией в левой доле, что связано с худшими условиями желчеоттока.
Ультразвуковая картина описторхозных печеночных кист соответствует признакам простых кист: в 95,5% наблюдений это жидкостные образования с однородным анэхогенным содержимым, тонкостенные, с неровными, чаще фестончатыми контурами. В 4,1% случаев в просвете кист отмечались хлопьевидные включения, а в 2,7% наблюдений — единичные внутренние перегородки [Толкаева М.В., 1999].
В дифференциальной диагностике помогают дополнительные ультразвуковые признаки описторхозного поражения, наблюдаемые у 83% пациентов с кистами печени: повышение эхогенности стенок внутрипеченочных желчных протоков и перипортальных тканей, наличие холангиоэктазов в периферических отделах печени, увеличение желчного пузыря с внутриполостными осадочными и хлопьевидными включениями.
Описторхозные абсцессы печени относятся к редким, но наиболее тяжелым по течению и трудным для диагностики осложнениям описторхоза.
По данным Н.А. Бражниковой (1989), в общей структуре хирургических осложнений описторхоза абсцессы составляют 2,56%.
Описторхозные абсцессы обычно развиваются на фоне гнойного холангита, но в ряде случаев возникают как следствие нагноения кист печени или тромбоза сосудов портальной системы.
Существует два типа ультразвукового изображения гнойников при описторхозе [Толкаева М.В., 1999].
• Абсцессы I типа. Располагаются в задних сегментах правой доли печени (S6-S7) и являются следствием локального нарушения дренирования сегмента или субсегмента органа. Представляют собой крупные неоднородные фрагменты печеночной паренхимы повышенной эхогенности без четких границ, от 6,5 до 9,0 см в диаметре, соответствующие зоне воспалительной инфильтрации. Участки деструкции внутри инфильтрата определяются в виде небольших очагов пониженной плотности или жидкостных включений неправильной, иногда древовидной формы с размытыми контурами.
Описторхозные абсцессы I типа при адекватной консервативной терапии не нуждаются в оперативном лечении. Дифференциальная диагностика с пиогенными абсцессами может вызывать затруднения.
• Абсцессы II типа. Имеют холангиогенное происхождение, развиваются на почве холангиоэктазов вследствие желчной гипертензии и гнойного холангита. Представляют собой множественные локально расширенные внутрипеченочные желчные протоки с утолщенными и уплотненными стенками на фоне общего повышения эхогенности ткани печени вследствие ее воспалительной инфильтрации. В просвете холангиоэктазов определяется слабоэхогенное содержимое, обусловленное гноем и детритом.
Для абсцессов II типа характерна множественная локализация в обеих долях печени, небольшие размеры, быстрое развитие печеночной недостаточности. Холангиогенные абсцессы требуют экстренного хирургического вмешательства. Отсутствие своевременного лечения (причиной чего может быть трудность диагностики) приводит к перфорации абсцессов с развитием гнойного перитонита, поддиафрагмальных и подпеченочных абсцессов, забрюшинных флегмон. Описторхозные абсцессы II типа эхоскопически не имеют существенных отличий от холангитических абсцессов непаразитарной этиологии.
Наиболее серьезное осложнение длительно существующего описторхоза — первичный рак печени. В регионах, эндемичных по описторхозу, частота первичного рака печени в 3—9 раз выше, чем на остальных территориях [Шайн А.А., 1972]. Преобладающей формой первичного рака печени при описторхозе является холангиоцеллюлярный рак. Развитие холангиоцеллюлярного рака — многофакторный процесс, при котором паразиты играют роль стимуляторов злокачественного роста.
В зависимости от уровня поражения желчных протоков у больных описторхозом, существует 3 типа эхоскопической картины холангиоцеллюлярного рака печени [Толкаева М.В., 1999].
• Опухоли внутрипеченочной локализации. Развиваются из мелких внутрипеченочных желчных протоков и характеризуются диффузно-инфильтративными изменениями паренхимы периферических отделов печени. Визуализируются в виде фрагментов гиперэхогенной ткани сглаженной структуры, без четких границ, с внутренними мелкими очагами пониженной или повышенной плотности и кальцинатами.
Часто сопровождаются мелкими холангиоэктазами в периферических отделах печени в зоне поражения. Дополнительный признак описторхозной инвазии — выраженные перидуктальные фиброзноинфильтративные изменения тканей, местами с элементами обызвествления. Опухоли внутрипеченочной локализации при описторхозе наиболее трудны для ультразвуковой диагностики в связи с диффузно-инфильтративным характером роста и невозможностью определения истинных границ поражения.
• Опухоли с поражением ворот печени (центральная локализация). Характеризуются наличием в области портальных ворот печени объемного образования небольших размеров (до 3—5 см), без четких контуров, гипер-, изо- или гипоэхогенного относительно печеночной паренхимы. Сопровождаются обструкцией желчных протоков в зоне поражения и расширением проксимальной части внутрипеченочных желчных протоков.
• Опухоли с поражением дистальных желчных протоков. Для холангиоцеллюлярного рака характерно длительное бессимптомное течение заболевания. Сложности визуализации опухолей при ультразвуковом исследовании определяют позднюю диагностику. К моменту постановки диагноза у 85,7% больных имеется метастатическое поражение печени и лимфатических узлов.
Ультразвуковое исследование благодаря своей неинвазивности, информативности и точности получаемой информации является ценнейшим диагностическим методом, дающим возможности в большинстве случаев верифицировать диагноз очагового поражения печени до такой степени достоверности, что использование других диагностических методов становится необязательным. Сочетание ультразвукового метода исследования с допплерографией позволяет выяснить взаимоотношения патологического очага с сосудисто-протоковыми структурами печени и достаточно точно планировать объем и характер предстоящего оперативного вмешательства.
источник
Хирурги не только XIX в., но и первой половины XX в. считали прижизненный диагноз гемангиомы печени невозможным. К 1957 г. правильный пооперационный диагноз гемангиомы печени был поставлен всего у 8 больных. По сведениям клиники Мэйо, из 11 оперированных больных у 3 опухоли до операции по клиническим симптомам были правильно отнесены к печени, у 2 отнесены к печени предположительно, остальные оперированы с ошибочным диагнозом.
Среди 25 оперированных B.C. Шапкиным больных диагноз «гемангиома печени» был поставлен у 7, опухоль печени — у 8, опухоль предположительно отнесена к печени — у 2, оперированы с неверным диагнозом 2 и у 5 больных гемангиома печени была найдена случайно. Действительно, если опухоль не пальпируется, то на основании только клинических данных диагноз весьма проблематичен.
В то же время специальные методы исследования устраняют трудности и способствуют установлению правильного диагноза. Среди больных Томского гепатологического центра при гемангиомах правильный диагноз был поставлен у всех больных.
В случае наличия пальпируемой опухоли обращает на себя внимание медленный рост новообразования, жалобы на боли и тяжесть в правом подреберье, сопровождающиеся диспептическими явлениями, гепатомегалия с очаговым увеличением печени. Опухоль обычно гладкая, овальной или круглой формы, мягкоэластической консистенции. Иногда удается отметить изменение формы опухоли при сдавлении ее.
У наших больных даже при больших опухолях не удавалось про слушать над ними сосудистые шумы. В случае осложнений гемангиом клиническая картина существенно изменяется. Если учесть, что у 41 из пациентов Томского гепатологического центра опухоль была размерами более 10 см, то можно полагать, что клиническая диагностика гемангиом печени при достаточных размерах опухоли возможна.
При злокачественном перерождении отмечается быстрый рост опухоли, выраженный болевой синдром с прогрессирующим похуданием больного. В ряде случаев у больных отмечается субфебрилитет и, наконец, наличие жидкости в животе.
Разрыв гемангиом характеризуется симптомами острого живота с внутрибрюшным кровотечением. Иногда при этом удается определить наличие жидкости в брюшной полости.
Клинический диагноз гемангиомы печени строится на основании следующих признаков:
— медленная эволюция, при этом речь идет о женщинах 30-40 лет; поражение мало отражается на общем состоянии организма;
— асимметричная увеличенная печень (опухоль на одной доле или изолированно увеличенная доля);
— опухоль переменного объема при различных обследованиях, болезненная или слабо болезненная, плотноватой консистенции;
— выслушивание систолического шума над опухолью — единственного патогномичного признака гемангиомы. К сожалению, признак встречается редко.
Дополнительные методы исследования верифицируют диагноз.
Результаты лабораторных исследований дают мало данных для диагноза гемангиомы печени. В случае очень больших размеров опухоли бывает анемия (гемоглобин от 101 до ПО г/л). По данным института хирургии РАМН, анемия отмечена у 5,75% больных с гемангиомами. При биохимических исследованиях не зарегистрировано существенных изменений, за исключением гипопротеинемии (4,67%) и снижения протромбитового индекса (3,45%).
По данным Томского гепатологического центра, при гемангиомах найдены гипералатемия (26%) и гиперасатемия (23%), гиперпротеинемия — в 20% случаев. Снижение фибриногена отмечено в 20%, а снижение количества эритроцитов — в 15% случаев. Гемоглобин был понижен у 16,6% больных. Наиболее часто наблюдалось увеличение скорости оседания эритроцитов — 51,6% и снижение протромбинового индекса до 33,3%. Все эти изменения не характерны для гемангиом, но их следует учитывать при подготовке больных к операции.
В последние годы в целях диагностики очаговых заболеваний печени, в том числе гемангиом, широко применяется лапароскопия. При использовании этого метода надо учитывать, что пункционную биопсию под контролем лапароскопа в диагностике применять не следует из-за возможности тяжелого кровотечения. Истинные размеры опухоли в толще печени при лапароскопии выявить не удается. Метод не позволяет судить об операбельности процесса.
В клинике он достаточно широко использовался в диагностике. При этом B.C. Шапкин считал, что внешний вид гемангиом настолько характерен, что после лапароскопии возможен окончательный диагноз. Мы согласны с этим при условии, что опухоль выходит на поверхность печени и находится в доступных осмотру зонах. При лапароскопии гемангиома печени выглядит как сине-багровая бугристая мягкая опухоль, вьгходящая на поверхность органа.

Лапароскопия. Гемангиома печени
При гемангиомах в случае использования обычной рентгенографии для диагноза дает скудные данные. На обзорной рентгенограмме в некоторых случаях удается выявить тень опухоли на контуре печени, высокое стояние купола диафрагмы или участки кальцификапии в опухоли. Значительно нагляднее эти изменения видны на рентгенограммах, сделанных на фоне пневмоперитонеума. Из всех этих признаков нам кажется наиболее перспективным выявление очажков кальцификации в зоне опухоли.

Гемангиома печени. Рентгенограмма. Обызвествление опухоли
Для диагностики гемангиом ангиография применялась в институте хирургии РАМН им. А.В. Вишневского и в Томском гепатологическом центре. На ангиограммах основным признаком гемангиом было накопление контраста в опухоли, дающее «снежноподобную» или «гроздевидную» картину у 97,44% больных.
Гемангиома печени. Ангиограмма. Гроздевидные сосуды
Ангиографическая картина при гемангиомах имеет следующие особенности:
— патологические сосуды в месте локализации опухоли;
— усиленное накопление контрастного вещества в артериальную, венозную и паренхиматозную фазы;
— сброс контраста через довольно крупный венозный ствол;
— значительное увеличение кровотока по сосудам, питающим опухоль;
— деформация и смещение внутрипеченочных артерий, расположенных вблизи от патологического очага.

Гемангиома печени. Ангиограмма. Патологические сосуды в тени опухоли

Гемангиома печени. Ангиограмма. Усиленное накопление контрастного вещества в тени опухоли

Гемангиома печени. Ангиограмма. Деформация и смещение артерий вблизи от патологического очага
Селективная ангиография имеет разрешающую способность не ниже 2,5 см. Чувствительность метода приближается к 100%.
На основании данных литературы и собственных исследований можно заключить, что ангиография дает много данных для диагностики гемангиом печени. Венозная ангиография в клинике не применялась, поскольку при этом заболевании другие методы исследования позволяют получить исчерпывающую информацию.
УЗИ весьма ценно и информативно для диагностики гемангиом печени. Поданным В.Л. Ганноты (1991), эффективность его составляет 100%, то есть у всех больных патологическое образование в печени было обнаружено. Чувствительностъ метода, то есть топический диагноз, составила 94% и зависела от размеров опухоли. При размерах опухоли до 3 см она была 87,5%, а при размерах ее от 3 см и выше достигала 100%. Специфичность исследования (морфологический диагноз) определялась наличием четких контуров — 88,4%, округлостью формы — 88,46%, эхопозитивным изображением опухоли — 92,86% и наличием эхонегативной окантовки — 5,7%.
Эхосемиотика гемангиом печени достаточно вариабельна, она часто зависит от размеров опухоли. При небольших опухолях до 3 см их акустическая идентификация достаточно проста. На эхограмме определяется обычно правильной формы округлое образование повышенной эхогенности с ровными четкими контурами.

УЗИ. Гемангиома печени. Неопределенные структуры в центре образования
По мере увеличения размеров опухоли эхографическая диагностика становится более сложной из-за того, что акустическая картина теряет специфичность и достаточно трудноотличима от злокачественных опухолей. Примерно у половины больных контуры опухоли были неровными и нечеткими. В толще образования выявляется неопределенность структуры.

УЗИ. Гемангиома печени. Отсутствие эхонегативного ободка
В гемангиомах с усиленной структурой определяются эхонегативные зоны различной формы и размеров, что служит ультразвуковым изображением сосудистых каверн.

УЗИ. Гемангиома печени. Эхонегативные зоны — сосудистые каверны
Наиболее типичной картиной для гемангиом большого размера можно считать наличие образования повышенной эхогенности с четкими ровными контурами, внутри которого определяются округлые гипоэхогенные зоны. При множественных гемангиомах приходится дифференцировать их от метастатических опухолей печени. Для гемангиом характерны ровность контура, отсутствие эхонегативного ободка по периметру новообразования и наличие питающего сосуда.
В.Л. Ганнота (1991) считает, что общая эффективность метода достигает 72,4%, а чувствительность не зависит от морфологической структуры опухоли. Она определяется ее размерами и локализацией. Во время γ-сцинтиграфии в зоне распространения опухоли определяется дефект накопления изотопа. Метод позволяет распознавать опухоли более 2 см в диаметре, но не дает возможности выяснить характер новообразования. При этом опухоли любого генеза дают аналогичную картину дефекта накопления изотопа в зоне поражения органа. В диагностике гемангиом печени метод недостаточно специфичен, поскольку выявляет лишь наличие в печени патологического очага.
Современный метод исследования. В нашей клинике применяется более 20 лет. По данным литературы и материалам автора, метод позволяет в 100% установить наличие в печени опухоли и выяснить ее распространенность. Применение дополнительного внутривенного контрастирования позволяет в ряде случаев добиться усиления плотности исследуемого объекта.
На характер изменений влияет размер опухоли. Мелкие гемангиомы (от 1 до 5 см) характеризуются круглой формой, четкими и обычно ровными контурами и однородной структурой паренхимы. Плотность их колеблется от 24 до 54 ед. Н (единиц Хоунефильда) при плотности паренхимы в норме 50-70 ед. Н. При гемангиомах 6-8 см в диаметре контур их также четкий, но более бугристый, чем у мелких гемангиом.
В паренхиме таких гемангиом на срезе появляются мелкие участки в виде отдельных точек диаметром 1-3 мм или полости 1-3 см плотностью 25—35 ед. Н. При размерах гемангиом свыше 8 см на срезах выявляется характерный только для гемангиом симптом «гиалиновой щели», проявляющийся в центре опухоли, как участок равномерной низкой плотности (15-30 ед. Н) звездчатой или продолговатой формы с четкими контурами.

Гемангиома печени. Компьютерная томограмма
Опухоли печени визуализируются как низкоплотные очаги с плотностью в среднем +40,92 ед. Н. Метод также перспективен для диагностики гемангиом печени в связи с неинвазивностью, эффективностью, равной 100%, и чувствительностью при опухолях, равной 93,75% [Ганнота В.Л., 1991].
В целом можно заключить, что диагностика гемангиом печени при жизни возможна и базируется на данных клинического исследования и материалах специальных исследований, из которых главными являются лапароскопия, ультразвуковое исследование, ангиография артериальной системы печени и компьютерная томография.
Клиническая диагностика аденом печени достаточно проста при наличии пальпируемой опухоли. Она плотна на ощупь, имеет округлую форму и слегка болезненна при пальпации.
Лабораторная диагностика аденом печени не помогает поставить диагноз, так как показатели крови почти не изменяются. Только при больших опухолях наблюдаются признаки анемии и неспецифические изменения свертывающей системы крови.
Пункционная биопсия дает некоторые данные для диагностики, но к ее результатам следует относиться с осторожностью. Б.И. Альперович сообщил о больном, у которого при пункционной биопсии был выставлен диагноз рака печени, а исследование резецированного препарата дало диагноз аденомы.
На рентгенограммах, как правило, выявляются опухоли, имеющие большие размеры. Кроме локального увеличения печени, имеющего округлую форму, довольно часто в тени печени удается выявить
круглую тень, по интенсивности отличающуюся от окружающих тканей.

Рентгенограмма. Аденома печени. Тень опухоли на рентгенограмме
В отличие от эхинококковой кисты, по периферии тени ни разу не было отмечено обызвествления.
Ангиографическая картина аденом печени достаточно характерна. В зоне опухоли имеется отличный от нормальной паренхимы печени уровень васкуляризации. При этом характерна гиповаскуляризация, в отличие от гемангиом печени. Имеют место деформация и смещение внутрипеченочных артерий по периферии зоны извращенной васкуляризации с ампутацией мелких ветвей в зоне опухоли.
Крупные магистральные стволы огибают опухоль в виде руки, держащей мяч. В отличие от гемангиом печени, в зоне опухоли не наблюдается гиперваскуляризации, отсутствуют сосудистые «озера». У ряда больных удается наблюдать на ангиограммах капсулу опухоли.

Аденома печени. Ангиография. Видна капсула опухоли
Чувствительность метода достигает 100%. Венозная ангиография печени для диагностики аденом печени нами не применялась.
При аденомах эффективность и чувствительность метода ультразвуковой диагностики составили 100%. У всех исследованных больных поставлен диагноз новообразования печени и точно установлена топография патологического процесса. Что касается специфичности метода, то у всех больных установлено наличие объемного образования в печени округлой формы и различного размера от 3 до 30 см. Контур образования четкий, но не обозначен, как при эхинококкозе или кисте.
У ряда больных выявлена капсула опухоли, что служит дифференциально-диагностическим признаком, отличающим аденомы от злокачественных опухолей. Особенно ценным при ультразвуковой диагностике аденом является возможность дооперационной визуализации крупных сосудистых стволов печени и выяснение взаимоотношений опухолей с ними (элементы ворот и их ветви, ствол нижней полой вены) без применения ангиографического исследования и компьютерной томографии.
При аденомах метод позволяет выявить в печени очаг, который не накапливает радиоактивный препарат. Этот дефект накопления изотопа помогает установить наличие в печени новообразования, но не позволяет выяснить его топографию и характер. В.Л. Ганнота считает, что эффективность метода при аденомах — 72,4%. Метод значительно уступает по точности ультразвуковому исследованию.
КТ позволяет установить наличие опухоли в печени, ее размеры и топографию. По данным В.Л. Ганноты (1991), эффективность метода 100%, а чувствительность — 93,75%.

Аденома печени. Компьютерная томограмма
• Клиническое обследование (наличие пальпируемой опухоли, изменяющей свои размеры при пальпации).
• Лабораторное исследование (малоэффективно).
• Ультразвуковое исследование.
• Компьютерная томография.
• Артериальная ангиография.
• Лапароскопия.
• При необходимости пункционная биопсия (осторожно!).
Доброкачественные опухоли печени необходимо дифференцировать со злокачественными опухолями и альвеококкозом. При злокачественных опухолях наблюдают быстрый рост опухоли, характерную ультразвуковую картину и прогрессирующую кахексию. При альвеококкозе характерен медленный рост, каменистая плотность паразитарного узла, положительные иммунологические реакции. Окончательный диагноз достоверен только после морфологического исследования биопсированного материала.
источник