В данной статье речь пойдёт о трансплантации печени: правовые аспекты трансплантации печени в РФ, показания к операции, подготовка к оперативному лечению, виды доноров, оперативное вмешательство у пациентов, особенности ведения реципиентов после операции.
Каждому человеку нужна здоровая печень для осуществления нормальной жизнедеятельности. Печень выполняет ряд жизненно важных функций в организме: она обеспечивает синтез глюкозы, белков, жиров, витаминов, выработку желчных кислот и холестирина, она отвечает за образования ряда факторов свёртывающей и противосвёртывающей систем организма. Также печень служит своего рода “фильтром” – она обеспечивает обезвреживание различных чужеродных веществ, в том числе аллергенов и токсинов. Если хотя бы одна из этих функций будет серьёзно нарушена, это может стать жизнеугрожающей ситуацией для организма.
- Желтуха – пожелтение кожи, и видимых слизистых оболочек;
- Потемнение мочи (цвет тёмного чая или тёмного пива);
- Обесцвечивание кала;
- Желудочно-кишечные кровотечения (рвота кровью, рвота чёрными массами, чёрный стул или кровь в стуле);
- Зуд;
- Асцит – скопление жидкости в животе;
- Склонность к кровоточивости слизистых носа, дёсен и т.д.;
- Энцефалопатия – нарушения памяти, забывчивость, спутанность сознания и подобные неврологические нарушения.
Помимо всего прочего, печеночная недостаточность даёт осложнения на другие органы и системы, что в итоге может привести к нарушению работы почек, лёгких, что в комплексе очень сильно ухудшает тяжесть состояния пациентов и требует дополнительного более сложного лечения.
При развитии печеночной недостаточности в исходе различных заболеваний, часто единственным методом лечения становится трансплантация печени.
Трансплантация печени является наиболее эффективным и, часто, единственным радикальным методом лечения больных с терминальной стадией хронических диффузных болезней печени (цирроз, фиброз и пр.), фульминантной печеночной недостаточностью, злокачественными и доброкачественными опухолями печени.
В трансплантации печени нуждаются пациенты со следующими заболеваниями:
- Цирроз печени в исходе вирусных гепатитов B, C и D;
- Аутоиммунный гепатит;
- Токсический гепатит;
- Криптогенный цирроз печени (цирроз печени неуточнённой этиологии);
- Билиарный цирроз печени;
- Первичный склерозирующий холангит (ПСХ);
- Болезнь Кароли;
- Алкогольный цирроз печени (цирроз Лаэннека) – при условии 6-месячной алкогольной ремиссии;
- Острая печеночная недостаточность;
- Опухоли печени;
- Нейроэндокринные опухоли;
- Гепатоцеллюлярная карцинома (ГЦК);
- Гемангиоэндотелиома;
- Метастазы гастроинтестинальной стромальной опухоли (при условии медленного роста);
- Цирроз печени в исходе дефицита альфа-1-антитрипсина;
- Муковисцидоз; (статья по теме – трансплантация печени при муковисцидозе);
- Семейная гиперхолестеринемия;
- Гемохроматоз;
- Болезнь Вильсона-Коновалова;
- Болезни накопления гликогена
- Синдром Бадда-Киари;
- Синдром Клиглера-Найяра;
- Поликистоз печени;
- Синдром Алажиля;
- Амилоидоз;
- Саркоидоз;
- Обширная травма печени, ведущая к печеночной недостаточности.
После того как были исчерпаны возможности консервативного лечения и установлена необходимость трансплантации печени требуется ответить на 3 основных вопроса:
- Сможет ли пациент перенести операцию и ранний послеоперационный период;
- Будет ли пациент привержен к терапии и режиму необходимому для выживания после трансплантации печени;
- Есть ли у пациента сопутствующие заболевания, которые могут скомпрометировать его выживание или функцию трансплантата.
- СПИД;
- внепечёночное распространение злокачественных опухолей;
- активная внепеченочная инфекция (туберкулез и другие);
- активный алкоголизм и наркомания;
- психические заболевания, исключающие регулярный прием иммунодепрессантов;
- высокий кардиологический или анестезиологический риск;
- распространенный тромбоз воротной вены (статья по теме – трансплантация печени у пациентов с тромбозом воротной вены);
- ранее перенесенные вмешательства на печени;
- возраст более 60 лет;
- индекс массы тела (ИМТ) более 35 кг/м2.
В качестве потенциальных доноров рассматриваются как посмертные доноры, так и живые родственные доноры.
Печень для трансплантации изымается только у посмертных доноров, перенесших смерть головного мозга (с сохранённым кровообращением и поддерживаемым аппаратным дыханием). Обстоятельства смерти и личности умерших доноров остаются конфиденциальными. Изъятие органов и (или) тканей не допускается, если установлено, что они принадлежат лицу, страдающему болезнью, представляющей опасность для жизни и здоровья реципиента. Подробнее здесь и здесь. Выполняют ортотопическую трансплантацию печени (целого органа), так и SPLIT-трансплантацию (донорская печени разделяется на две части и каждая часть пересаживается отдельному реципиенту).
В Российской Федерации, как и во многих других странах, в целях трансплантации печени широко распространено использование фрагментов печени взрослых доноров. Этот вид трансплантологической помощи обладает рядом преимуществ – хорошее качество трансплантата, возможность проведения операции в необходимые сроки, и как правило, тканевая совместимость с донором. Такой вид трансплантации в нашей стране наиболее часто выполняют детям (трансплантация левого латерального сектора печени, трансплантация правой или левой доли печени).
По законам Российской Федерации, трансплантация печени (как и почки) от живого донора может быть произведена только в том случае, если потенциальный донор является биологическим родственником реципиента. Это могут быть ближайшие родственники – мать или отец, а так же более отдалённые – тётки, дяди, сёстры и братья. Стоит отметить, что супруги не являются кровными родственниками. Также, если реципиент является усыновлённым ребенком, его усыновители не могут быть донорами для него, в отличие от его биологических родителей. К донорству нельзя принуждать. Изъятие органов и (или) тканей не допускается, если установлено, что они принадлежат лицу, страдающему болезнью, представляющей опасность для жизни и здоровья реципиента. Изъятие органов и (или) тканей для трансплантации у лиц, находящихся в служебной или иной зависимости от реципиента, не допускается. Подробнее здесь и здесь.
В качестве живого родственного донора обследуется кровный родственник реципиента старше 18 лет. В первоначальной беседе врач выявляет первичные противопоказания к донорству – проводит сбор анамнеза (выясняет у пациента подробно о перенесенных заболеваниях, наличии аллергических реакций, проводит измерение роста и веса, проводит психоэмоциональную оценку потенциального донора).
Далее проводится комплекс лабораторно-диагностического обследования, который включает в себя:
- Определение группы крови и резус-фактора;
- Клинический анализ крови с подсчётом лейкоцитарной формулы;
- Общий анализ мочи;
- Биохимический анализ крови;
- КЩС и электролитный статус;
- HLA-типирование и перекрестная лимфоцитотоксическая проба;
- Обзорная рентгенография органов грудной клетки;
- Электрокардиография;
- УЗИ сердца (ЭХО-КГ);
- Эзофагогастродуоденоскопия;
- Исследование функции внешнего дыхания (по показаниям);
- Ультразвуковая допплерография нижних конечностей.
Также, особенно важным аспектом обследования родственного донора является дооперационная оценка печени. Для этого выполняются УЗИ органов брюшной полости, мультиспиральная компьютерная томография органов брюшной полости с внутривенным болюсным контрастированием. При индексе массы тела потенциального донора печени боле 25,0 баллов, выполняется пункционная биопсия печени.
Собственно оперативное вмешательства начинается с двухстороннего субкостального разреза, дополненного срединным разрезом до мечевидного отростка. При выполнении доступа требуется соблюдение тщательного гемостаза, ввиду наличия обширной развитой сети подкожных вен. Хирургическое вмешательство у реципиента включает в себя следующие этапы:
- Гепатэктомия;
- Наложение сосудистых анастомозов (в следующей последовательности – кавальная, портальная, артериальная реконструкция);
- Гемостаз и формирование желчеотводящего анастомоза.
Удаление пораженной печени в большинстве случаев представляет собой наиболее трудоемкий этап. В случае опухолевых поражений печени это связано с выраженной гепатомегалией. В случаях же цирроза, несмотря на значительное уменьшение размеров печени, гепатэктомия усложняется наличием венозных коллатералей в связках печени и ее воротах, наличием спаек, а также изменением обычных топографо-анатомических отношений в верхнем отделе брюшной полости и, нарушениями свертывающей системы крови.
Рассечение связочного аппарата начинают с круглой и серповидной связок. Затем пересекаются левая треугольная и левая венечная связки. Следующей составляющей этапа гепатэктомии является диссекция печеночно- двенадцатиперстной связки, при этом выделение воротной вены и печеночной артерии предусматривает полное освобождение от околососудистой ткани, тогда как при выделении желчного протока скелетирование последнего нежелательно.
Доступ к элементам печеночно-двеннадцатиперстной связки может быть крайне сложен. Изоляции элементов могут мешать увеличенные лимфатические узлы, содержащие множественные венозные и лимфатические коллатерали, спайки после перенесенных оперативных вмешательств. Общий желчный проток с окружающей клетчаткой пересекается. Собственная печеночная артерия выделяется до паренхимы. Она или ее долевые ветви должны быть лигированы как можно дистальнее. Проксимально артерия мобилизуется до желудочно- двеннадцатиперстной с выделением последней и взятием на держалку. Воротная вена склелетируется с подведением турникета.
После мобилизации элементов печеночно-двеннадцатиперстной связки рассекают правую венечную связку и мобилизуют правую долю печени. Данная манипуляция в условиях выраженного фиброза, развития венозных коллатералей, в особенности при уменьшении размеров печени представляет значительные трудности и нередко осложняется диффузным кровотечением из паренхимы печени. После описанных манипуляций становится доступной позадипеченочный отдел НПВ.
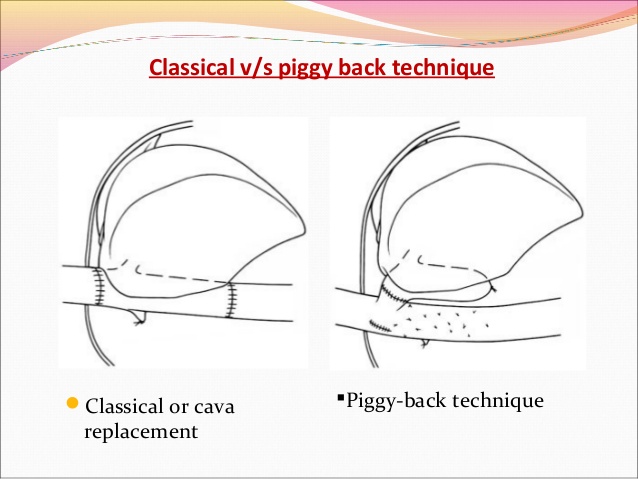
Дальнейшие действия зависят от избранной техники имплантации печени «классической» или Piggyback.
Техника классической трансплантации печени и техника Piggy-back.
Позадипеченочный отдел нижней полой вены мобилизуется на всем протяжении ретрокавального пространства: от почечный вен до диафрагмы. Ключевым моментом является выделение и пересечение правой надпочечниковой вены, впадающей непосредственно в нижнюю полую вену. После подготовки нижней полой вены пережимается воротная и полая вены (проксимально и дистально), выполняется гепатэктомия. Формируются анастомозы нижней полой вены донорской печени и реципиента проксимально и дистально и анастомоз воротной вены. Для поддержания гемодинамики традиционно использовалось обходное вено-венозное шунтирование. Для этого до гепатэктомии канюлируется воротная вена, предварительно подготовленные левая бедренная и подмышечная вены. Кровь от нижней половины тела и органов брюшной полости с помощью насоса направляется в верхнюю полую вену. Обходное вено-венозное шунтирование может применяться на начальных этапах освоения трансплантации печени.
Данный вариант подразумевает сохранение кровотока по нижней полой вене, отделение печени от позадипеченочного отдела НПВ. Пересечение связки НПВ по является ключевым моментом мобилизации позадипеченочного отдела НПВ, особенно в той ситуации, когда гипертрофированная хвостатая доля (I сегмент) окружает НПВ. Все мелкие печеночные вены, дренирующие хвостатую долю, и добавочные правые печеночные вены раздельно лигируются и пересекаются по направлению снизу вверх до уровня основных печеночных вен Таким образом, нижняя полая вена реципиента сохраняется на всем протяжении. Производится пережатие печеночных вен и воротной вены. Выполняется гепатэктомия без пережатия нижней полой вены. Устья печеночных вен объединяются, формируется анастомоз с надпеченочным отделом НПВ донорской печени. Подпеченочный отдел НПВ трансплантата ушивается. В некоторых случаях правая печеночная вена расположена каудально, что делает невозможным вовлечение ее в шов. В этом случае последнюю обходят циркулярно и пересекают между двумя зажимами, затем ушивают стороны НПВ непрерывным швом нитью / . В то же время пересечение правой печеночной вены позволяет отвести печень влево и провести безопасную изоляцию средней и левой печеночных вен.
Вариантом методики Piggyback, предложенным Belghiti является формирование анастомоза по типу «бок в бок» между ретропеченочным отделом НПВ реципиента и трансплантата. Производят предварительную подготовку НПВ трансплантата: ушиваются проксимальный и дистальный отдел полой вены донорской печени. После продольного частично пережатия полой вены реципиента максимально широко рассекается ее передняя стенка. Соответственно этому рассекается задняя стенка НПВ трансплантата, выполняется формирование анастомоза. В течение кавальной реконструкции трансплантат перфузируется мл или 1 раствора альбумина. Приступают к анастомозу воротной вены, которая предварительно максимально укорачивается. После окончания портального анастомоза снимаются зажимы с нижней полой и воротной вен, начинается реперфузия трансплантата. Кровотечение по линии анастомозов останавливается дополнительными швами. Артериальный анастомоз может быть выполнен в различных вариантах, в зависимости от состояния сосудов донора и реципиента, а также предпочтений хирурга. Наиболее часто артерия трансплантата на уровне чревного ствола анастомозируется с артерией реципиента на уровне гастродуоденальной артерии. В некоторых случаях использование артерии реципиента для анастомоза не представляется возможным (малый диаметр, доминирующая правая печеночная артерия из системы верхней брыжеечной артерии, изменения стенки сосуда после эндоваскулярных вмешательств). В этом случае может быть использована селезеночная артерия трансплантата. Альтернативным вариантом является использование подвздошных сосудов донора или сосудистого протеза и анастомоз с инфраренальным отделом аорты. Имплантация печени завершается билиарной реконструкцией. Наиболее предпочтительна холедохо-холедохостомия без дренирования. При невозможности использования собственного протока следует выполнить холедохоеюностомию. Операция завершается тщательным гемостазом и дренированием брюшной полости.
Донору выполняется левосторонняя латеральная секторэктомия. На основании принципов хирургии живых родственных доноров и необходимости получить жизнеспособный трансплантат с приемлемым анатомическим вариантом кровоснабжения и желчеоттока, основными задачами при операции у донора являются:
- минимизация кровопотери при сохранённом кровоснабжении печени в период разделения паренхимы;
- сокращение времени тепловой ишемии трансплантата;
- получение пригодных для последующей реконструкции участков сосудов (левой печ ночной вены, левой ветви воротной вены и левой печёночной артерии).
Левый латеральный сектор печени.
Операция у детей раннего возраста имеет ряд особенностей ввиду маленьких размеров брюшной полости ребёнка и проявлений основной болезни: гепатомегалии, спленомегалии, а также портальной гипертензии. Факторами, осложняющими операцию, могут быть последствия перенесённого ранее оперативного вмешательства. После пересечения связочного аппарата печени, мобилизации над-, подпечёночных и ретропечёночного отделов нижней полой вены и диссекции на протяжении элементов печёночно-двенадцатиперстной связки приступают к собственно гепатэктомии, которая включает:
- лигирование и пересечение долевых печёночных артерий;
- пережатие воротной вены сосудистым зажимом над областью слияния верхней брыжеечной и селезёночной вен;
- пережатие подпечёночного (над устьями почечных вен), затем надпечёночного отделов нижней полой вены;
- отсечение печени острым путём по паренхиме над нижней полой веной с оставлением на ней небольшого фрагмента;
- продольное рассечение остатка печени над нижней полой веной;
- прецизионное лигирование, клипирование и пересечение коротких вен, дренирующих преимущественно I сегмент и следующих к нижней полой вене от правой доли печени.
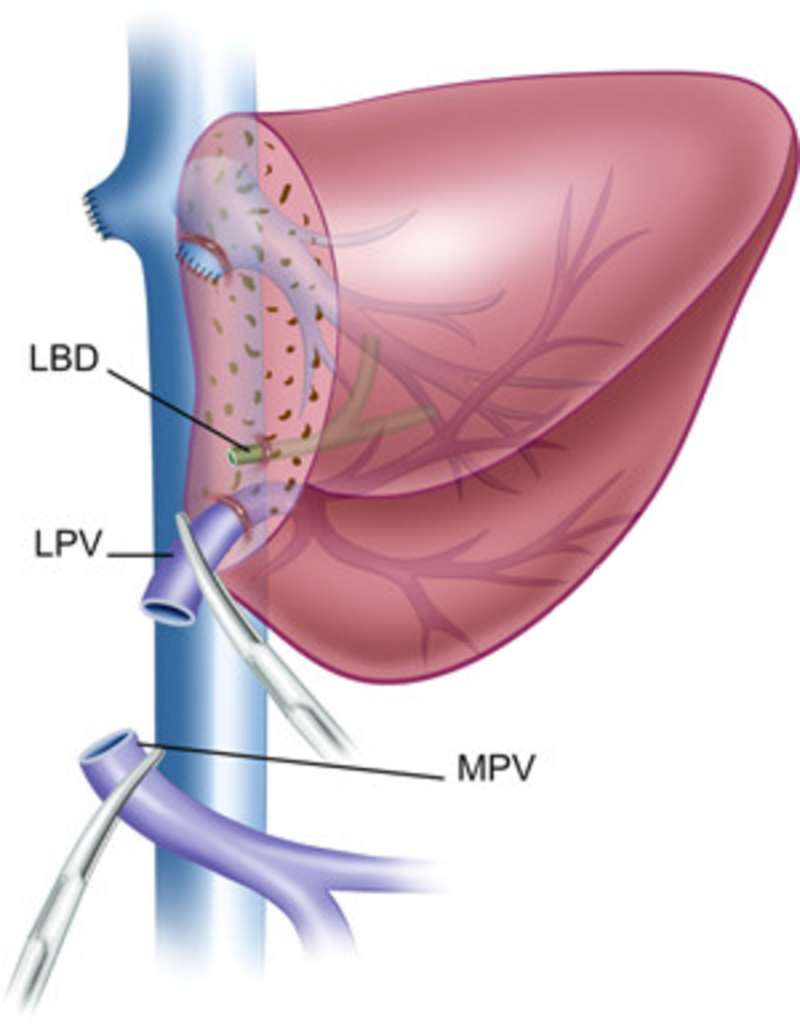
Методика имплантации левого латерального сектора печени После скелетизации и проверки герметичности нижней полой вены приступают к наложению сосудистых анастомозов. При наложении гепатико-кавального анастомоза необходимо создание широкого соустья путём объединения устий печёночных вен реципиента с последующим рассечением нижней полой вены в нисходящем направлении, таким образом создается треугольный дефект последней высотой 2,5-3 см, адекватный сформированному устью левой печ ночной вены трансплантата. Анастомоз накладывается непрерывным швом нитью PDS 5/0 или 4/0. Следующим накладывается порто-портальный анастомоз непрерывным швом нитью PDS 6/0. Завершение портальной реваскуляризации позволяет осуществить реперфузию трансплантата путём поочерёдного снятия зажимов:
- с надпечёночного отдела нижней полой вены;
- с воротной вены;
- с подпечёночного отдела нижней полой вены.
После выполнения гемостаза, следующего за реперфузией, в основном заключающегося в коррекции герметичности гепатикокавального анастомоза и дефектов стенки нижней полой вены, приступают к артериальной реконструкции. Принимается решение о выборе уровня печ ночной артерии реципиента для анастомозирования с левой долевой печёночной артерией трансплантата. Анастомоз накладывается атравматической нерассасывающейся нитью Prolene 7/0. Для увеличения просвета анастомозируемых сосудов прибегают к продольному рассечению соответствующих стенок артерий трансплантата и реципиента. Сосудистые анастомозы необходимо формировать при оптическом 3-х кратном увеличении операционного поля.
Билиарную реконструкцию выполняют путем наложения гепатикоеюноанастомоза с выключенной по Ру петлей тощей кишки. Диаметр протока трансплантата может быть увеличен за счет продольного рассечения его стенки. Дренирование желчных путей при выполнении билиарной реконструкции нецелесообразно. Операция завершается тщательным гемостазом и дренированием брюшной полости.
В раннем послеоперационном периоде пациентам проводится мониторинг, который включает в себя:
- ЭКГ – ежечасно, запись на ленту – 1 р/сут с последующим описанием в отделении функциональной диагностики;
- Пульсоксиметрия – постоянно;
- Частота дыхания – постоянно;
- Диурез – катетер Фолея со стерильным мочеприемником для измерения почасового диуреза;
- Контроль отделяемого из дренажей, учет отделяемого по каждому дренажу в отдельности;
- Учет отделяемого по назогастральному зонду;
- Температура тела – постоянно.
Помимо этого, оцениваются следующие данные:
- Контроль показателей газового и электролитного состава крови, кислотно- щелочного равновесия каждые 3 часа;
- Контроль показателей тканевого метаболизма каждые 3 часа: уровень лактата, содержание глюкозы в плазме крови;
- Общий анализ крови (подсчет форменных элементов крови, уровень гемоглобина, гематокрита) один раз в сутки в течение 1 дней, далее при благоприятном течении послеоперационного периода 2 раза в неделю;
- Биохимическое исследование крови (билирубин (общий прямой), АСТ, АЛТ, ЛДГ, ГГТ, ЩФ, мочевина, креатинин, холестерин) один раз в сутки в течение 7 дней, затем два раза в неделю;
- Показатели коагулограммы (время свертывания крови, протромбиновый индекс, МНО, агрегационная способность тромбоцитов, фибриноген, антитромбин III, протеин С) один раз в сутки в течение 7 дней, затем два раза в неделю;
- Контроль титров группоспецифических антител, проводится в течение первой недели после трансплантации – ежедневно, далее 1 раз в 1-2 дня.С 3-й недели после операции, при условии гладкого течения послеоперационного периода, определение титров антигрупповых антител проводится дважды в неделю. С 4-й недели после операции и до выписки пациентов, перенесших трансплантацию от АВО-несовместимого донора, из стационара достаточным можно считать определение группоспецифических антител 1 раз в неделю (при отсутствии эпизодов их повышения);
- Ежедневные микробиологические исследования крови в течение 7 суток, затем в течение 7 суток 2 раза в неделю;
- Определение концентрации иммуносупрессивных препаратов. В течение 14 суток – ежедневно, далее – не менее 2 раза в неделю;
- УЗИ – ежедневно 1-2р/сут в течение 14 суток;
- Рентгенография органов грудной клетки 1-2 раза в неделю первые 2-3 недели;
- КТ по показаниям
Пациентам проводится антибактериальная, противогрибковая, противовирусная, иммуносупрессивная, гастропротективная, спазмолитическая, инфузионно-трансфузионная терапия, которая подбирается индивидуально.
Иммуносупрессивная терапия, как правило, назначается пожизненно.
После выписки из стационара, пациент должен регулярно наблюдаться амбулаторно.
источник
Печень – самый большой внутренний орган нашего организма. Она выполняет около сотни функций, основными из которых являются:
- Продукция и выведение желчи, которая необходима для пищеварения и всасывания витаминов.
- Синтез белков.
- Дезинтоксикация организма.
- Накопление энергетических веществ.
- Выработка факторов свертывания крови.
Без печени человек прожить не сможет. Можно жить с удаленной селезенкой, поджелудочной железой, почкой (даже при отказе обеих почек возможна жизнь на гемодиализе). Но научиться заменять чем-то функции печени медицина пока не научилась.
А заболеваний, приводящих к полному отказу работы печени, достаточно много и с каждым годом число их увеличивается. Лекарств, эффективно восстанавливающих клетки печени, нет (несмотря на рекламу). Поэтому единственным способом сохранить жизнь человеку при прогрессирующих склеротических процессах в этом органе, остается пересадка печени.
Трансплантация печени – метод достаточно молодой, первые экспериментальные операции были проведены в 60-х годах ХХ века. К настоящему времени по всему миру насчитывается около 300 центров по пересадке печени, разработано несколько модификаций этой операции, число успешно выполненных пересадок печени насчитывает сотни тысяч.
Недостаточная распространенность этого метода в нашей стране объясняется малым количеством центров по трансплантации (всего 4 центра на всю Россию), пробелы в законодательстве, недостаточно четкие критерии по забору трасплантатов.
Если сказать в двух словах, то трансплантация печени показана тогда, когда ясно, что болезнь неизлечима и без замены этого органа человек погибнет. Какие же это болезни?
- Конечная стадия диффузных прогрессирующих заболеваний печени.
- Врожденные аномалии печени и протоков.
- Неоперабельные опухоли (рак и другие очаговые образования печени).
- Острая печеночная недостаточность.
Основные кандидаты на пересадку печени – это пациенты с циррозом. Цирроз – это прогрессирующая гибель печеночных клеток и замещение их соединительной.

- Инфекционной природы (в исходе вирусных гепатитов В, С).
- Алкогольный цирроз.
- Первичный билиарный цирроз печени.
- Как исход аутоиммунного гепатита.
- На фоне врожденных нарушений обмена веществ (болезнь Вильсона-Коновалова).
- В исходе первичного склерозирующего холангита.
Больные циррозом печени погибают от осложнений – внутреннего кровотечения, асцита, печеночной энцефалопатии.
Показаниями для трансплантации является не само наличие диагноза цирроза, а скорость прогрессирования печеночной недостаточности (чем быстрее нарастают симптомы, тем скорее нужно принимать меры для поиска донора).
Существуют абсолютные и относительные противопоказания для этого метода лечения.
Абсолютными противопоказаниями для пересадки печени являются:
- Хронические инфекционные заболевания, при которых происходит длительное персистирование инфекционного агента в организме (ВИЧ, туберкулез, активный вирусный гепатит, другие инфекции).
- Тяжелые нарушения функции других органов (сердечная, легочная, почечная недостаточность, необратимые изменения нервной системы).
- Онкологические заболевания.
Относительные противопоказания:
- Возраст старше 60 лет.
- Ранее перенесенные операции на верхнем этаже брюшной полости.
- Пациенты с удаленной селезенкой.
- Тромбозы воротной вены.
- Низкий интеллект и социальный статус пациента, в том числе и на фоне алкогольной энцефалопатии.
- Ожирение.

- Ортотопическая.
- Гетеротопическая.
Ортотопическая пересадка печени – это пересадка печени донора на свое обычное место в поддиафрагмальное пространство справа. При этом сначала удаляется больная печень вместе с участком нижней полой вены, и на ее место помещается печень донора (целая или только часть).
Гетеротопическая трансплантация – это пересадка органа или его части на место почки или селезенки (к соответствующим сосудам) без удаления своей больной печени.
По видам используемого трансплантата пересадка печени делится на:
- Пересадка целой печени от трупа.
- Пересадка части или одной доли трупной печени (методика СПЛИТ- разделение печени донора на несколько частей для нескольких реципиентов).
- Пересадка части печени или одной доли от ближайшего родственника.
Печень – это орган, очень удобный для подбора донора. Для определения совместимости достаточно иметь одну и ту же группу крови без учета антигенов системы HLA. Еще очень важен подбор по величине органа (особенно это актуально при пересадке печени детям).
Донором может быть человек со здоровой печенью, у которого зафиксирована смерть мозга (чаще всего это люди, погибшие от тяжелой черепно-мозговой травмы). Здесь существует достаточно много препятствий для забора органа у трупа в связи с несовершенностью законов. Кроме того, в некоторых странах забор органов у трупов запрещен.
Процедура пересадки печени от трупа состоит в следующем:
- При установлении показаний для пересадки печени пациент направляется в ближайший центр трансплантации, где проходит необходимые обследования и заносится в лист ожидания.
- Место в очереди на трансплантацию зависит от тяжести состояния, скорости прогрессирования заболевания, наличия осложнений. Довольно четко это определяется несколькими показателями – уровнем билирубина, креатинина и МНО.
- При появлении подходящего трупного органа специальная врачебная комиссия всякий раз пересматривает лист ожидания и определяет кандидата на пересадку.
- Пациент экстренно вызывается в центр (в течение 6 часов).
- Проводится экстренная предоперационная подготовка и сама операция.
Родственная пересадка части печени проводится от кровного родственника (родителей, детей, братьев, сестер) при условии достижения донором возраста 18 лет, добровольного согласия, а также совпадения групп крови. Родственная трансплантация считается более приемлемой.
Основные преимущества родственной пересадки:
- Не нужно долго ждать донорскую печень (время ожидания в очереди на трупную печень может составлять от нескольких месяцев до двух лет, многие нуждающиеся просто не доживают).
- Есть время для нормальной подготовки как донора, так и реципиента.
- Печень от живого донора, как правило, хорошего качества.
- Реакция отторжения наблюдается реже.
- Психологически легче переносится пересадка печени от родственника, чем от трупа.
- Печень способна регенерировать на 85%, часть печени «вырастает», как у донора, так и у реципиента.
Для родственной пересадки печени ребенку до 15 лет достаточно половины одной доли, взрослому – одной доли.
80% всех пересадок печени – это ортотопическая пересадка. Длительность такой операции -8-12 часов. Основные этапы этой операции:

Идеально, когда две операции проходят одновременно и в одной больнице: изъятие органа у донора и гепатэктомия у пациента. Если это невозможно, донорский орган сохраняют в условиях холодовой ишемии (максимальный срок – до 20 часов).
Трансплантация печени относится к самым сложным операциям на органах брюшной полости. Восстановление кровотока через донорскую печень происходит обычно сразу на операционном столе. Но самой операцией лечение пациента не заканчивается. Начинается очень сложный и долгий послеоперационный этап.
Около недели после операции пациент проведет в отделении реанимации.

- Первичная недостаточность трансплантата. Пересаженная печень не выполняет свою функцию – нарастает интоксикация, некроз печеночных клеток. Если не провести срочную повторную трансплантацию, больной погибает. Причиной такой ситуации чаще всего является острая реакция отторжения.
- Кровотечения.
- Разлитие желчи и желчный перитонит.
- Тромбоз воротной вены или печеночной артерии.
- Инфекционные осложнения (гнойные процессы в брюшной полости, пневмонии, грибковые инфекции, герпетическая инфекция, туберкулез, вирусный гепатит).
- Отторжение трансплантата.
Отторжение трансплантата – это основная проблема всей трансплантологии. Иммунная система человека вырабатывает антитела на любой чужеродный агент, попадающий в организм. Поэтому если не подавлять эту реакцию, произойдет просто гибель клеток донорской печени.
Поэтому пациенту с любым пересаженным органом придется всю жизнь принимать препараты, подавляющие иммунитет (иммуносупрессоры). Чаще всего назначается циклоспорин А и глюкокортикоиды.
В случае с печенью особенность в том, что с течением времени риск реакции отторжения снижается и возможно постепенное снижение дозы этих препаратов. При пересадке печени от родственника также требуются меньшие дозы иммуносупрессоров, чем после пересадки трупного органа.
После выписки из центра больного просят в течение 1-2 месяцев не уезжать далеко и еженедельно наблюдаться у специалистов центра трансплантации. За это время подбирается доза иммуносупрессивной терапии.
Пациенты с пересаженной печенью, получающие постоянно препараты, подавляющие иммунитет – это группа высокого риска прежде всего по инфекционным осложнениям, причем заболевание у них могут вызвать даже те бактерии и вирусы, которые у здорового человека болезней обычно не вызывают (условно-патогенные). Они должны помнить, что при любых проявлениях инфекции им нужно получать лечение (антибактериальное, антивирусное или противогрибковое).
И, конечно, несмотря на наличие современных препаратов, риск реакции отторжения сохраняется всю жизнь. При появлении признаков отторжения требуется повторная трансплантация.
Несмотря на все трудности, более чем тридцатилетний опыт трансплантологии печени показывает, что пациенты с донорской печенью в подавляющем большинстве живут более 10 лет после пересадки, возвращаются к трудовой активности и даже рожают детей.

Пациентам, не желающим ждать и имеющим деньги, интересно будет знать цены на платную трансплантацию.
Операция пересадки печени относится к самым дорогим. За рубежом цена такой операции составляет от 250 до 500 тыс. долларов. В России- порядка 2,5-3 миллионов рублей.
Существует несколько основных центров по пересадке печени, а также есть около десятка медучреждений в крупных городах, имеющих на это лицензию.
- Основной центр пересадки печени в России – ФНЦ трансплантологии и искусственных органов им. Шумакова, Москва;
- Московский центр трансплантации печени НИИ Скорой помощи им. Склифосовского;
- РНЦРХТ в Санкт-Петербурге;
- ФБУЗ « Приволжский окружной медицинский центр» в Нижнем Новгороде;
- Пересадками печени занимаются также в Новосибирске, Екатеринбурге, Самаре.
источник
Сайт предоставляет справочную информацию исключительно для ознакомления. Диагностику и лечение заболеваний нужно проходить под наблюдением специалиста. У всех препаратов имеются противопоказания. Консультация специалиста обязательна!
Печень является одним из жизненно важных органов. Современные врачи уже научились пересаживать большинство органов. Самой дорогой является пересадка печени.
Первая трансплантация печени была осуществлена в 1963 году в Денвере. Донором был умерший человек. Особый статус операция имеет, в том числе, и потому, что ткани печени очень легко повреждаются. Поэтому сохранить и пересадить орган в целостности очень сложно. Еще одной проблемой была работа иммунной системы больного, которая всеми силами отторгала чужеродные ткани. И только к 80-м годам проблема была решена – были созданы лекарства, предупреждающие разрушение пересаженного органа иммунитетом реципиента (получателя).
Больше всего пересадок осуществляется ежегодно в США, Японии и Европейских странах. Сегодня количество пересаженных органов исчисляется тысячами в год. Но даже при таких количествах операций далеко не все нуждающиеся до них доживают. Пересадку осуществляют, в основном, в специальных центрах.
В конце 80-х годов в трансплантации печени произошел значительный сдвиг. То, что ткани печени способны к регенерации, врачам было известно давно. И именно этот факт натолкнул ученых на идею о трансплантации части печени. Методика такой пересадки была разработана в Соединенных Штатах Америки. Для трансплантации изымали из организма кровного родственника левую часть печени. Ее и пересаживали больному.
Подобное решение вопроса очень выгодно с нескольких точек зрения:
1. Орган обычно достаточно хорошего качества.
2. В некоторых странах религия не разрешает брать органы у трупов.
3. То, что орган уже есть и его не нужно искать, дает врачам возможность тщательно подготовиться.
Дать часть своего органа может лишь кровный родственник, которому уже исполнилось 18 лет. Группы крови, в лучшем случае, должны быть одинаковыми, в крайнем случае — совместимыми.
Если пересаживают от взрослого ребенку, нужна лишь одна половина левой доли.
Современные российские ученые разработали методику пересадки правой доли. До нее легче добраться, она быстрее приживается, так как имеет большие размеры. Причем это не ухудшает состояния донора.
- Гепатиты вирусные (кроме А),
- Врожденные аномалии развития,
- Гепатиты аутоиммунной природы: склерозирующий холангит, билиарный цирроз печени в первичной форме,
- Болезнь Вильсона,
- Поликистоз печени,
- Гемохроматоз,
- Онкологические заболевания печени (не всегда),
- Муковисцидоз,
- Нарушение метаболизма альфа-1-антитрипсина,
- Печеночная недостаточность в острой форме, вызванная отравлением.
Перечисленные заболевания вызывают увеличение количества соединительных волокон в тканях печени. Постепенно их становится так много, что печень перестает выполнять свою функцию. Печень является незаменимым органом, так как она обеспечивает выведение ядовитых веществ из организма, терморегуляцию, метаболизм, переработку пищи.
На окончательной стадии разрушения органа у пациента появляются асцит, кровотечения в органах пищеварения, желтуха, ухудшается сон, увеличивается диаметр пищеводных вен. На такой стадии болезни пациенту грозит печеночная кома и летальный исход.
Если больным, например, с почечной недостаточностью, можно проводить гемодиализ, то работу печени никакими приборами пока заменить невозможно. И единственным шансом к спасению жизни является пересадка печени.
Временным решением проблемы неработающей печени является альбуминовый гемодиализ. Но эта процедура может помочь на считанные часы. Чаще всего ее назначают уже после трансплантации, до тех пор пока уже пересаженный орган не начнет свою работу.
Существует всего два источника донорской печени:
1. От погибшего человека, у которого совершенно здоровая печень,
2. От живого человека. Изымается лишь часть печени. Процедура безопасна для донора, ведь даже после изъятия части печени уже через некоторое время ее объем достигает 85% прежнего.
В связи с тем, что найти целую здоровую печень от умершего донора очень сложно, в мире все больше используют часть органа, изъятую у здорового и живого родственника пациента.
В операции участвуют гепатолог, хирург, координатор. Иногда подключают кардиолога и пульмонолога.
На животе больного делается надрез в форме буквы L. Для того чтобы откачать из печени кровь и жидкость, применяется специальный прибор. В брюшную полость вводятся дренажные трубки и оставляются там, иногда, на несколько дней.
В желчный проток больному вставляют трубку для отвода желчи. Для врачей очень важен как объем выделившейся желчи, так и ее цвет. Она может быть желтой или зеленой. Трубку иногда оставляют в уже приживленном органе на несколько месяцев.
Кровеносные сосуды перерезаются и пораженный орган изымается. Все это время насос качает кровь от ног к сердцу. Далее орган или его часть переносятся в тело больного, сшиваются кровеносные сосуды и желчные протоки. Желчный пузырь в организм больного не пересаживается.
Первое время вместо пока еще не «запущенной» в ход печени ее работу выполняет аппарат «искусственная печень».
В период восстановления очень важным является супрессия иммунитета, который будет пытаться отторгнуть чужеродные ткани. Наиболее вероятным отторжение является первые полгода после трансплантации.
Азиатские страны стали пионерами в этой области потому, что их религия и культура не позволяет использовать части тела умерших людей для пересадки. Именно эти страны добились наилучших показателей по выживаемости после трансплантации печени. Сегодня в Японии 99% всех трансплантаций печени осуществляется именно от живого донора, в Соединенных Штатах Америки — 80%.
Такая практика в первую очередь позволяет обеспечить практически всех нуждающихся. В Америке, например, среди ожидающих трансплантации умирают лишь 10%, а в России 50% (здесь не так развита практика пересадки от живого донора).
Печень от живого донора лучше приживляется. Причем, лучше всего осуществляются пересадки детям. Здесь выживаемость у 92% пациентов (если печень взята у родственника). После пересадки органа, изъятого из трупа, этот показатель составляет 85%. Даже среди пациентов с новообразованиями выживаемость достаточно высока – 80%.
Чем этот метод лучше, чем пересадка от трупа?
1. Не нужно ожидать появления «подходящего трупа»,
2. Орган лучше приживляется,
3. Можно пить меньше иммуноподавляющих препаратов,
4. Период холодовой ишемии печени донора уменьшается (особая подготовительная процедура),
5. Ускоряется процесс подготовки органа.
Есть и недостатки метода:
1. Существует вероятность осложнения у донора,
2. Техника операции более тонкая. Доктор должен иметь не только практику сосудистого хирурга, но и опыт по хирургии печени,
3. В связи с тем, что пересаживается лишь небольшая часть, ее следует правильно «подогнать» под организм пациента,
4. Вероятность возврата первичного заболевания у реципиента увеличивается.
Сегодня можно сказать, что данная процедура только отрабатывается хирургами всех стран мира. Одним из важнейших моментов в вопросе о пересадке от живого донора является показатель смертности. К сожалению, погибают не только реципиенты, но и доноры. Так, после разглашения данных о нескольких смертях доноров количество пересадок от родственников уменьшилось на 15 часть в год.
Японские ученые утверждают, что осложнения у доноров развиваются приблизительно в 12% случаев. Причем чаще страдают доноры, у которых изымают правую долю органа. Наиболее частым осложнением является тромбоз воротной вены, послеоперационные грыжи и истечение желчи. Уже через год после операции почти все доноры могут продолжать привычный образ жизни.
2. Иммунологические проблемы. Печень занимает особое отношение к иммунной системе. Она менее уязвима, чем другие органы. Но, несмотря на это, у многих пациентов присутствуют признаки отторжения в большей или меньшей степени. Отторжение может быть острым (с ним можно успешно бороться) и хроническим (такая форма не поддается контролю). При пересадке части органа от живого родственника отторжение, практически, не наблюдается.
3. Кровотечение – наблюдается в среднем в 7,5% случаев.
4. Сосудистые осложнения: стеноз печеночной артерии, тромбоз, синдром обкрадывания. Наблюдаются в среднем в 3,5% случаев. Осложнения этой категории очень опасны и нередко приводят к необходимости повторной пересадки. Развиваются такие осложнения по вине хирурга. Если осложнение обнаруживается на ранней стадии и срочно приняты меры, положение может быть спасено.
5. Тромбоз либо стеноз воротной вены. При пересадке от живого донора наблюдается в среднем в 1,3% случаев. Обнаруживается по определенным признакам и с помощью УЗИ. Принятые срочно меры могут спасти исход операции.
6. Обструкция печеночных вен. Встречается редко и чаще всего по ошибке хирурга. Чаще наблюдается при пересадке части органа.
7. Билиарные стриктуры и желчеистечение. Наблюдаются достаточно часто в 25% случаев независимо от возраста пациента.
8. Синдром малого размера трансплантата (только при пересадке от живого донора) наблюдается, если врачи неправильно вычислили размер пересаживаемой части. Если признаки не исчезают в течение двух суток, необходимо делать повторную трансплантацию.
9. Инфицирование. У многих пациентов инфицирование протекает без клинических проявлений. У некоторых же возможно развитие воспаления легких и даже летальный исход. Для предупреждения инфицирования, пациент должен принимать антибиотики, до тех пор пока не будут удалены все дренажи и катетеры.
Чтобы процесс приживления органа шел успешно, пациенту ни в коем случае нельзя приостанавливать прием препаратов по собственному желанию.
Кроме этого, прием любых других лекарств тоже должен осуществляться только после консультации гепатолога. Иммуносупрессоры придется пить до конца жизни, но подавляющее большинство больных привыкают и не испытывают никаких неудобств в связи с этим.
Время от времени нужно сдавать анализы мочи, крови на присутствие вирусов, а также на уровень иммуносупрессоров, УЗИ печени, почек, сердца, поджелудочной, электрокардиограмму. Иногда доктор прописывает дополнительные диагностические методы.
Если пациент до трансплантации был заражен вирусом гепатита В или С, после операции существует вероятность активизации вируса. Это может спровоцировать отторжение печени. Более опасен в этом смысле вирус гепатита В, а при дельта-вирусе отторжение бывает очень редко.
После операции, желательно, нахождение в специальном реабилитационном центре под наблюдением специалистов.
Очень важно соблюдать режим питания. Пища не должна осложнять работу печени. Пациент должен получать домашнюю еду, включающую достаточное количество калорий. Уменьшить в рационе жареное, жирное, копченое. Питаться дробно по 4 раза в день. Основную долю пищи должны составлять овощи и фрукты. Категорически запрещены спиртные напитки. Следует меньше пить кофе, отказаться от никотина (по крайней мере, на некоторое время после операции).
В связи с тем, что иммунитет пациента подавляется с помощью специальных препаратов, он очень уязвим для инфекций. Поэтому лучше не бывать в людных местах и, ни в коем случае, не посещать друзей и родных, больных ОРВИ, гриппом или другими подобными заболеваниями.
Многие больные после трансплантации возвращаются к своей работе (85%). Но на этот показатель влияет и возраст пациента. Важно хорошо отдыхать и высыпаться. Конечно, если до операции работа больного была связана с большими физическими нагрузками, ее следует сменить. Кроме этого, теперь противопоказаны и многие виды спорта.
Существуют данные о женщинах, которые после трансплантации печени успешно беременели и воспроизводили на свет совершенно здоровых деток.
Психологические проблемы у пациентов после подобной операции наблюдаются крайне редко, поэтому они хорошо адаптируются в обществе.
Через определенный период времени у пациентов с пересаженной печенью могут появиться некоторые проблемы со здоровьем. Самые распространенные: инфекционные заболевания, нарушение работы желчного протока и сосудов.
Нарушения выявляются на периодических приемах у различных специалистов. Сужение желчного протока из-за появления шрамов устраняется с помощью стентов, вводимых эндоскопически. Чаще всего все основные осложнения проявляются в первые 6 месяцев после операции.
Прием иммуносупрессоров может привести к увеличению массы тела, нарушению обменных процессов, сахарному диабету и изменению метаболизма липидов. Поэтому такие пациенты более подвержены инсультам, инфарктам.
Если трансплантацию проводили пациенту с алкогольным циррозом, новообразованиями или гепатитом, ему необходимы периодические проверки, так как заболевание может рецидивировать.
На прогноз выживаемости очень большое влияние оказывает предоперационное состояние больного. Так, если он на время трансплантации был в работоспособном состоянии, его шанс выжить на протяжении года составляет 85%. Если перед трансплантацией больной долго лежал в больнице, его шанс составляет 70%, если же он находился в отделении интенсивной терапии, то шанс уменьшается до 50%. Таким образом, чем раньше проведена трансплантация, тем выше вероятность благоприятного исхода.
Еще один параметр, влияющий на выживаемость – это то, по какому диагнозу попадает на пересадку больной. Так, в группе высокого риска люди с гепатитом В, раком печени, молниеносным гепатитом, с тромбозом воротной вены, с осложнением в виде почечной недостаточности, те, которым нужно делать искусственную вентиляцию легких и те, которые много раз до этого оперировались по другим поводам. Кроме этого, к группе высокого риска относятся и больные старше 65 лет.
Пациенты, не относящиеся к вышеперечисленным категориям, включаются в группу низкого риска.
Выживаемость на протяжении года в первой группе составляет 60%, на протяжении 5 лет – 35%.
Выживаемость на протяжении года во второй группе составляет 85%, на протяжении 5 лет – 80%.
Если пациенту второй раз пересаживают печень, вероятность выжить у него составляет 50%. Причина неудачной операции при этом не имеет значения.
Многие пациенты, перенесшие пересадку печени, выживают на протяжении десяти – пятнадцати и даже двадцати пяти лет. Не следует забывать, что на пересадку идут лишь те люди, у которых нет других возможностей для выживания. Кроме этого, технологии пересадки каждый год развиваются, и показатели выживаемости улучшаются.
Показания:
- Нарушения обменных процессов,
- Холестатические нарушения,
- Цирроз печени,
- Острая печеночная недостаточность,
- Врожденный порок формирования желчных протоков (билиарная атрезия).
Наиболее предпочтительным является, в таком случае, метод пересадки от живого донора, являющегося кровным родственником.
В период подготовки проводится резонансная томография, позволяющая обследовать мелкие кровеносные сосуды и желчные протоки. Чаще всего используют боковую часть левой доли печени. Это связано с тем, что расположение сосудов в ней наиболее подходящее для детского организма.
Хотя прогноз лучше для детей с большей массой тела и старшим возрастом, этот фактор ни в коем случае не должен быть определяющим при выборе времени операции. Так как неработающая печень тормозит развитие детского организма.
Родителям детей, которым показана трансплантация печени, не следует впадать в панику. Сегодня подобная операция уже достаточно хорошо отработана и успешно проводится. Так, например, в Минске была проведена операция полуторагодовалой девочке, отравившейся поганками. Печень ребенка полностью перестала работать. Операцию нужно было сделать настолько быстро, что даже не было времени обследовать родителей в качестве потенциальных доноров. Поэтому девочке пересадили орган от умершего восьмимесячного малыша.
При отравлении бледной поганкой печень тут же перестает функционировать и восстановить ее работу не представляется возможным.
Процедура длилась 10 часов. Операция прошла достаточно успешно. Девочка чувствует себя хорошо. Времени, правда, прошло не так много (всего, около года), но данный факт дает надежду на то, что в будущем подобные операции станут вполне нормальным явлением.
Если в сутки женщина будет выпивать по 20 гр. чистого алкоголя, а мужчина 40 гр., у них начинает поражаться печень.
Еще одним фактором, приводящим к циррозу и необходимости пересадки, является аутоиммунный гепатит. Достаточно длительное время это заболевание можно контролировать с помощью гормональных противовоспалительных препаратов и других лекарств.
Кроме этого, пожилые представительницы слабого пола страдают первичным билиарным циррозом, при котором также единственным методом спасения жизни является пересадка.
Молодые мужчины нередко страдают склерозирующим холангитом, также приводящим к пересадке печени. У таких пациентов желчные протоки становятся непроходимыми.
Пересадку назначают в том случае, если цирроз поразил большую часть органа, при частых кровотечениях из вен пищевода, асците, печеночной коме, а также при явно слабой работе органа.
На фоне вирусных заболеваний печени или цирроза значительно увеличивается развитие рака печени – гепатоцеллюлярной карциномы.
Если размер опухоли невелик, пересадка может дать очень хорошие результаты. Операция по удалению опухоли чаще всего не очень эффективна, так как после нее часто развивается рецидив. Лишь в том случае, если рак не сочетается с циррозом, операция может быть действенной. Используется трансплантация и при других видах новообразований, например, при эндокринных опухолях.
Если раком поражены желчные протоки, существует высокий риск того, что даже после пересадки печени опять разовьется опухоль. Лишь если новообразование очень мало и перед пересадкой больной прошел химиотерапию и местную радиотерапию, существует шанс излечиться с помощью пересадки.
Если печень поражена метастазами, пересадка бесполезна, так как это означает, что метастазы присутствуют уже и в других органах.
Если при гепатите С осуществляют трансплантацию печени, то повторное заражение органа после пересадки наблюдается почти у ста процентов больных. Перерождение клеток в уже прижившемся органе под действием употребления иммунодепрессантов происходит скорее. У трети больных через пять лет после пересадки опять наблюдается цирроз и им опять нужно делать пересадку.
Гепатит С прогрессирует быстрее у:
- Людей старше 40 лет,
- При наличии цитомегаловируса,
- При употреблении кортикостероидов,
- При длительной холодовой ишемии органа перед пересадкой,
- При пульс-терапии мощными дозами кортикостероидов на фоне отторжения приживленного органа.
Применение противовирусных препаратов до операции и после нее уменьшает интенсивность повторного развития болезни после пересадки. Около 40% пациентов могут быть подвергнуты противовирусной терапии.
В Америке трансплантация стоит около 500 тыс. долларов.
В Европе операция по трансплантации печени стоит от 230 до 400 тысяч евро.
В Сингапуре за программу по пересадке, включающую 30 суток в больнице для пациента и неделю для донора придется выложить 120 тыс. евро.
В Москве пересадка обойдется в 2,5 – 3 млн. рублей.
В Украине от родственного донора можно пересадить часть органа за 100 тыс. гривен.
Автор: Пашков М.К. Координатор проекта по контенту.
источник