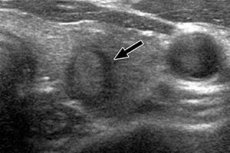
Часто после проведения обследования пациенты буквально впадают в панику, обнаруживая непонятные им специфические медицинские термины, например, «гипоэхогенное образование в печени». В этом случае пугаться не стоит, так как этот термин не означает заболевание, а лишь является характеристикой обнаруженного в печени образования.
Гипоэхогенное образование в печени
При проведении ультразвукового обследования могут обнаруживаться особые участки, которые отличаются от других тканей органа более низкой плотностью. Аппарат УЗИ посылает в орган звуковые волны высокой частоты.
Структуры органа, имеющие разную плотность и строение, по-разному отражают эти волны, которые возвращаются обратно, фиксируются особыми датчиками аппарата УЗИ и формируют картину состояния органа. Если в структуре органа имеется образование или участок с более низкой плотностью, чем другие части или ткани, оно будут выглядеть на экране УЗИ как гипоэхогенное образование в печени.
Обследование на УЗИ позволяет не просто определить наличие таких образований, но и узнать их месторасположение, количество и размеры. На экране гипоэхогенная зона выглядит как темное пятно. Чаще всего в роли таких образований выступает участок ткани в виде полости, заполненной жидкостью. Она обычно бывает окружена тонкими стенками, отделяющими ее от соседних тканей. У нее могут быть гладкие ровные края или же неровные очертания.
Наличие гипоэхогенных зон свидетельствует о патологии в печени, однако она может быть как доброкачественной, так и злокачественной природы.
Четкие ровные контуры структуры могут указывать на ее паразитарное происхождение, например, на лямблии или эхинококки в печени, окруженные плотной капсулой, или же на наличие обычной кисты. Криволинейные или расплывчатые образования также могут оказаться кистами, опухолями различного происхождения или фиброаденомами.
Выявление таких участков в печени потребуют дополнительных исследований и взятия анализов. Если существует онкологическая настороженность, может возникнуть необходимость при возможности взятия биопсии образования, чтобы исключить раковую опухоль или же метастаз.
Симптомы гипоэхогенного образования в печени
Больной обращается за медицинской помощью и обследованием, если ощущает постоянный дискомфорт в области печени. Это может выражаться:
- Болями в правом боку и эпигастральной области – рвущими, ноющими или колющими.
- Часто боли сопровождаются изжогой и тошнотой после приема пищи, чувством горечи во рту, особенно хорошо ощутимым с утра, увеличением печени, отсутствием аппетита или искажением вкуса.
- Некоторые больные жалуются на необъяснимое и достаточно резкое снижение веса
- Появление желтых пятен или пожелтению кожных покровов и белков глаз, зуду кожи.
Все эти симптомы могут относиться к разнообразным патологиям печени и желчного пузыря. Так как они очень субъективны, то четко указывать на конкретное заболевание не могут.
Само наличие участков затемнения на эхограмме не означает обязательной патологии, однако сочетания субъективных жалоб и показания УЗИ – это повод для углубленного исследования с целью исключения опасных для жизни заболеваний, таких как цирроз и рак печени, метастазы в этот орган или глистная инвазия.
Ультразвуковое исследование печени
Проведение УЗИ-диагностики поможет выявить наличие разнообразных образований и дать возможность разобраться в причинах недомогания больного.
Иногда по внешнему облику, которое имеет гипоэхогенное образование в печени, можно сделать первичные выводы об имеющейся проблеме:
- Аденомы проявляются затененными участками с однородной структурой, возможно, с единичными включениями материала другой плотности и гладким краем.
- На абсцессы печени могут указывать многочисленные очаги инфицирования с неровными контурами, возможно, с включениями пузырей внутри, при этом внешняя оболочка плотная и хорошо отражающая сигналя УЗИ.
- Ровные контуры темного пятна с имеющимися внутри него отраженными сигналами ультразвуковых волн могут указывать на кисту с внутренними одиночными или множественными кровоизлияниями.
- Круглые с бугристым краем образования могут свидетельствовать о наличии цирроза печени.
- Если образования имеют форму овала и/или треугольника, локализуются возле воротной вены или желчного пузыря, а у пациента имеются признаки жирового перерождения печени, логично предположить, что это оставшиеся нетронутыми части здоровой печеночной ткани.
- Если на экране возникает неравномерное образование с фрагментами кальцификатов, кровоизлияниями, это дает возможность заподозрить смертельно опасное заболевание – рак печени.
- Метастазы из других органов также имеют неравномерные очертания без четких контуров, при этом основные ткани печени без изменений.
- Глистные капсулы читаются как четкие образования, обычно округлой или овальной формы, с плотным гладким краем и полостью, заполненной жидкостью. Внутри капсулы имеются участки уплотнений, заметные на экране.
Диагностика при помощи УЗИ позволяет «вычислить» наличие патологий и несколько сузить круг возможных заболеваний. Эта несложная для пациента процедура помогает лечащему врачу в проведении дальнейших исследований и точной постановке диагноза.

Каждое из выявленных при помощи УЗИ заболеваний печени имеет свое специфическое лечение. Например, лечение цирроза зависит от степени заболевания и включает в себя как медикаментозное лечение, так и полное изменение больным образа жизни. Иногда для спасения жизни пациента приходится прибегать к оперативному вмешательству с целью удаления очага заболевания или же полной пересадки всего органа.
При лечении абсцессов активно используются антибиотики, которые назначаются лечащим врачом с учетом всех имеющихся у пациента заболеваний, его возраста и стадии болезни. Обязательно принимается во внимание возможная индивидуальная реакция на лекарства и склонность к аллергиям.
Если УЗИ дает основание заподозрить рак или метастазы, обследования должны проводиться глубже и тщательнее для выявления очага заболевания и подтверждения (или опровержения) диагноза.
Если данные находят свое подтверждение, больного передают онкологам, ему назначают специфическое противоопухолевое лечение , которое зависит от типа опухоли, а если это метастаз, то лечение должно быть направлено против основного очага и способствовать уменьшению и исчезновению метастазов. Не все обнаруженные участки пониженной плотности требуют лечения, по крайней мере, медикаментозного. В некоторых случаях достаточно соблюдения диеты, похудения и смены образа жизни, поэтому пугаться заключения УЗИ совершенно не стоит.
Больше информации о подготовке к УЗИ печени можно узнать из видео.
источник
Ультразвуковое исследование основано на способности органов отражать волны высокой частоты. Иногда диагностика выявляет участки с пониженной плотностью, они могут иметь различную форму, размер, определяются и описываются в протоколе УЗИ как «гипоэхогенное образование в печени».
При обнаружении в протоколе исследования данной формулировки не нужно делать поспешных выводов самостоятельно, эффективнее обратиться к специалисту, который подробно расскажет о выявленных элементах и назначит лечение, а при необходимости и дополнительные методы исследования.
Помимо снижения акустической плотности печени могут выявляться участки с ее увеличением, которые называются гипоэхогенным образованием.
Любое из выявленных отклонений в проводниковой способности органа говорит о формировании патологического очага в структуре печеночной ткани. Это может быть доброкачественное или злокачественное образование, имеющее различные формы и степень распространенности, а также выявляемое в единственном или множественном числе. Подробное изучение характеристик и расположения данных образований способствует постановке диагноза и подбору возможного лечения.
При подозрении на злокачественную опухоль скорее всего будет назначена биопсия патологической структуры для гистологического изучения, по результатам которой и оценивается опасность данного заболевания.
Качественное исследование печени с помощью УЗИ и определение всех характеристик выявленной патологии позволяет с большой долей достоверности установить имеющийся диагноз.
Возможные заболевания печени, проявляющиеся пониженной проводимостью ультразвуковой волны:
- Цирроз печени на УЗИ – определяются множественные узлы небольшого размера (по несколько миллиметров), вся поверхность органа имеет бугристую структуру, возможно увеличение или уменьшение органа в сравнении с показателями нормы.
- Геморрагическая киста определяется в виде четко очерченного очага круглой или продолговатой формы, имеющего четко очерченные границы. В центре кисты визуализируется жидкость, которая проявляется как очаг анэхогенного образования. Киста может быть единичная, нередко определяется поликистоз (много включений в ткани печени).
- Абсцесс проявляется включением в виде неровного образования с определяемыми пузырьками газа в центре патологического очага.
- Аденома описывается как псевдокапсула с четкими краями (имеется валик более плотной ткани, окружающий патологический очаг). Аденома имеет однородную структуру и характеризуется наличием четкой границы от здоровой ткани.
- Карцинома определяется при исследовании ультразвуком обычно в содружестве с метастазами, поразившими окружающие ткани и органы.
- Тромбоз воротной вены.
- Капсулы, характеризующие глистное поражение печени, имеют четкую форму с усилением эхогенности в центре, окруженной жидкостью.
- Признаки жирового перерождения печени по УЗИ определяются в локализации желчного пузыря и воротной вены, имеют треугольную или овальную форму.
Однако существуют заболевания, определение которых даже первоначально затруднительно по одним лишь признакам ультразвуковой диагностики. При необходимости дифференцировать болезнь большое внимание уделяется клиническим проявлениям недуга, анализам крови и другим данным, полученным с использованием разнообразных принципов современного исследования.
Главной опасностью патологии печени считается длительное бессимптомное течение. Отсутствие нервных окончаний в печеночных тканях позволяет недугу распространиться на значительную площадь и укорениться. Рак выявляется чаще при метастазировании в окружающие ткани, что значительно затрудняет лечение.
Диагностическое исследование печени в процессе жизнедеятельности с интервалом в 1-2 года позволит избежать печального опыта определения болезни на поздних стадия развития.
Помимо очагов гипоэхогенного характера при доброкачественном поражении специалист опишет полную картину, отраженную на аппарате ультразвукового исследования. Важно место расположения патологии, распространенность и глубина поражения, прорастания в прилегающие ткани и структуры, единичное включение или множественное распространение.
Одним из достоинств УЗИ можно считать возможность просканировать не только интересующий орган, но все структуры, окружающие его, а при необходимости и все органы брюшной полости. Неограниченность в осмотре пределами одной лишь печени позволяет:
- оценить общую картину заболевания;
- определить реальный риск здоровью и жизни человека;
- назначить необходимый направленный объем дополнительного обследования, не распыляя силы на ненужные диагностические процедуры.
В описании обязательно будет указана доля пораженной печени, размеры и структура. При разрастании опухоли более 3 см будет нарушена структура всего органа, края потеряют четкость и в результатах размер будет превышать нормальные показатели УЗИ печени.
В проекции гипоэхогенного образования печени при злокачественном поражении будет наблюдаться изменение в строении сосудистой сети и желчных протоков.
При прорастании опухоли в крупный сосуд процесс приобретает угрожающее значение. Обильное кровоснабжение новообразования ускоряет процессы ее распространения и метастазирования по организму. Вовлечение сосудистой сети в процесс хорошо определяется при ультразвуковой диагностике с применением доплера, определяется усиление рисунка с хаотично расположенными линиями кровеносного русла.
Выявление гипоэхогенных участков в печени позволяет заподозрить патологию органа и определить дальнейший объем диагностики. Лишь после проведения целого комплекса исследования выставляется окончательный диагноз, от которого будет зависеть дальнейший объем терапевтического и хирургического вмешательства.
источник
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Инструментальная диагностика методом ультразвукового сканирования (УЗИ), которое также называется ультрасонографией, может выявлять во внутренних органах и полостях участки с различной акустической плотностью – гиперэхогенное или гипоэхогенное образование.
Локальное гипоэхогенное образование в том или ином органе, в отличие от гиперэхогенного, является результатом более низкой эхогенности тканей – в сравнении с параметрами акустической плотности здоровых тканей органа. То есть данный участок слабо отражает направленный на него ультразвуковой сигнал (в частотных диапазонах 2-5, 5-10 или 10-15 МГц). И это свидетельство того, что данное образование – с точки зрения его структуры – либо содержит жидкость, либо имеет полость.
Гипоэхогенное образование на экране визуализируются в виде серых, темно-серых и практически черных зон (при гиперэхогенности зоны светлые, часто – белые). Для расшифровки ультразвукового изображения существует шкала шести категорий серого Gray Scale Imaging, где каждый пиксель полученного на мониторе изображения гипоэхогенного образования – в зависимости от силы ультразвукового сигнала, возвращающегося на датчики – представляет собой конкретный оттенок серого.
Расшифрованные узи-диагностами (сонографами) результаты ультразвукового обследования изучаются врачами конкретного профиля (эндокринологом, гастроэнтерологом, урологом, нефрологом, онкологом и др.), сопоставляются с показателями сданных пациентами анализов и результатами прочих исследований.
Во многих случаях требуется дифференциальная диагностика, для чего, кроме УЗИ, используются другие аппаратные методы визуализации патологии (ангиография, цветная допплерография, КТ, МРТ и т.д.), а также проводится гистологическое исследование биоптатов.
Как показатель ультрасонографии, гипоэхогенное образование может иметь любую локализацию. Причины гипоэхогенного образования также разные и полностью зависят от этиологии и патогенеза тех заболеваний, которые развиваются у пациентов.
Например, гипоэхогенное образование в поджелудочной железе считается диагностическим критерием выявления таких патологий, как кисты, геморрагический панкреатит, муцинозная цистоаденома (которая склонна к малигнизации), аденокарцинома головки поджелудочной железы, метастазы при злокачественных опухолях других органов.
Здоровые печеночные ткани умеренно гиперэхогенны, и гипоэхогенное образование в печени может быть при циррозных очагах; очаговом стеатозе; кистах (в том числе при Echinococcus multilocularis); билиарном абсцессе; гепатоцеллюлярной аденоме; очаговой паренхиматозной гиперплазии; гепатоме и холангиоцеллюлярной аденокарциноме небольших размеров.
Гипоэхогенные образования визуализируются также в случаях распространения в печень диффузных метастазов рака поджелудочной железы, яичников, молочных желез, яичка, желудочно-кишечного тракта.
В УЗИ-диагностике патологий желчного пузыря особое значение имеет строение его стенок, так как при отсутствии повреждений органа они визуализируется в виде трех слоев: внешнего и внутреннего гиперэхогенных и среднего гипоэхогенного.
Среди причин, вызывающих гипоэхогенное образование в желчном пузыре, следует назвать полипы, аденокарциному (с интактным внешним слоем пузыря), лимфомы (опухоли лимфоузов), ангиосаркому.
В норме эхогенность селезенки однородна, хотя чуть выше, чем печени. Но из-за высокой васкуляризации УЗИ селезенки проводится с контрастным веществом, которое накапливается в паренхиме и дает возможность (в конце паренхиматозной фазы) визуализировать очаговые поражения и гипоэхогенные образования селезенки.
К числу таких образований относят:
- острую интрапаренхимальную гематому при разрыве селезенки (вследствие травмы живота);
- гемангиомы (доброкачественные сосудистые образования) при спленомегалии;
- инфаркты селезенки (инфильтративные или гематологические);
- лимфому селезенки;
- метастазы различного происхождения (чаще всего саркомы мягких тканей, остеосаркомы, рака почки, молочной железы или яичников).
Как отмечают специалисты, эхинококковые, солитерные и дермоидные кистозные образования селезенки могут иметь эхоструктуру смешанного характера.
Гипоэхогенное образование в почке может быть выявлено при включениях в паренхиму кистозных образований (в том числе недоброкачественных), гематомах (на начальных стадиях), пиогенных паранефральных абсцессах (на стадии некроза) или кавернозном туберкулезе почки.
По словам эндокринологов, обнаружить гипоэхогенное образование надпочечника – задача непростая, и УЗИ, к сожалению, справляется с ней не всегда. Например, верификация диагноза аденомы при первичном альдостеронизме, а также патологической пролиферации клеток коры надпочечников при гиперкортицизме (болезни Иценко-Кушинга) базируется на симптомах. УЗИ безошибочно обнаруживает достаточно крупную феохромоцитому, а также лимфому, карциному и метастазы. Так что, обследовать надпочечники целесообразнее всего с помощью КТ и МРТ.
При развитии доброкачественной лейомиомы, переходно-клеточного рака мочевого пузыря или феохромоцитомы (параганглиомы) мочевого пузыря, которая сопровождается артериальной гипертензией и гематурией, при обследовании на УЗИ визуализируется гипоэхогенное образование в мочевом пузыре.
Патологии, локализованные в брюшной полости, в частности, в кишечном отделе ЖКТ, беспрепятственно исследуются ультразвуком: больной пустой кишечник имеет утолщенные гипоэхогенные стенки, контрастирующие с окружающей гиперэхогенной жировой тканью.
В далеко не полном списке причин, вызывающих визуализируемое при УЗИ гипоэхогенное образование в брюшной полости, значатся:
- грыжа, выпирающая в паховый канал;
- интраабдоминальные гематомы (травматические или связанные с коагулопатиями);
- серозная и гнойная флегмона брюшины или забрюшинного пространства;
- абсцесс терминального отдела подвздошной кишки при трансмуральном илеите (болезни Крона);
- воспаление мезентериальных лимфоузлов (лимфатических узлов брыжейки);
- B-клеточная неходжкинская лимфома или лимфома Беркитта;
- метастазирование в висцеральные лимфатические узлы брюшной полости;
- карцинома слепой кишки и др.
При УЗИ органов малого таза и матки образования с низкой акустической плотностью выявляются у женщин – при наличии миомы, аденомы, кисты или эндометриоза матки; функциональной или дермоидной кист придатков. А гипоэхогенное образование в яичнике бывает при геморрагической кисте, а также тубоовариальном абсцессе (гнойном воспалении в фаллопиевых трубах и яичниках), фолликулярной лимфоме и карциноме.
У мужчин патологиями с таким диагностическим показателем являются рак яичка, лимфоцеле яичка, варикоцеле канатика, а в ходе проведения УЗИ простаты у пациентов с доброкачественной аденомой или раком данной железы визуализируется гипоэхогенное образование предстательной железы.
Выявленное во время УЗИ гипоэхогенное образование в подключичной области может быть признаком:
- доброкачественных новообразований и злокачественных лимфом переднего средостения;
- хронического лимфолейкоза;
- поражений периферических лимфатических узлов метастазами рака щитовидной железы, гортани, пищевода, молочных желе, легких;
- остеосарком торакальной локализации;
- кисты и эхинококкоза легких;
- тимомы или карциномы тимуса (вилочковой железы).
Гипоэхогенность структур в данной области отмечается клиницистами у пациентов с гиперплазией или кистой паращитовидных желез, гиперпаратиреозом или узелковым аденоматозом.
Кроме анатомо-топографической характеристики возникшего образования, ультрасонография выявляет его форму (округлую, овальную, неправильную), размер по ширине (кранио-каудальный) и глубину относительно наружной стенки органа или полости.
По этому параметру основные виды гипоэхогенного образования включают:
- округлое гипоэхогенное образование или гипоэхогенное овальное образование (это различные кисты, варикоцеле, аденомы, опухоли надпочечников метастатической этиологии);
- гипоэхогенное узловое образование (свойственное гемангиомам, узловой билиарной гипертрофии, миомам матки, узелковому аденоматозу и др.);
- гипоэхогенное очаговое образование (характерное для цирроза и очаговой жировой инфильтрации печени, гематом и инфаркта селезенки и т.д.).
В заключении проведенного УЗИ отмечаются особенности контуров изображения:
- гипоэхогенное образование с ровными контурами (кисты, узловая гипертрофия печени, опухоли молочной железы);
- гипоэхогенное образование с неровными контурами (многие опухоли, большинство метастазов);
- гипоэхогенное образование с четким контуром (кисты, аденомы, абсцессы, имеющие на ультразвуковом изображении гиперэхогенный ободок);
- гипоэхогенное образование с нечеткими контурами (кавернозные гемангионы печени, рак щитовидной железы, метастазы в ткани органов любой локализации).
Далее оценивается гомогенность/гетерогенность образования, то есть его внутренняя структура:
- гипоэхогенное однородное образование (карциномы);
- гипоэхогенное неоднородное образование (крупные аденомы, рак печени, диффузные формы карцином и др.);
- гипоэхогенное образование с гиперэхогенными включениями (почечно-клеточный рак, аденома яичника, рак предстательной железы).
В обязательном порядке дается описание состояния окружающих тканей, дистальных акустических эффектов (усиление, ослабление, акустическая тень) и особенность латеральных теней (симметричность, асимметричность, отсутствие).
Кроме того, отмечается наличие/отсутствие васкуляризации (то есть кровеносных сосудов) в образованиях узлового характера с определением таких видов, как: гипоэхогенное образование без кровотока (аваскулярное) и гипоэхогенное образование с кровотоком.
Образования, имеющие кровеносные сосуды, разделяю на:
- гипоэхогенное образование с перинодулярным кровотоком (подтип с перинодулярной, т.е. окружающей узел васкуляризацией);
- гипоэхогенное образование с сочетанным кровотоком (сосуды имеются возле образования и внутри него);
- гипоэхогенное образование с интранодулярным кровотоком (наличие васкуляризации зафиксировано только внутри образования).
Как показывает клиническая практика, гипоэхогенное образование с интранодулярным кровотоком может указывать на его злокачественный характер.
И, наконец, принимается во внимание наличие в структуре образования соединений кальция. И гипоэхогенное образование с кальцинатами (кальцинозом) характерно для инкапсулированного хронического абсцесса печени при амебиазе, рака печени, новообразований в щитовидной и предстательной железе, злокачественных опухолей молочной железы и др.
источник
Первичный рак печени по гистогенезу разделяют на гепатоцеллюлярный рак, исходящий из гепатоцитов, холангиоцеллюлярный рак или холангиокарцинома), исходящий из эпителия желчных протоков, и смешанный гепатохолангиоцеллюлярный рак. Основная доля поражений приходится на гепатоцеллюлярный рак, в то время как холангиоцеллюлярный рак считается относительно редким заболеванием и составляет около 10% всех злокачественных опухолей печени [Parkin et al., 1993].
Ультразвуковая картина при первичном раке печени весьма разнообразна. Обычно первичный рак печени характеризуется наличием объемных образований в печени, одиночных или множественных (узловая форма). Вместе с тем существует диффузная форма первичного рака печени, эхографическое изображение которой в ряде случаев напоминает цирротические изменения органа (надежные критерии дифференциальной диагностики этих заболеваний отсутствуют до настоящего времени).
Выделяют несколько типов ультразвукового изображения узловой формы первичного рака печени [Догра, Рубенс, 2005]:
1) гиперэхогенный, наиболее часто встречающийся;
Наиболее часто первичный рак печени локализуется в правой доле, в толще паренхимы. Поверхностное субкапсульное расположение встречается значительно реже. Размеры и форма первичного рака печени вариабельны. При выявлении достаточно крупных образований (более 4-5 см в диаметре) определяется увеличение размеров печени, сопровождающееся неровностью контуров в месте поражения. Отмечается аномальный ход сосудов и желчных протоков в проекции опухоли, ампутация крупных сосудистых стволов, а в ряде случаев сегментарное либо генерализованное расширение желчных протоков.
Прорастание первичного рака печени в магистральные сосуды органа в итоге приводит к нарушению печеночной гемодинамики: поражение системы воротной вены в 30-68% случаев заканчивается формированием опухоли или тромба в полости сосуда; вовлечение в неопластический процесс печеночных вен и реже нижней полой вены вызывает развитие синдрома Бадда—Киари. Злокачественные новообразования обильно кровоснабжаются. В цветовом, особенно энергетическом, допплеровском режиме может визуализироваться хаотический рисунок сосудистой сети опухоли [Митьков В.В. и др., 1999].
Ультразвуковые признаки узловой формы первичного рака печени отличаются вариабельностью и не являются патогномоничными в дифференциальной диагностике гепатоцеллюлярного рака с холангиоцеллюлярным раком.
Около половины очаговых образований при гепатоцеллюлярном раке (53%) имеют изоэхогенное изображение относительно печеночной паренхимы, при холангиоцеллюлярном раке этот признак наблюдается только у 30% больных. Гиперэхогенная картина опухоли выявлена у 40% больных с холангиокарциномами и только в 13% случаев при печеночноклеточном раке. Эхонегативные участки внутри объемных образований чаще наблюдают при гепатоцеллюлярном раке.
Нечеткость и неровность контуров более характерна для холангиоцеллюлярного рака. Вероятность диагноза холангиоцеллюлярного рака повышается, если наличие опухоли сопровождается внутрипеченочной сегментарной или генерализованной билиарной гипертензией.
Дифференциально-диагностическим признаком первичного рака печени относительно других солидных образований печени может быть эхонегативная окантовка изображений опухоли или отдельных узлов в ней (встречается одинаково часто при гепатоцеллюлярном и холангиоцеллюлярном раках: в 60-70% случаев).
Диффузная форма первичного рака печени при ультразвуковом исследовании может быть представлена 2 вариантами изображений: множественные узлы различного размера и эхогенности во всех отделах печени и крупноочаговая неоднородность печеночной паренхимы смешанной эхогенности, при которой отдельные узлы практически не дифференцируются.
В обоих вариантах печень обычно увеличена, часто с бугристыми контурами. Структура паренхимы неоднородна, по типу множественного очагового либо крупноочагового диффузного поражения. Наблюдаются выраженные нарушения сосудистого рисунка печени. При многоузловом варианте диффузной формы первичного рака печени отмечается деформация и сдавление венозных сосудов органа. Для крупноочагового диффузного поражения печени характерно обеднение сосудистого рисунка, включая крупные ветви воротной и печеночных вен, деформация и ампутация сосудов.
Изменения сосудистой архитектоники печени и хаотический рисунок сосудистой сети опухоли лучше выявляются в цветовом и особенно энергетическом допплеровском режимах. При диффузной форме первичного рака печени часто наблюдается быстрое развитие портальной и билиарной гипертензии, обусловленных выраженными нарушениями структуры печени и ее анатомических образований.
При ультразвуковом исследовании возникают сложности в дифференциальной диагностике злокачественных и доброкачественных опухолей, первичного и вторичного рака, а также злокачественных опухолей и других очаговых поражений печени (абсцесс, альвеококк).
Метастазы — наиболее часто встречаемые злокачественные опухоли печени. Могут быть одиночными и множественными (в 90% случаев). При метастатическом поражении наблюдается деформация контуров, локальное или генерализованное увеличение, очаговая неоднородность структуры печени. Одиночные метастазы приводят к локальному сдавлению и смещению сосудистого рисунка печени. Массивное очаговое поражение вызывает выраженное изменение ангиоархитектоники органа с обеднением сосудистого рисунка. Ультразвуковая картина вторичных опухолей весьма разнообразна и может быть представлена несколькими вариантами.
• Гиперэхогенный (образования с четкими контурами, повышенной эхогенности, чаще неоднородные).
Дифференциальная диагностика с гемангиомами печени, очаговой жировой инфильтрацией и очаговым фиброзом печени, первичным раком печени. Осложненными формами этого варианта эхоскопической картины вторичных опухолей, по мнению В. Догра и Д.Дж. Рубенса (2005), являются метастазы типа «бычий глаз» (гипоэхогенный центр и гиперэхогенная периферия) и «мишень» (гиперэхогенная центральная часть и гипоэхогенная периферия). В ряде публикаций эта разновидность вторичных опухолей выделяется в отдельный вариант ультразвуковой картины [Митьков В.В., Брюховецкий Ю.А, 1996). Дифференциальная диагностика практически со всеми известными очаговыми поражениями печени.
• Изоэхогенный (образования по структуре и эхогенности практически неотличимы от печеночной паренхимы). Дифференциальная диагностика с очаговой узловой гиперплазией печени, ПРП.
Имеют ряд черт, присущих опухолям: отсутствие капсулы, неоднородная внутренняя структура при полипозиционном исследовании с применением соответствующей частоты датчика в режиме двойной гармоники, отсутствие эффекта дистального псевдоусиления тканей, увеличение размеров и количества образований при динамическом исследовании в относительно короткие промежутки времени.
Дифференциальная диагностика с простыми, нагноившимися и малигнизированными кистами, некротизированным первичным раком печени, абсцессами печени, кавернозными гемангиомами, эхинококкозом.
• Смешанной эхогенности или диффузный (образования с неоднородной внутренней структурой, часто плохо дифференцируемые на фоне паренхимы печени, особенно при наличии диффузных изменений органа).
Такие осложнения описторхоза, как кисты, абсцессы и холангиогенные опухоли печени требуют динамического наблюдения либо оперативного лечения.
Существование описторхозных кист, как самостоятельного поражения печени, доказано патоморфологическими исследованиями. Описторхозные кисты развиваются у лиц с массивной и супермассивной степенью инвазии в результате длительной желчной гипертензии. Они представляют собой резко расширенные желчные ходы с сохраненной или частично разрушенной стенкой, окруженной фиброзной тканью. Содержат желчь, слизь, экссудат, яйца описторхов или самих паразитов.
Описторхозные кисты вариабельны по форме, как правило, небольших или средних размеров, чаще множественные. Обычно они расположены в периферических отделах печени, субкапсульно или по ходу портальных трактов с преимущественной локализацией в левой доле, что связано с худшими условиями желчеоттока.
Ультразвуковая картина описторхозных печеночных кист соответствует признакам простых кист: в 95,5% наблюдений это жидкостные образования с однородным анэхогенным содержимым, тонкостенные, с неровными, чаще фестончатыми контурами. В 4,1% случаев в просвете кист отмечались хлопьевидные включения, а в 2,7% наблюдений — единичные внутренние перегородки [Толкаева М.В., 1999].
В дифференциальной диагностике помогают дополнительные ультразвуковые признаки описторхозного поражения, наблюдаемые у 83% пациентов с кистами печени: повышение эхогенности стенок внутрипеченочных желчных протоков и перипортальных тканей, наличие холангиоэктазов в периферических отделах печени, увеличение желчного пузыря с внутриполостными осадочными и хлопьевидными включениями.
Описторхозные абсцессы печени относятся к редким, но наиболее тяжелым по течению и трудным для диагностики осложнениям описторхоза.
По данным Н.А. Бражниковой (1989), в общей структуре хирургических осложнений описторхоза абсцессы составляют 2,56%.
Описторхозные абсцессы обычно развиваются на фоне гнойного холангита, но в ряде случаев возникают как следствие нагноения кист печени или тромбоза сосудов портальной системы.
Существует два типа ультразвукового изображения гнойников при описторхозе [Толкаева М.В., 1999].
• Абсцессы I типа. Располагаются в задних сегментах правой доли печени (S6-S7) и являются следствием локального нарушения дренирования сегмента или субсегмента органа. Представляют собой крупные неоднородные фрагменты печеночной паренхимы повышенной эхогенности без четких границ, от 6,5 до 9,0 см в диаметре, соответствующие зоне воспалительной инфильтрации. Участки деструкции внутри инфильтрата определяются в виде небольших очагов пониженной плотности или жидкостных включений неправильной, иногда древовидной формы с размытыми контурами.
Описторхозные абсцессы I типа при адекватной консервативной терапии не нуждаются в оперативном лечении. Дифференциальная диагностика с пиогенными абсцессами может вызывать затруднения.
• Абсцессы II типа. Имеют холангиогенное происхождение, развиваются на почве холангиоэктазов вследствие желчной гипертензии и гнойного холангита. Представляют собой множественные локально расширенные внутрипеченочные желчные протоки с утолщенными и уплотненными стенками на фоне общего повышения эхогенности ткани печени вследствие ее воспалительной инфильтрации. В просвете холангиоэктазов определяется слабоэхогенное содержимое, обусловленное гноем и детритом.
Для абсцессов II типа характерна множественная локализация в обеих долях печени, небольшие размеры, быстрое развитие печеночной недостаточности. Холангиогенные абсцессы требуют экстренного хирургического вмешательства. Отсутствие своевременного лечения (причиной чего может быть трудность диагностики) приводит к перфорации абсцессов с развитием гнойного перитонита, поддиафрагмальных и подпеченочных абсцессов, забрюшинных флегмон. Описторхозные абсцессы II типа эхоскопически не имеют существенных отличий от холангитических абсцессов непаразитарной этиологии.
Наиболее серьезное осложнение длительно существующего описторхоза — первичный рак печени. В регионах, эндемичных по описторхозу, частота первичного рака печени в 3—9 раз выше, чем на остальных территориях [Шайн А.А., 1972]. Преобладающей формой первичного рака печени при описторхозе является холангиоцеллюлярный рак. Развитие холангиоцеллюлярного рака — многофакторный процесс, при котором паразиты играют роль стимуляторов злокачественного роста.
В зависимости от уровня поражения желчных протоков у больных описторхозом, существует 3 типа эхоскопической картины холангиоцеллюлярного рака печени [Толкаева М.В., 1999].
• Опухоли внутрипеченочной локализации. Развиваются из мелких внутрипеченочных желчных протоков и характеризуются диффузно-инфильтративными изменениями паренхимы периферических отделов печени. Визуализируются в виде фрагментов гиперэхогенной ткани сглаженной структуры, без четких границ, с внутренними мелкими очагами пониженной или повышенной плотности и кальцинатами.
Часто сопровождаются мелкими холангиоэктазами в периферических отделах печени в зоне поражения. Дополнительный признак описторхозной инвазии — выраженные перидуктальные фиброзноинфильтративные изменения тканей, местами с элементами обызвествления. Опухоли внутрипеченочной локализации при описторхозе наиболее трудны для ультразвуковой диагностики в связи с диффузно-инфильтративным характером роста и невозможностью определения истинных границ поражения.
• Опухоли с поражением ворот печени (центральная локализация). Характеризуются наличием в области портальных ворот печени объемного образования небольших размеров (до 3—5 см), без четких контуров, гипер-, изо- или гипоэхогенного относительно печеночной паренхимы. Сопровождаются обструкцией желчных протоков в зоне поражения и расширением проксимальной части внутрипеченочных желчных протоков.
• Опухоли с поражением дистальных желчных протоков. Для холангиоцеллюлярного рака характерно длительное бессимптомное течение заболевания. Сложности визуализации опухолей при ультразвуковом исследовании определяют позднюю диагностику. К моменту постановки диагноза у 85,7% больных имеется метастатическое поражение печени и лимфатических узлов.
Ультразвуковое исследование благодаря своей неинвазивности, информативности и точности получаемой информации является ценнейшим диагностическим методом, дающим возможности в большинстве случаев верифицировать диагноз очагового поражения печени до такой степени достоверности, что использование других диагностических методов становится необязательным. Сочетание ультразвукового метода исследования с допплерографией позволяет выяснить взаимоотношения патологического очага с сосудисто-протоковыми структурами печени и достаточно точно планировать объем и характер предстоящего оперативного вмешательства.
источник
Первичный рак печени по гистогенезу разделяют на гепатоцеллюлярный рак, исходящий из гепатоцитов, холангиоцеллюлярный рак или холангиокарцинома), исходящий из эпителия желчных протоков, и смешанный гепатохолангиоцеллюлярный рак. Основная доля поражений приходится на гепатоцеллюлярный рак, в то время как холангиоцеллюлярный рак считается относительно редким заболеванием и составляет около 10% всех злокачественных опухолей печени [Parkin et al., 1993].
Ультразвуковая картина при первичном раке печени весьма разнообразна. Обычно первичный рак печени характеризуется наличием объемных образований в печени, одиночных или множественных (узловая форма). Вместе с тем существует диффузная форма первичного рака печени, эхографическое изображение которой в ряде случаев напоминает цирротические изменения органа (надежные критерии дифференциальной диагностики этих заболеваний отсутствуют до настоящего времени).
Выделяют несколько типов ультразвукового изображения узловой формы первичного рака печени [Догра, Рубенс, 2005]:
1) гиперэхогенный, наиболее часто встречающийся;
Наиболее часто первичный рак печени локализуется в правой доле, в толще паренхимы. Поверхностное субкапсульное расположение встречается значительно реже. Размеры и форма первичного рака печени вариабельны. При выявлении достаточно крупных образований (более 4-5 см в диаметре) определяется увеличение размеров печени, сопровождающееся неровностью контуров в месте поражения. Отмечается аномальный ход сосудов и желчных протоков в проекции опухоли, ампутация крупных сосудистых стволов, а в ряде случаев сегментарное либо генерализованное расширение желчных протоков.
Прорастание первичного рака печени в магистральные сосуды органа в итоге приводит к нарушению печеночной гемодинамики: поражение системы воротной вены в 30-68% случаев заканчивается формированием опухоли или тромба в полости сосуда; вовлечение в неопластический процесс печеночных вен и реже нижней полой вены вызывает развитие синдрома Бадда—Киари. Злокачественные новообразования обильно кровоснабжаются. В цветовом, особенно энергетическом, допплеровском режиме может визуализироваться хаотический рисунок сосудистой сети опухоли [Митьков В.В. и др., 1999].
Ультразвуковые признаки узловой формы первичного рака печени отличаются вариабельностью и не являются патогномоничными в дифференциальной диагностике гепатоцеллюлярного рака с холангиоцеллюлярным раком.
Около половины очаговых образований при гепатоцеллюлярном раке (53%) имеют изоэхогенное изображение относительно печеночной паренхимы, при холангиоцеллюлярном раке этот признак наблюдается только у 30% больных. Гиперэхогенная картина опухоли выявлена у 40% больных с холангиокарциномами и только в 13% случаев при печеночноклеточном раке. Эхонегативные участки внутри объемных образований чаще наблюдают при гепатоцеллюлярном раке.
Нечеткость и неровность контуров более характерна для холангиоцеллюлярного рака. Вероятность диагноза холангиоцеллюлярного рака повышается, если наличие опухоли сопровождается внутрипеченочной сегментарной или генерализованной билиарной гипертензией.
Дифференциально-диагностическим признаком первичного рака печени относительно других солидных образований печени может быть эхонегативная окантовка изображений опухоли или отдельных узлов в ней (встречается одинаково часто при гепатоцеллюлярном и холангиоцеллюлярном раках: в 60-70% случаев).
Диффузная форма первичного рака печени при ультразвуковом исследовании может быть представлена 2 вариантами изображений: множественные узлы различного размера и эхогенности во всех отделах печени и крупноочаговая неоднородность печеночной паренхимы смешанной эхогенности, при которой отдельные узлы практически не дифференцируются.
В обоих вариантах печень обычно увеличена, часто с бугристыми контурами. Структура паренхимы неоднородна, по типу множественного очагового либо крупноочагового диффузного поражения. Наблюдаются выраженные нарушения сосудистого рисунка печени. При многоузловом варианте диффузной формы первичного рака печени отмечается деформация и сдавление венозных сосудов органа. Для крупноочагового диффузного поражения печени характерно обеднение сосудистого рисунка, включая крупные ветви воротной и печеночных вен, деформация и ампутация сосудов.
Изменения сосудистой архитектоники печени и хаотический рисунок сосудистой сети опухоли лучше выявляются в цветовом и особенно энергетическом допплеровском режимах. При диффузной форме первичного рака печени часто наблюдается быстрое развитие портальной и билиарной гипертензии, обусловленных выраженными нарушениями структуры печени и ее анатомических образований.
При ультразвуковом исследовании возникают сложности в дифференциальной диагностике злокачественных и доброкачественных опухолей, первичного и вторичного рака, а также злокачественных опухолей и других очаговых поражений печени (абсцесс, альвеококк).
Метастазы — наиболее часто встречаемые злокачественные опухоли печени. Могут быть одиночными и множественными (в 90% случаев). При метастатическом поражении наблюдается деформация контуров, локальное или генерализованное увеличение, очаговая неоднородность структуры печени. Одиночные метастазы приводят к локальному сдавлению и смещению сосудистого рисунка печени. Массивное очаговое поражение вызывает выраженное изменение ангиоархитектоники органа с обеднением сосудистого рисунка. Ультразвуковая картина вторичных опухолей весьма разнообразна и может быть представлена несколькими вариантами.
• Гиперэхогенный (образования с четкими контурами, повышенной эхогенности, чаще неоднородные).
Дифференциальная диагностика с гемангиомами печени, очаговой жировой инфильтрацией и очаговым фиброзом печени, первичным раком печени. Осложненными формами этого варианта эхоскопической картины вторичных опухолей, по мнению В. Догра и Д.Дж. Рубенса (2005), являются метастазы типа «бычий глаз» (гипоэхогенный центр и гиперэхогенная периферия) и «мишень» (гиперэхогенная центральная часть и гипоэхогенная периферия). В ряде публикаций эта разновидность вторичных опухолей выделяется в отдельный вариант ультразвуковой картины [Митьков В.В., Брюховецкий Ю.А, 1996). Дифференциальная диагностика практически со всеми известными очаговыми поражениями печени.
• Изоэхогенный (образования по структуре и эхогенности практически неотличимы от печеночной паренхимы). Дифференциальная диагностика с очаговой узловой гиперплазией печени, ПРП.
Имеют ряд черт, присущих опухолям: отсутствие капсулы, неоднородная внутренняя структура при полипозиционном исследовании с применением соответствующей частоты датчика в режиме двойной гармоники, отсутствие эффекта дистального псевдоусиления тканей, увеличение размеров и количества образований при динамическом исследовании в относительно короткие промежутки времени.
Дифференциальная диагностика с простыми, нагноившимися и малигнизированными кистами, некротизированным первичным раком печени, абсцессами печени, кавернозными гемангиомами, эхинококкозом.
• Смешанной эхогенности или диффузный (образования с неоднородной внутренней структурой, часто плохо дифференцируемые на фоне паренхимы печени, особенно при наличии диффузных изменений органа).
Такие осложнения описторхоза, как кисты, абсцессы и холангиогенные опухоли печени требуют динамического наблюдения либо оперативного лечения.
Существование описторхозных кист, как самостоятельного поражения печени, доказано патоморфологическими исследованиями. Описторхозные кисты развиваются у лиц с массивной и супермассивной степенью инвазии в результате длительной желчной гипертензии. Они представляют собой резко расширенные желчные ходы с сохраненной или частично разрушенной стенкой, окруженной фиброзной тканью. Содержат желчь, слизь, экссудат, яйца описторхов или самих паразитов.
Описторхозные кисты вариабельны по форме, как правило, небольших или средних размеров, чаще множественные. Обычно они расположены в периферических отделах печени, субкапсульно или по ходу портальных трактов с преимущественной локализацией в левой доле, что связано с худшими условиями желчеоттока.
Ультразвуковая картина описторхозных печеночных кист соответствует признакам простых кист: в 95,5% наблюдений это жидкостные образования с однородным анэхогенным содержимым, тонкостенные, с неровными, чаще фестончатыми контурами. В 4,1% случаев в просвете кист отмечались хлопьевидные включения, а в 2,7% наблюдений — единичные внутренние перегородки [Толкаева М.В., 1999].
В дифференциальной диагностике помогают дополнительные ультразвуковые признаки описторхозного поражения, наблюдаемые у 83% пациентов с кистами печени: повышение эхогенности стенок внутрипеченочных желчных протоков и перипортальных тканей, наличие холангиоэктазов в периферических отделах печени, увеличение желчного пузыря с внутриполостными осадочными и хлопьевидными включениями.
Описторхозные абсцессы печени относятся к редким, но наиболее тяжелым по течению и трудным для диагностики осложнениям описторхоза.
По данным Н.А. Бражниковой (1989), в общей структуре хирургических осложнений описторхоза абсцессы составляют 2,56%.
Описторхозные абсцессы обычно развиваются на фоне гнойного холангита, но в ряде случаев возникают как следствие нагноения кист печени или тромбоза сосудов портальной системы.
Существует два типа ультразвукового изображения гнойников при описторхозе [Толкаева М.В., 1999].
• Абсцессы I типа. Располагаются в задних сегментах правой доли печени (S6-S7) и являются следствием локального нарушения дренирования сегмента или субсегмента органа. Представляют собой крупные неоднородные фрагменты печеночной паренхимы повышенной эхогенности без четких границ, от 6,5 до 9,0 см в диаметре, соответствующие зоне воспалительной инфильтрации. Участки деструкции внутри инфильтрата определяются в виде небольших очагов пониженной плотности или жидкостных включений неправильной, иногда древовидной формы с размытыми контурами.
Описторхозные абсцессы I типа при адекватной консервативной терапии не нуждаются в оперативном лечении. Дифференциальная диагностика с пиогенными абсцессами может вызывать затруднения.
• Абсцессы II типа. Имеют холангиогенное происхождение, развиваются на почве холангиоэктазов вследствие желчной гипертензии и гнойного холангита. Представляют собой множественные локально расширенные внутрипеченочные желчные протоки с утолщенными и уплотненными стенками на фоне общего повышения эхогенности ткани печени вследствие ее воспалительной инфильтрации. В просвете холангиоэктазов определяется слабоэхогенное содержимое, обусловленное гноем и детритом.
Для абсцессов II типа характерна множественная локализация в обеих долях печени, небольшие размеры, быстрое развитие печеночной недостаточности. Холангиогенные абсцессы требуют экстренного хирургического вмешательства. Отсутствие своевременного лечения (причиной чего может быть трудность диагностики) приводит к перфорации абсцессов с развитием гнойного перитонита, поддиафрагмальных и подпеченочных абсцессов, забрюшинных флегмон. Описторхозные абсцессы II типа эхоскопически не имеют существенных отличий от холангитических абсцессов непаразитарной этиологии.
Наиболее серьезное осложнение длительно существующего описторхоза — первичный рак печени. В регионах, эндемичных по описторхозу, частота первичного рака печени в 3—9 раз выше, чем на остальных территориях [Шайн А.А., 1972]. Преобладающей формой первичного рака печени при описторхозе является холангиоцеллюлярный рак. Развитие холангиоцеллюлярного рака — многофакторный процесс, при котором паразиты играют роль стимуляторов злокачественного роста.
В зависимости от уровня поражения желчных протоков у больных описторхозом, существует 3 типа эхоскопической картины холангиоцеллюлярного рака печени [Толкаева М.В., 1999].
• Опухоли внутрипеченочной локализации. Развиваются из мелких внутрипеченочных желчных протоков и характеризуются диффузно-инфильтративными изменениями паренхимы периферических отделов печени. Визуализируются в виде фрагментов гиперэхогенной ткани сглаженной структуры, без четких границ, с внутренними мелкими очагами пониженной или повышенной плотности и кальцинатами.
Часто сопровождаются мелкими холангиоэктазами в периферических отделах печени в зоне поражения. Дополнительный признак описторхозной инвазии — выраженные перидуктальные фиброзноинфильтративные изменения тканей, местами с элементами обызвествления. Опухоли внутрипеченочной локализации при описторхозе наиболее трудны для ультразвуковой диагностики в связи с диффузно-инфильтративным характером роста и невозможностью определения истинных границ поражения.
• Опухоли с поражением ворот печени (центральная локализация). Характеризуются наличием в области портальных ворот печени объемного образования небольших размеров (до 3—5 см), без четких контуров, гипер-, изо- или гипоэхогенного относительно печеночной паренхимы. Сопровождаются обструкцией желчных протоков в зоне поражения и расширением проксимальной части внутрипеченочных желчных протоков.
• Опухоли с поражением дистальных желчных протоков. Для холангиоцеллюлярного рака характерно длительное бессимптомное течение заболевания. Сложности визуализации опухолей при ультразвуковом исследовании определяют позднюю диагностику. К моменту постановки диагноза у 85,7% больных имеется метастатическое поражение печени и лимфатических узлов.
Ультразвуковое исследование благодаря своей неинвазивности, информативности и точности получаемой информации является ценнейшим диагностическим методом, дающим возможности в большинстве случаев верифицировать диагноз очагового поражения печени до такой степени достоверности, что использование других диагностических методов становится необязательным. Сочетание ультразвукового метода исследования с допплерографией позволяет выяснить взаимоотношения патологического очага с сосудисто-протоковыми структурами печени и достаточно точно планировать объем и характер предстоящего оперативного вмешательства.
источник