Воротная вена печени — крупный сосуд, который отвечает за транспорт крови в организме. При возникновении патологий происходят нарушения в его функционировании, а также в работе других, расположенных рядом, вен. У пациента может развиться портальная гипертензия, тромбоз, гнойные воспаления и кавернозная трансформация.
Диагностику состояния воротной вены печени проводят с помощью УЗИ и других инструментальных методов. Прогноз заболеваний зависит от стадии их развития. При появлении первых симптомов патологии необходимо обратиться к терапевту за помощью.
Воротная вена печени — крупный сосудистый ствол. Сосуд образуется соединением верхней и нижней брыжеечных и селезеночных вен.
Воротная вена представляет собой толстый ствол, который входит в печень. Благодаря толстой стенке сосуд может выдержать давление в несколько раз больше нормальных показателей.
В анатомии человека она формирует дополнительный круг венозного кровообращения, который выполняет функцию очищения плазмы крови от токсинов. Ее значение в организме связано с тем, что она собирает кровь от органов живота. В печень, кроме артерии, входит венозный сосуд, кровь из которого поступает в печеночные вены, проходя через ткань органа.
У некоторых людей нижняя брыжеечная вена попадает в селезеночную, а соединение селезеночной и верхней брыжеечной образует ствол воротной.
В норме размеры воротной вены печени составляют: протяженность — 6-8 см, а диаметр — до 1,5 см.
В схеме кровообращения портальную систему образуют крупные стволы вен, сливающихся между собой. Брыжеечные вены выполняют функцию транспорта крови от кишечника, а селезеночная принимает ее из вен желудка и поджелудочной железы. В воротах печени происходит разделение на правую и левую ветви воротной вены, которые дальше распадаются на мелкие венозные сосуды. Достигая печеночной дольки, они оплетают ее снаружи и входят внутрь.
Выделяют четыре вида патологий воротной вены:
- тромбоз;
- портальная гипертензия;
- кавернозная трансформация;
- гнойный воспалительный процесс.
Тромбоз (пилетромбоз) представляет собой формирование тромба в печеночных венах до полной закупорки просвета сосуда. Патология имеет прогрессирующее течение.
При тромбозе воротной вены у больных, по результатам УЗИ, диаметр сосуда увеличивается до 13 мм.
У детей эта патология связана с попаданием инфекции в пуповину. В более старшем возрасте ее развитие связано с острым аппендицитом. У взрослых людей в 50% случаев причина возникновения тромбоза воротной вены остается не установленной.
К факторам развития заболевания относятся:
- операции на брюшине;
- травмы стенок вены;
- опухоли панкреаса;
- цирроз;
- инфекционные поражения;
- сердечная недостаточность;
- многоплодная беременность;
- осложнения беременности и родов.
По локализации выделяют несколько видов тромбов:
| Вид | Характеристика |
| Корешковый | Формируется в вене желудка, селезенки и проникает в воротную вену |
| Трункулярный | Развивается в стволе вены |
| Внутрипеченочный | Формируется внутри печени |
Выделяют острый и хронический пилетромбоз. Первая форма развивается резко, встречается редко и влечет за собой летальный исход в течение двух дней на фоне отмирания клеток желудка, поджелудочной железы, кишечника, печени и селезенки. Хронический протекает медленно, характеризуется частичным перекрытием просвета сосуда.
При острой форме больные жалуются на резкие и неожиданные боли в области живота. Отмечается вздутие живота на фоне асцита (накопления жидкости в брюшной полости). Нередко происходит расширение подкожной венозной сети.
У больных постоянно появляется рвота со сгустками крови. Наблюдается открытие кровотечения из прямой кишки и желтуха. Развивается отечность ног.
При хронической форме наблюдается чувство слабости, потеря веса, снижение аппетита или его отсутствие и боли в животе. Иногда встречается подъем температуры тела, повышение количества лейкоцитов в крови, при этом печень увеличена.
Пилетромбоз имеет четыре стадии развития:
| Стадия | Проявления |
| Первая | Поражение затрагивает не более половины сосуда, а сгусток крови находится выше зоны перехода воротной вены в селезеночную |
| Вторая | Тромб доходит до верхней брыжеечной вены |
| Третья | Происходит поражение всех вен брюшины, а отток крови сохраняется частично |
| Четвертая | Развивается поражение с отсутствием кровотока |
Возможные осложнения заболевания:
- кишечное и желудочное кровотечение;
- перитонит (воспаление в брюшной полости).
Заболевание развивается на фоне нарушения оттока крови и повышения давления в бассейне воротной вены. Основной причиной развития этого патологического состояния является повреждение печени при гепатитах, циррозе и опухолях органа. Иногда это заболевание возникает при отравлении лекарствами, грибами, различными ядами. У лиц, страдающих этой патологией, давление повышается до 250-600 мм вод. ст.
К развитию портальной гипертензии приводят:
- тромбоз;
- цирроз;
- операции;
- травмы;
- ожоги;
- воспалительная реакция на инфекционную патологию;
- алкогольная зависимость;
- геморрагии;
- прием транквилизаторов и диуретиков.
Развитие данного заболевания врачи связывают с формированием механического барьера, препятствующего нормальному току крови. Объем крови, который проходит через печень, уменьшается в 4-5 раз.
Выделяют тотальную и сегментарную портальную гипертензию. При первой форме происходит поражение всей сосудистой сети, а при второй отмечается нарушение кровотока в селезеночной вене при сохранении нормального тока крови и давления в воротной и брыжеечной.
Существует четыре стадии заболевания:
| Стадия | Признаки |
| Первая (начальная) | Появляются сбои в работе органов и систем |
| Вторая (компенсированная) | Отмечается небольшое увеличение селезенки и расширение вен пищевода. Асцит отсутствует |
| Третья (декомпенсированная) | Наблюдается спленомегалия и асцит. Появляются кровотечения |
| Четвертая | Развивается печеночная недостаточность, перитонит. Открываются кровотечения из вен пищевода, желудка и прямой кишки |
Изначально пациенты начинают жаловаться на метеоризм, проблемы со стулом и тошноту. Происходит ухудшение аппетита, возникают боли в животе и правом подреберье. Появляются слабость и быстрая утомляемость, снижается концентрация внимания. Нередко развивается желтуха, сопровождаемая пожелтением кожных покровов и склер. Происходит потеря веса.
Первым признаком развития этой болезни может являться спленомегалия (увеличение селезенки). При асците происходит увеличение объемов живота, отеки лодыжек. Геморрагии обильные и развиваются внезапно на фоне поражения слизистой, увеличения внутрибрюшного давления, нарушения свертываемости крови. Если у больного открывается кровотечение из пищевода и желудка, то появляется кровавая рвота.
У пациента возможно появление кавернозной трансформации. Она характеризуется наличием большого количества переплетающихся сосудов, которые частично возмещают дефект кровообращения в портальной системе.
источник
Для УЗИ печени используют конвексный датчик 3,5-7 МГц. Исследование проводят натощак.
Нажимайте на картинки, чтобы увеличить.
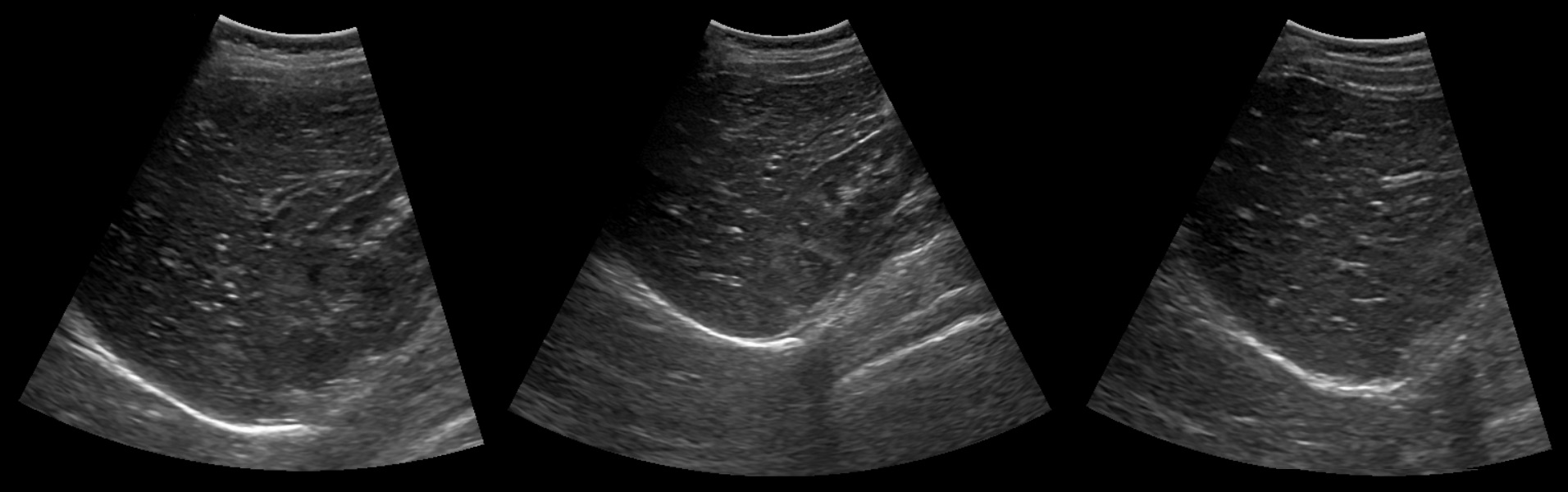
Рисунок. Если изображение нечеткое (1), добавьте гель. На идеальной картинке видно стенки сосудов и диафрагму — яркая изогнутая линия (2). Осмотрите край печени и 3 см за пределами, иначе можно пропустить опухоль (3).
На УЗИ печени нас интересует размер, эхогенность и эхоструктура. Как оценить размер печени смотри Размеры печени и желчного пузыря на УЗИ (лекция на Диагностере).
Эхогенность — это способность тканей отражать ультразвук. На УЗИ самые светлые оттенки серого у более плотных структур.
Рисунок. Градиент эхогенности паренхиматозных органов: пирамидки почек (ПП) наименее эхоплотные; в ряду кора почек (КП) ⇒ печень (П) ⇒ поджелудочная железа (ПЖ) ⇒ селезенка (С) эхоплотность нарастает; синусы почек (СП) и жир самые эхоплотные. Иногда кора почек и печень, поджелудочная железа и печень изоэхогенные.
Рисунок. Поджелудочная железа гиперэхогенная в сравнении с печенью, а печень гипоэхогенная в сравнении с поджелудочной железой (1). Кора почек и печень изоэхогенные, а синус почки и жир гиперэхогенные (2). Селезенка гиперэхогенная относительно печени, а печень гипоэхогенная относительно селезенке (3).
Эхоструктура — это те элементы, которые мы можем различить на эхограмме. Сосудистый рисунок печени представлен воротными и печеночными венами. Общую печеночную артерию и общий желчный проток можно увидеть в воротах печени. В паренхиме видно только патологически расширенные печеночные артерии и желчные протоки.
Рисунок. В воротах печени желчный проток, воротная вена и печеночная артерия тесно прилегают друг к другу, образуя печеночную триаду. В паренхиме печени эти структуры продолжают совместный ход. По печеночным венам кровь из печени отходит в нижнюю полую вену.
Риунок. На УЗИ нормальная печень ребенка 4-х лет (1) и новорожденного (2, 3). Маленькие отверстия в паренхиме — это сосуды. Ветви воротной вены с яркой гиперэхогенной стенкой, а печеночные вены без.
- Кровоток в воротных венах направлен К печени — гепатопетальный.
- В воротах печени главная воротная вена делится на правую и левую ветви, которые ориентированы горизонтально.
- Воротная вена, желчный проток и печеночная артерия окружены глиссоновой капсулой, поэтому стенка воротных вен повышенной эхоплотности.
Рисунок. В воротной вене кровоток направлен К УЗ-датчику — при ЦДК красный цвет и спектр выше изолинии (1). Ствол воротной вены, общий желчный проток и общую печеночную артерию можно увидеть в воротах печени — «голова Микки Мауса» (2, 3).
- Кровоток в печеночных венах направлен ОТ печени — гепатофугальный.
- Печеночные вены ориентированы почти вертикально и сходятся у нижней полой вены.
- Печеночные вены отделяют сегменты печени.
Рисунок. В печеночных венах кровоток направлен ОТ УЗ-датчика — при ЦДК синий цвет, сложная форма спектра отражает изменение давления в правом предсердии во все фазы сердечного цикла (1). В срезах через верхушку печени видно, как правая, средняя и левая печеночные вены впадают в нижнюю полую вену (2). Стенки печеночных вен гиперэхогенна, только в положении под 90° к УЗ-лучу (3).
Типы эхоструктуры печени: нормальная, центролобулярная, фиброзно-жировая.
Печень бывает отечная при остром вирусном гепатите, острой правожелудочковой недостаточности, синдроме токсического шока, лейкозах, лимфоме и т.д. На УЗИ эхоструктура центролобулярная: на фоне паренхимы пониженной эхоплотности диафрагма очень яркая, сосудистый рисунок усилен. Стенки мелких воротных вен сияют — «звездное небо». Центролобулярная печень встречается у 2% здоровых людей, чаще у молодых.
Рисунок. Здоровая девочка 5-ти лет. До беременности мама болела гепатитом С. У девочки анализ на гепатит С отрицательный. На УЗИ паренхима печени пониженной эхоплотности, сосудистый рисунок усилен — симптом «звездного неба». Заключение: Центролобулярная печень (вариант нормы).
Рисунок. Мальчик 13-ти лет заболел остро: подъем температуры до 38,5°С, ломота, частая рвота в течение суток; на момент осмотра сохраняется тошнота, под давлением датчика боль в эпигастрии. На УЗИ печень пониженной эхогенности, сосудистый рисунок усилен — стенки воротных вен «сияют». Заключение: Реактивные изменения печени на фоне кишечной инфекции.
Жир замещает нормальную ткань печени при ожирении, диабете, хроническом гепатите и т.д. На УЗИ диффузные изменения по типу жирового гепатоза: печень увеличена, паренхима повышенной эхоплотности, диафрагма часто не просматривается; сосудистый рисунок бедный — стенки мелких воротных вен почти не видно.
Рисунок. На УЗИ размеры печени увеличены, на фоне резко повышенной эхогенности сосудистый рисунок практически отсутствует (1). Ненормальную эхоплотность печени особенно хорошо видно в сравнении с поджелудочной железой (2) и селезенкой (3). Заключение: Диффузные изменения печени по типу жирового гепатоза.
Кровь от плаценты по пупочной вене входит в тело плода. Малая часть поступает в воротную вену, а основая — по венозному протоку в нижнюю полую вену. У ребенка увидеть пупочную вену можно сразу после рождения, затем ненужная спадается. В передней части левой продольной борозды печени залегает облитерированная пупочная вена или круглая связка, а в задней части — облитерированный венозный проток или венозная связка. Связки окружены жиром, поэтому на УЗИ гиперэхогенные.
Рисунок. На УЗИ в передне-нижнем отделе печени видно круглую связку. В поперечном срезе (1, 2) гиперэхогенный треугольник разделяет латеральный и парамедиальный сектор левой доли (смотри Сегменты печени на УЗИ). Когда круглая связка в положении под 90° к УЗ-лучу, позади акустическая тень (1). Слегка измените угол, у настоящего кальцификата тень не исчезнет. В продольном срезе (3) облитерированная пупочная вена, она же круглая связка, входит в пупочный сегмент левой воротной вены.
Рисунок. На УЗИ венозную связку видно в задне-нижнем отделе печени. В продольном срезе облитерированный венозный проток тянется от нижней полой вены к воротам печени, где общая печеночная артерия, ствол воротной вены и общий желчный проток. Кзади от венозной связки хвостатая доля, а кпереди левая доля печени. В поперечном срезе гиперэхогенная линия от нижней полой вены к пупочному сегменту воротной вены отделяет хвостатую долю от левой доли печени. Пупочный сегмент левой воротной вены — это единственное место в портальной системе с резким поворотом вперед.
При портальной гипертензии пупочная вена реканализуется, а венозный проток нет. Крайне редко его можно увидеть у новорожденных, которым установлен пупочный катетер.
Хвостатая доля печени — это функционально автономный сегмент. Кровь поступает от обеих, правой и левой, воротных вен, а так же имеется прямой венозный дренаж в нижнюю полую вену. При заболеваниях печени хвостатая доля поражается менее других областей и компенсаторно увеличивается. Подробнее смотри здесь.
Рисунок. На УЗИ видно веточка от правой воротной вены подходит к хвостатой доле (2, 3).
Рисунок. У пациента с ожирением на УЗИ печень увеличена, паренхима повышенной эхогенности, сосудистый рисунок бедный — стенки мелких воротных вен не видно; хвостатая доля увеличена, эхоструктура близка к нормальной. Заключение: Размер печени увеличен. Диффузные изменения по типу жирового гепатоза; компенсаторная гипертрофия хвостатой доли.
Рисунок. Когда УЗ-луч проходит через плотные структуры ворот печени, из-за затухания сигнала мы видим гипоэхогенную зону на месте хвостатой доли (1). Переместите датчик и посмотрите под другим углом, псевдоопухоль исчезнет. На УЗИ вблизи головки поджелудочной железы определяется образование изоэхогенное печени (2, 3). При смене положения датчика видно, что это длинный отросток хвостатой доли. При таком варианте строения часто ошибочно диагностируют опухоль или лимфаденит.
Для хирургов важно четко понимать, где находится патологический очаг. Определить сегмент печени на УЗИ легко, если различать анатомические ориентиры:
- в верхнем отделе — нижняя полая вена, правая, средняя и левая печеночные вены;
- в центральном отделе — нижняя полая вена, горизонтально расположенные воротные вены и венозная связка;
- в нижнем отделе — нижняя полая вена, круглая и венозная связка печени.
Берегите себя, Ваш Диагностер!
источник
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Воротная вена образуется из слияния верхней брыжеечной вены и селезеночной вены. Последняя отходит от ворот селезенки и идет вдоль заднего края поджелудочной железы, сопровождая одноименную артерию. Картина внутрипеченочного ветвления и печеночных вен определяется сегментарным строением печени. Анатомическая диаграмма показывает вид печени спереди. MP-ангиография в корональной плоскости является альтернативной методикой визуализации системы воротной вены.
Внепеченочные сегменты визуализируются на расширенном межреберном изображении. Если данная методика оказывается безуспешной вследствие наложения газа в толстой кишке или неприемлемого допплеровского угла, внепеченочные ветви воротной вены можно сканировать из правого переднего межреберного доступа с поднятой правой рукой, что позволяет увеличить межреберные промежутки. Зачастую основной перипортальный ствол визуализируется лишь в этой плоскости вследствие того, что акустическое окно, обусловленное печенью, является наилучшим. Ход внутрипеченочных ветвей таков, что лучше всего они визуализируются на подреберном косом скане. После проведения сканирования в В- и цветовом режимах для количественной оценки перипортального кровотока в воротной вене записываются допплеровские спектры.
Ультразвуковая допплерография воротной вены показывает постоянный приток крови к печени, дающий однофазный допплеровский спектр в виде полосы. Изменяя положение тела и режим дыхания, можно управлять кровотоком. Скорость кровотока в воротной вене, например, значительно уменьшается в сидячем положении и на полном вдохе.
Ультразвуковая допплерография в диагностике патологических изменений воротной вены при различных заболеваниях
Цветовой режим при портальной гипертензии демонстрирует снижение кровотока или даже значительные изменении, такие, как кропоток от печени по воротной вене или селезеночной вене и помогает визуализировать коллатерали.
Тромбоз воротной вены приводит к увеличению сопротивления в системе циркуляции воротной вены. Он может быть результатом цирроза, опухолевой инвазии, повышения свертываемости крови или воспаления. Кровоток в основной печеночной артерии усиливается, чтобы компенсировать дефицит кислорода, вызванный нарушением перфузии по воротной вене. По ходу затромбированной воротной вены может отмечаться кавернозная трансформация, приводящая к возникновению гепатопетального кровотока.
Косвенные признаки портальной гипертензии по ультразвуковой допплерографии
- Уменьшение скорости кровотока менее 10 см/с
- Тромбоз
- Кавернозная трансформация воротной вены
Прямые признаки портальной гипертензии по ультразвуковой допплерографии
- Портокавальные анастомозы
- Кровоток от печени
Чрезъяремный внутрипеченочный портосистемный шунт
Установка чрезъяремного внутрипеченочного портосистемного шунта стала первичным методом декомпрессии системыворотной вены. Катетер вводится через внутреннюю яремную вену в правую печеночную вену и затем через ткань печени — в перипортальный сегмент воротной вены. Это сообщение держится в открытом состоянии благодаря металлическому стенту. Одним из результатов этой процедуры является компенсаторное усиление кровотока в общей печеночной артерии. Рецидивный стеноз стента или окклюзия его являются частыми осложнениями и требуют повторного вмешательства.
Ультразвуковая допплерография, особенно в энергетическом режиме, играет важную роль в контроле после осуществления интервенционной процедуры.
Ультразвуковая допплерография помогает в дифференциальной диагностике неопределенных сосудистых и солидных образований печени. Аденомы, очаговая узловая гиперплазия и гемангиомы можно отличить от злокачественных опухолей по характерным признакам. Отсутствие кровотока в гиперэхогенном гомогенном образовании позволяет заподозрить гемангиому. Этот диагноз можно уточнить, определив дополнительные характеристики кровотока при использовании контрастных веществ.
Применение контрастных веществ
В последние годы использование допплеровского и энергетического допплеровского режимов улучшило дифференциальную диагностику внутрипеченочных образований по сравнению с традиционным В-режимом, однако даже у опытных специалистов до сих пор могут возникать проблемы.
Во-первых, некоторые глубоко расположенные образования печени, а также образования у очень полных людей можно визуализировать лишь с неприемлемым допплеровским углом, что ограничивает точность исследования. Во-вторых, очень медленный кровоток, который часто наблюдается, особенно при небольших опухолях, дает неадекватные частотные сдвиги. В-третьих, в некоторых участках печени очень сложно избежать артефактов от движения вследствие передачи сердечных сокращений на паренхиму печени.
Ультразвуковые контрастные вещества в сочетании с модифицированной методикой сканирования позволяют помочь в решении данных проблем. Они значительно усиливают внутрисосудистый сигнал, улучшая выявление даже медленного кровотока в мелких опухолевых сосудах.
При болюсном введении контрастных препаратов в картине усиления выделяют несколько фаз. Они могут в какой-то степени варьировать в зависимости от индивидуальных особенностей кровообращения у пациента.
Фазы усиления после внутривенного введения контрастного препарата
- Ранняя артериальная: 15-25 с после введения
- Артериальная: 20-30 с после введения
- Воротная: 40-100 с после введени
- Поздняя венозная: 110-180 с после введения
Доброкачественные образования печени: очаговая узловая гиперплазия и аденома
Доброкачественные образования печени, в отличие от злокачественных, не содержат патологических шунтов. В результате они остаются усиленными даже в позднюю венозную фазу. Это характерно для очаговой узловой гиперплазии и гемангиомы. Очаговая узловая гиперплазия чаще поражает женщин, постоянно применяющих оральные контрацептивы Аденомы печени имеют практически идентичную картину в В-режиме, и дифференцировка часто требует гистологической оценки. При использовании цветового и энергетического допплеровских режимов при очаговой узловатой гиперплазии определяется типичная картина кровотока, что позволяет провести дифференциальную диагностику.
Сосудистое сплетение при очаговой узловатьй гиперплазии расходится рааиаиыю от центральной артерии, демонстрируя центрифугальныи кров ток с образованием симптома «спиц колеса». Очаговая узловая гиперплазия и аденома могут характеризоваться схожей симптоматикой вследствие увеличения за счет роста или кровотечения. При КТ очаговая узловая гиперплазия и аденомы наиболее четко определяются в раннюю артериальную фазу усиления. В паренхимальную фазу они гипер- или изоэхогенны по отношению к окружающей ткани печени.
В отличие от очаговой узловатой гиперплазии, гемангиомы кровоснабжаются от периферии к центру. В артериальную фазу наружные области образования усиливаются, тогда как центр остается гипоэхогенным. Центральная часть становится значительно более эхогенной в последующую воротную фазу, а все образование приобретает гиперэхогенный характер в позднюю венозную фазу. Эта картина усиления от периферии к центру, также называемая симптомом «диафрагмы радужки», типична для гемангиом печени. Она также определяется при КТ.
Выявление при ультразвуковой допплерографии внутри- и околоопухолевых артериальных допплерипскнх сигналов, обрывов сосудов, сосудистой инвазии, спиральных конфигураций и увеличение количества артериовенозных шунтоэ рассматриваются, как критерии злокачественности. Гепатоцеллюлярный рак обычно имеет гетерогенную картину усиления сигнала в артериальную фазу после введения контрастного препарата. Он остается гиперэхогенным в воротную фазу и принимает изоэхогенный характер по отношению к нормальной паренхиме печени в позднюю венозную фазу.
Метастазы в печень могут быть гипо- или гиперваскулярными. Хотя точное расположение первичной опухоли по сосудистой картине печеночного метастаза определить невозможно, было обнаружено, что для некоторых первичных опухолей характерна определенная степень васкуляризации. Нейроэндокринные опухоли, такие, как С-клеточный рак щитовидной железы или карциноид, имеют тенденцию к образованию гиперваскулярных метастазов, тогда как метастазы первичных колоректальных опухолей обычно гиповаскулярны.
В артериальную фазу после введения контрастного препарата при стандартной методике сканирования метастазы характеризуются небольшим контрастным усилением в зависимости от степени васкуляризации. Они обычно остаются гипоэхогенными по отношению к паренхиме печени в позднюю венозную фазу или могут становиться изоэхогенными. Эта низкая эхогенность в позднюю венозную фазу после введения контрастного препарата является ключевым критерием дифференциальной диагностики метастазов от вышеописанных доброкачественных образований печени Что из этого вытекает? Отличительной характеристикой метастазов является их тенденция к формированию артериовенозных шунтов. Это может объяснить, почему контрастные препараты быстрее выводятся из печеночных метастазов, чем из нормальной паренхимы печени, именно поэтому в позднюю фазу контрастной перфузии картина метастазов относительно гипоэхогенна.
Типичными признаками печеночных метастазов являются неравномерная картина усиления, спиралеобразная или штопорообразная конфигурация сосудов и наличие большого числа артериовенозных шунтов. Вследствие последнего аспекта попадание контрастного вещества в печеночные вены происходит в течение 20 секунд вместо 40 секунд в норме. Помочь в дифференциальной диагностике между гепатоцеллюлярным раком и метастазами может и клиническая картина: больные гепатоцеллюлярным раком часто страдают от цирроза печени, хронического гепатита и/или имеют повышенный уровень альфа-фетопротеина в крови. Эта комбинация гораздо реже отмечается у больных с печеночными метастазами.
Специальные методики сканирования
При сканировании с низким механическим индексом (МИ
0,1), часто совмещенном с фазовой инверсией, мелкие микропузырьки сразу же разрушаются во время начального прохождения болюса. Это удлиняет контрастное усиление В то же время использование низкого механического индекса снижает чувствительность исследования. Например, при использовании низкого механического индекса заднее акустическое усиление уже не является эффективным критерием дифференцировки кист от других гипоэхогенных образований. В некоторых случаях заднее акустическое усиление вновь появляется лишь при подъеме механического индекса до «нормальных» величин от 1,0 до 2,0.
Переменная трансмиссия двух ультразвуковых импульсов в секунду вместо 15 (переменная гармоническая визуализация) позволяет визуализировать даже мельчайшие капилляры, поскольку более длительная межимпульсная задержка ведет к меньшему разрушению микропузырьков. В результате их большая концентрация приводит к капиллярному усилению сигнала, когда отсроченный импульс проходит через ткань.
При применении методики переменной импульсной трансмиссии при низком механическом индексен даже гиповаскулярные метастазы становятся гиперэхогенными в раннюю артериальную фазу (в течение первых 5-10 секунд от прохождения контрастного вещества), при этом создается видимое различие между ранней артериальной и артериальной фазами контрастного усиления.
Важное правило дифференциальной диагностики образований печени
Применение контрастных веществ позволяет использовать следующее диференциально-диагностическое правило: образования с большей продолжительностью усиления сигнала скорее всего являются доброкачественными, тогда как метастазы и гепатоцеллюлярном раке часто гипоэхогенны по сравнению с окружающей паренхимой печени даже в позднюю венозную фазу.
Воспалительные заболевания кишечника
Несмотря на сложные условия сканирования желудочно-кишечного тракта некоторые патологические состояния можно выявить и оценить с помощью ультразвукового метода. В-режим позволяет заподозрить воспалительный процесс по наличию экссудата и утолщению стенок кишки Выявление гиперваекуляризации дает возможность предположить хроническое или острое воспалительное заболевание кишечника. При флюороскопической энтерографии (контрастное исследование тонкой кишки с помощью техники Sellink) определяется сегмент остаточного просвета. Острый энтерит и лучевой энтерит также характеризуются неспецифической гиперваскуляризацией, что приводит к увеличению скорости кровотока и его объема в верхней брыжеечной артерии. При аппендиците также определяется неспецифическая гиперваскуляризация утолщенной и воспаленной кишечной стенки.
Ультразвуковая допплерография является неинвазивной методикой исследования с различными возможностями оценки органов и сосудистых систем брюшной полости. Печень легко доступна ультразвуковому исследованию даже в сложных клинических условиях. Для оценки очаговых и диффузных изменений паренхимы и сосудов печени определены специфические показания. Ультразвуковая допплерография стала методикой выбора в диагностике и оценке портальной гипертензии, а также в планировании и контроле постановки чрезяремного внутрипеченочного портосистемного шунта. Ультразвуковая допплерография позволяет произвести неинвазивное измерение скорости и объема кровотока, выявить такие осложнения, как стеноз и окклюзия.
Ультразвуковая допплерография используется для послеоперационного контроля трансплантатов печени с целью определения перфузии органа. Однако не существует стандартных критериев, позволяющих поставить диагноз отторжения трансплантата печени.
Характеристика очаговых образований печени основана на степени васкуляризации. Известны некоторые критерии злокачественности, которые помогают более точно диагностировать объемное образование печени. Применение ультразвуковых контрастных препаратов позволяет улучшить отображение васкуляризации и оценить изменения картины перфузии в различные фазы контрастирования.
При исследовании сосудов брюшной полости ультразвуковая допплерография используется для скрининга и оценки аневризм. Для планирования терапевтического и хирургического лечения могут потребоваться дополнительные методы, такие, как КТ, МРТ и ДСА. Ультразвуковая допплерография также является методом скрининга при хронической ишемии кишечника.
Способность ультразвуковой допплерографии выявлять повышенную васкуляризацию при воспалительных заболеваниях, таких, как аппендицит и холецистит, расширила возможности ультразвуковой диагностики.
Опытный специалист УЗИ может определить специализированные нестандартные показания к ультразвуковой допплерографии, используя датчик с высоким пространственным разрешением. Однако существуют и определенные ограничения этого метода. Например, для проведения полного обследования может потребоваться значительное время. Более того, операторозависимость ультразвуковой допплерографии при обследовании брюшной полости достаточно высока. Благодаря достижениям в электронной обработке данных результаты исследований будут продолжать улучшаться, становясь более детализированными и легко интерпретируемыми, например, при использовании панорамной техники SieScape и трехмерных реконструкций.
Тканевая гармоническая визуализация является новой методикой, которая используется в диагностически сложных случаях, позволяя улучшить визуализацию при плохих условиях сканирования брюшной полости. Использование различных контрастных препаратов значительно улучшило возможности ультразвуковой диагностики, особенно у больных с объемными образованиями печени. Таким образом, ультразвуковая допплерография представляет собой неинвазивную диагностическую методику с высоким потенциалом развития, которая при обследовании брюшной полости обязательно должна применяться значительно шире, чем в настоящее время.
источник
Воротная вена печени (ВВ, портальная вена) представляет собой крупный ствол, в который поступает кровь из селезенки, кишечника и желудка. Затем она перемещается в печень. Орган обеспечивает очищение крови, и она снова поступает в общее русло.
Анатомическое строение воротной вены сложное. Ствол имеет множество ответвлений на венулы и прочие различные по диаметру кровеносные русла. Портальная система представляет собой еще один круг кровотока, назначением которой является очистка плазмы крови от продуктов распада и токсических компонентов.
Изменившиеся размеры воротной вены позволяют диагностировать определенные патологии. Ее нормальная длина равна 6–8 см, а диаметр – не больше 1,5 см.
Чаще всего встречаются следующие патологии воротной вены:
- тромбоз;
- портальная гипертензия;
- кавернозная трансформация;
- пилефлебит.
Тромбоз воротной вены представляет собою тяжелую патологию, при котором в ее просвете формируются кровяные сгустки, препятствующие ее оттоку после очищения. При отсутствии лечения диагностируется увеличение сосудистого давления. В итоге развивается портальная гипертензия.
К основным причинам формирования патологии принято относить:
- циррозное поражение печени;
- злокачественные новообразования ЖКТ;
- воспаление пупочной вены в процессе постановки катетеров младенцам;
- воспаления органов пищеварительной системы;
- травмы и хирургия селезенки, печени, желчного пузыря;
- нарушение свертываемости крови;
- инфекции.
К редким причинам развития тромбоза относят: период гестации, продолжительный прием оральных контрацептивов. Симптомами заболевания становятся: сильный болевой синдром, приступы тошноты, заканчивающиеся рвотой, диспепсические расстройства, повышение температуры тела, геморроидальные кровотечения (иногда).
Для прогрессирующей хронической формы тромбоза – при условии частичного сохранения проходимости воротной вены – типична следующая симптоматика: скопление жидкости в брюшной полости, увеличение размера селезенки, болезненность/чувство тяжести в области левого подреберья, расширение вен пищевода, что увеличивает риск развития кровотечения.
Основной способ диагностирования тромбоза – проведение УЗИ-исследования. На мониторе тромб определяется как гиперэхогенное (плотное) образование, заполняющее и венозный просвет и ветви. Тромбы небольших размеров выявляются во время эндоскопического УЗИ. Методики КТ и МРТ позволяют выявить точные причины патологии и выявить сопутствующие патологии.
Патология развивается на фоне врожденных пороков формирования вен – сужения, полного/частичного отсутствия. В этом случае в области ствола воротной вены обнаруживается кавернома. Она представляет собой множество мелких сосудиков, в определенной степени компенсирующих нарушение кровообращение портальной системы.
Кавернозная трансформация, выявленная в детском возрасте, является признаком врожденного нарушения строения сосудистой системы печени. У взрослых людей кавернозное образование указывает на развитие портальной гипертензии, спровоцированной гепатитом либо циррозом.
Портальная гипертензия – патологическое состояние, характеризующееся увеличением давления в портальной системе. Становится причиной формирования тромбов. Физиологическая норма давления в воротной вене – не выше 10 мм рт. ст. Повышение этого показателя на 2 и больше единиц становится поводом для диагностирования портальной гипертензии.
Провоцирующими патологию факторами становятся:
- цирроз печени;
- тромбоз печеночных вен;
- гепатиты различного происхождения;
- тяжелые сердечные патологии;
- нарушения обменных процессов;
- тромбы селезеночных вен и воротной вены.
Клиническая картина портальной гипертензии выглядит следующим образом: диспепсическая симптоматика; тяжесть в области левого подреберья, желтуха, снижение веса, общая слабость.
Характерный признак синдрома – увеличение объема селезенки. Причиной становится венозный застой. Кровь не может покинуть пределы органа из-за закупорки вен селезенки. Кроме спленомегалии, отмечается скопление жидкости в брюшной полости, а также варикозное расширение вен нижней части пищевода.
В ходе УЗИ-исследования выявляются увеличенные в размерах печень и селезенка, скопление жидкости. Размеры воротной вены и кровоток оцениваются с помощью допплерографии. Для портальной гипертензии характерно увеличение ее диаметра, а также расширение верхней брыжеечной и селезеночной вен.
Среди воспалительных процессов ведущее место занимает гнойное воспаление воротной вены – пилефлебит. Провоцирующим фактором чаще всего выступает острый аппендицит. При отсутствии лечения происходит некротизация тканей печени, завершающаяся смертью человека.
Заболевание не имеет характерной симптоматики. Клиническая картина выглядит следующим образом:
- сильный жар; озноб;
- появляются признаки отравления;
- сильные боли в животе;
- внутреннее кровоизлияние в области вен пищевода и/или желудка;
- желтуха, вызванная поражение паренхимы печени.
Лабораторные исследования показывают увеличение концентрации лейкоцитов, повышение скорости оседания эритроцитов. Такое смещение показателей указывает на острое гнойное воспаление. Подтвердить диагноз можно только при помощи УЗИ, МРТ и КТ.
Заболевание протекает в острой и хронической форме, что отражается на текущей симптоматике. Для острой формы типичны следующие симптомы: развитие сильных болей в животе, повышение температуры тела до значительных показателей, лихорадка, увеличение объема селезенки, развитие тошноты, рвота, диарея.
Симптоматика развивается одновременно, что приводит к сильному ухудшению общего состояния.тХроническое течение болезни опасно полным отсутствием какой-либо симптоматики. Заболевание диагностируется совершенно случайно в ходе планового УЗИ-исследования.
Отсутствие патологической симптоматики становится причиной запуска компенсаторных механизмов. Чтобы защититься от болей, тошноты и прочих проявлений, организм запускает процесс вазодилатации – увеличение диаметра печеночной артерии и образование каверномы.
По мере ухудшения состояния у больного, все же, развиваются определенные симптомы: слабость, нарушения аппетита. Особую опасность для человека представляет портальная гипертензия. Для нее характерно развитие асцита, увеличение подкожных вен, расположенных на передней брюшной стенке, а также варикоз вен пищевода.
Для хронической стадии тромбоза характерно воспаление воротной вены. Признаками состояния могут выступать:
- тупые непрекращающиеся боли в животе;
- долго удерживающаяся субфебрильная температура;
- увеличение печени и селезенки.
Основная диагностическая методика, позволяющая выявлять изменения воротной вены, остается УЗИ. Исследование может назначаться женщинам в положении, детям и пациентам преклонного возраста. Допплерометрия, используемая совместно с УЗИ, помогает дать оценку скорости и направлению кровотока. В норме он должен быть направлен в сторону органа.
При развитии тромбоза в просвете сосуда выявляется гиперэхогенное (плотное) неоднородное образование. Оно может заполнять как весь просвет сосуда, так и перекрывать его только частично. В первом случае движение крови полностью прекращается.
При развитии синдрома портальной гипертензии выявляется расширение сосудистого просвета. Кроме этого, медик выявляет увеличенную в размерах печень, скопление жидкости. Допплерография покажет снижение скорости кровотока.
Возможным признаком портальной гипертензии становится кавернома. Пациенту в обязательном порядке назначают проведение ФГДС с целью оценки состояния анастомозов пищевода. Дополнительно может быть рекомендована эзофагоскопия и рентгенология пищевода и желудка.
Кроме УЗИ-исследования, может использоваться методика компьютерной томографии с контрастирующим веществом. К преимуществу применения КТ стоит отнести визуализацию паренхимы печени, лимфатических узлов и прочих образований, расположенных в непосредственной близости.
Ангиография – наиболее точная методика диагностирования тромбоза воротной вены. Инструментальные исследования дополняются тестированием крови. Клинический интерес представляют показатели лейкоцитов, печеночных ферментов, билирубина.
Лечение заболевания предполагает комплексный подход и включает прием лекарственных средств, оперативное вмешательство. Медикаментозная терапия включает прием следующих средств:
- препаратов из группы антикоагулянтов – предупреждает формирование тромбов и улучшает проходимость сосудов;
- тромболитиков – растворяют уже имеющиеся тромбы, освобождая просвет воротной вены.
При отсутствии терапевтического результата от подобранной лекарственной терапии, человеку назначается оперативное лечение. Может быть выполнена чрезпеченочная ангиопластика либо тромболиз.
Основным осложнением оперативного лечения становится кровотечения вен пищевода и развития кишечной ишемии. Любая патология воротной вены печени – серьезное состояние, требующее назначения адекватной состоянию терапии.
источник
Воротная вена (портальная вена или ВВ) – это крупный сосудистый ствол, который собирает кровь из желудка, селезёнки, кишечника, после чего транспортирует её в печень. Там кровь очищается и опять возвращается в гемациркуляторное русло.
Анатомия сосуда довольно сложная: главный ствол разветвляется на венулы и другие кровеносные сосуды с разным диаметром. Благодаря портальной вене, (ПВ) печень насыщается кислородом, витаминами, минералами. Этот сосуд очень важен для нормального пищеварения и детоксикации крови. При нарушении работы ВВ проявляются тяжёлые патологии.
Как упоминалось ранее, воротная вена печени имеет сложную структуру. Портальная система является своеобразным дополнительным кругом кровотока, главная задача которого – очистить плазму от токсинов и продуктов распада.
При отсутствии системы воротной вены (СВВ) вредные вещества сразу бы попадали в нижнюю полую вену (НПВ), сердце, малый круг кровообращения и артериальную часть большого. Подобное нарушение возникает при диффузном изменении и уплотнении печёночной паренхимы, которое проявляется, например, при циррозе. Вследствие того, что отсутствует «фильтр» на пути венозной крови, повышается вероятность сильного отравления организма метаболитами.
Из курса анатомии известно, что во многие органы входят артерии, которые насыщают их полезными веществами. А выходят из них вены, которые транспортируют кровь после переработки к правой части сердца, лёгким.
ПС устроена немного по-другому – в так называемые ворота печени входит артерия и вена, кровь из которых проходит паренхиму и вновь попадает в вены органа. То есть образуется вспомогательный круг кровообращения, который влияет на функциональность организма.
Образование СВВ происходит, благодаря крупным стволам вен, которые объединяются рядом с печенью. Брыжеечные вены переносят кровь от кишечника, селезёночный сосуд выходит из одноименного органа и принимает питательную жидкость (кровь) из желудка, поджелудочной железы. За последним органом сливаются крупные вены, которые дают начало СВВ.
Между панекретодуоденальной связкой и ПВ проходят желудочные, околопупочные, препилорические вены. На этом участке ПВ располагается за печёночной артерией и общей желчевыводящей протокой, вместе с которой она следует к воротам печени.
Возле ворот органа венозный ствол делится на правую и левую ветку ВВ, которые проходят между печеночными долями и разветвляются на венулы. Мелкие вены покрывают печёночную дольку снаружи и внутри, а после контакта крови с печёночными клетками (гепатоциты), они двигаются к центральным венам, выходящих из середины каждой дольки. Центральные венозные сосуды соединяются в более крупные, после чего формируют вены печени, которые впадают в НПВ.
Воротная система печени не изолирована от других систем. Они проходят рядом, чтобы при нарушении кровообращения на данном участке можно было сбросить «лишнюю» кровь в другие венозные сосуды. Таким образом, на время компенсируется состояние пациента при тяжёлых патологиях паренхимы печени или тромбозе ВВ, но при этом повышается вероятность кровоизлияний.
ПВ и другие венозные коллекторы соединены, благодаря анастомозам (соединения). Их размещение хорошо знают хирурги, которые часто останавливают кровотечения из анастомозирующих участков.
Соединения портального и полых венозных сосудов не выражены, так как не несут особой нагрузки. При расстройстве функциональности ВВ, когда затрудняется ток крови в печень, портальный сосуд расширяется, давление в нём повышается, как следствие, кровь сбрасывается в анастомозы. То есть кровь, которая должна была попасть в ПВ, через портокавальные анастомозы (система соустий) наполняет полую вену.
Наиболее значимые анастомозы ВВ:
- Соединения между венами желудка и пищевода.
- Соустья между венозными сосудами прямого кишечника.
- Анастомозы вен передней стенки живота.
- Соединения вен пищеварительных органов с сосудами забрюшинного пространства.
Как упоминалось ранее, возможность выброса крови в полый сосуд через пищеводные сосуды ограничена, поэтому они из-за перегрузки расширяются, повышается вероятность опасного кровоизлияния. Сосуды нижней и средней трети пищевода не спадаются, так как размещены продольно, однако существует риск их повреждения во время еды, рвоты, рефлюкса. Часто кровоизлияние из поражённых варикозом вен пищевода, желудка наблюдается при циррозе.
От вен прямого кишечника кровь устремляется в ПС и НПВ. Когда повышается давление в бассейне ВВ, возникает застойный процесс в сосудах верхней части печени, откуда жидкость через коллатерали попадает в среднюю вену нижней части толстой кишки. Как следствие, проявляется геморрой.
Третье место, где сливаются 2 венозных бассейна – это передняя стенка живота, где сосуды околопупочной зоны принимают «лишнюю» кровь, расширяясь ближе к периферии. Это явление называют «голова медузы».
Соединения между венами забрюшинного пространства и ПВ не так выражены, как вышеописанные. Выявить их по внешним симптомам не получится, а к кровоизлиянию они не предрасположены.
Тромбоз воротной вены (ТВВ) – это патология, для которой характерно замедление или блокирование кровотока в ПВ тромбами. Сгустки препятствуют движению крови к печени, вследствие чего в сосудах возникает гипертония.
Причины тромбоза воротной вены печени:
- Цирроз.
- Рак кишечника.
- Воспалительное поражение пупочной вены во время катетеризации у грудного ребенка.
- Воспалительные заболевания пищеварительного тракта (воспаление желчного пузыря, кишечника, язва и т. д.).
- Травмы, операции (шунтирование, спленэктомия, холецистэктомия, трансплантация печени).
- Расстройства коагуляции (болезнь Вакеза, опухоль поджелудочной железы).
- Некоторые инфекционные заболевания (туберкулёз портальных лимфоузлов, цитомегаловирусная инфекция).
Реже всего тромбоз провоцирует беременность, а также оральные контрацептивы, которые женщина принимает на протяжении длительного времени. Особенно это касается пациенток старше 40 лет.
При ТВВ у человека наблюдается дискомфорт, боль в животе, тошнота, извержение рвотных масс, расстройства стула. Кроме того, существует вероятность жара, ректального кровотечения.
При прогрессирующем тромбозе (хронический) кровоток в ПВ частично сохранён. Тогда становятся более выраженными симптомы портальной гипертензии (ПГ):
- жидкость в брюшной полости;
- увеличение селезёнки;
- ощущение тяжести и боль слева под рёбрами;
- расширение вен пищевода, при котором повышается вероятность опасного кровоизлияния.
Если пациент стремительно теряет вес, страдает от избыточной потливости (ночью), то необходимо провести качественную диагностику. Если у него увеличен лимфоузел возле ворот печени и сам орган, то без грамотной терапии не обойтись. Таким образом проявляется лимфаденопатия, которая является признаком рака.
Выявить тромбоз ВВ поможет УЗИ, на снимке тромб в портальной вене выглядит как образование с высокой плотностью для УЗ-волн. Сгусток крови заполняет ВВ, а также её ветви. УЗИ-Доплера покажет, что кровоток на повреждённом участке отсутствует. Мелкие вены расширяются, как следствие, наблюдается кавернозное перерождение сосудов.
Эндо-УЗИ, компьютерная или МР-томография поможет определить небольшие сгустки крови. Кроме того, с помощью этих исследований можно выявить причины тромбоза, его осложнения.
Портальная гипертензия (ПГ) – это состояние, которое проявляется повышением давления в ПС. Патология часто сопутствует тромбу ВВ, тяжёлым системным заболеваниям (чаще всего печени).
ПГ обнаруживают при блокировке кровообращения, из-за чего повышается давление в СВВ. Блокировка может происходить на уровне ВВ (предпечёночная ПГ), перед синусоидными капиллярами (печёночная ПГ), в полой нижней вене (надпечёночная ПГ).
У здорового человека давление в ПВ составляет около 10 мм рт. ст., если это значение увеличивается на 2 единицы, то это явный признак ПГ. В таком случае постепенно включаются соустья между притоками ВВ, а также притоками верхней, нижней полых вен. Тогда варикоз поражает коллатерали (обходные пути кровотока).
- Цирроз.
- Тромбоз печёночных вен.
- Разные типы гепатита.
- Врождённые или приобретённые изменения структур сердца.
- Нарушение обмена веществ (например, пигментный цирроз).
- Тромбоз селезёночной вены.
- Тромбоз ПВ.
ПГ проявляется диспепсией (метеоризм, расстройства дефекации, тошнота и т. д.), тяжестью справа под рёбрами, окрашиванием кожи, слизистых оболочек в жёлтый цвет, снижением веса, слабостью. При повышении давления в СВВ проявляется спленомегалия (увеличена селезёнка). Это обусловлено тем, что селезёнка больше всего страдает от венозного застоя, так как кровь не может покинуть одноименную вену. Кроме того, проявляется асцит (жидкость в животе), а также варикоз вен нижнего участка пищевода (после шунтирования). Иногда у пациента увеличены лимфатические узлы у ворот печени.
С помощью ультразвукового исследования органов брюшной полости можно выявить изменение размера печени, селезёнки, а также жидкость в животе. Допплерометрия поможет оценить диаметр сосуда, скорость движения крови. Как правило, при ПГ портальная, верхняя брыжеечная и селезёночные вены увеличены.
Когда пациенту ставят диагноз «кавернозная трансформация портальной вены» далеко не все понимают, что это значит. Кавернома может быть врождённым пороком развития печёночных вен или следствием заболевания печени. При портальной гипертензии или тромбозе ВВ возле её ствола иногда обнаруживают множество мелких сосудов, которые переплетаются между собой и компенсируют кровообращение на этом участке. Кавернома внешне выглядит как новообразование, поэтому её так называют. Когда образования дифференцированы, важно начать лечение (хирургическое вмешательство).
У младших пациентов кавернозная трансформация свидетельствует о врождённых патологиях, а у взрослых – о портальной гипертензии, циррозе, гепатите.
Гнойное воспалительное поражение портальной вены и её ветвей именуют пилефлебитом, который часто переходит в ТВВ. Нередко заболевание провоцирует острый аппендицит, заканчивается оно гнойно-некротическим воспалением ткани печени и летальным исходом.
Пиефлебит не имеет характерных симптомов, поэтому выявить его достаточно тяжело. Не так давно такой диагноз давали пациентам после их гибели. Сейчас, благодаря новым технологиям (МРТ), заболевание можно выявить при жизни.
Проявляется гнойное воспаление жаром, ознобом, сильным отравлением, болью в животе. Иногда возникает кровоизлияние из вен пищевода или желудка. При инфицировании паренхимы печени развиваются гнойные процессы, что проявляется желтухой.
После лабораторных исследований станет известно, что повысилась скорость оседания эритроцитов, увеличилась концентрация лейкоцитов, что свидетельствует об остром гнойном воспалении. Но установить диагноз «пиефлебит» можно только после проведения УЗИ, КТ, МРТ.
Чаще всего для выявления изменений портальной вены применяют УЗИ. Это дешёвый, доступный, безопасный метод диагностики. Процедура безболезненна, подходит пациентам разной возрастной категории.
УЗИ-Доплера позволяет оценить характер движения крови, портальная вена просматривается у ворот печени, где она делится на 2 ветки. Кровь двигается в сторону печени. С помощью 3-D/4-D-УЗИ можно получить объёмное изображение сосуда. Нормальная ширина просвета ВВ во время ультразвукового исследования – около 13 мм. Проходимость сосуда имеет огромное значение в диагностике.
Также этот метод позволяет выявить гипоэхогенное (сниженная акустическая плотность) или гиперэхогенное (повышенная плотность) содержимое в портальной вене. Такие очаги свидетельствуют об опасных заболеваниях (ТВВ, цирроз, абсцесс, карцинома, рак печени).
При портальной гипертензии УЗИ покажет, что диаметр сосудов увеличен (это касается и размера печени), а в брюшной полости скопилась жидкость. С помощью цветного допплера можно выявить, что кровообращение замедлилось, появились кавернозные изменения (косвенный симптом портальной гипертензии).
Магнитно-резонансная томография полезна тем, что помогает определить причины изменений в системе воротной вены. Проводится осмотр паренхимы печени, лимфоузлов и окружающих образований. МРТ покажет, что в норме максимальный вертикальный размер правой доли печени составляет 15 см, левой – 5 см, билобарный размер у ворот печени – 21 см. При отклонениях эти значения меняются.
Кроме инструментальных исследований, проводятся ещё и лабораторные. С их помощью обнаруживают отклонения от нормы (избыток лейкоцитов, повышение ферментов печени, сыворотка крови содержит большое количество билирубина и т. д.).
Для лечения патологий воротной вены необходима комплексная медикаментозная терапия, хирургическое вмешательство. Пациенту, как правило, назначают антикоагулянты (Гепарин, Пелентан), тромболитические препараты (Стрептокиназа, Урокиназа). Первая разновидность медикаментов необходима для профилактики тромбообразования, восстановления проходимости вены, а вторая разрушает сам сгусток крови, который перекрывает просвет ВВ. Чтобы предотвратить тромбоз портальной вены, применяют неселективные β-блокаторы (Обзидан, Тимолол). Это наиболее эффективные медикаменты для лечения и профилактики ТВВ.
Если медикаменты оказались неэффективными, то врач назначает чреспечёночную ангиопластику или тромболитическую терапию с портосистемным шунтированием в печени. Основное осложнение тромбоза ВВ – это кровоизлияние из вен пищевода, а также ишемия кишечника. Лечить эти опасные патологии нужно только хирургическим методом.
Прогноз при патологиях воротной вены зависит от степени повреждений, которые они спровоцировали. Если тромболитическая терапия при лечении острого тромбоза оказалась не совсем эффективной, то без операции не обойтись. Тромбоз с хроническим течением грозит опасными осложнениями, поэтому пациенту сначала нужно оказать первую помощь. В противном случае повышается риск летального исхода.
Таким образом, воротная вена – это важный сосуд, который собирает кровь от желудка, селезёнки, поджелудочной железы, кишечника и транспортирует её к печени. После фильтрации она вновь возвращается в венозное русло. Патологии ВВ не проходят бесследно и грозят опасными осложнениями, вплоть до смерти, поэтому важно вовремя выявить заболевание и провести грамотную терапию.
источник