Особая ранимость печени при недостаточности правого сердца объясняется тем, что печень является ближайшим к сердцу резервуаром, способным депонировать большое количество крови и тем самым значительно облегчать работу правого желудочка сердца.
Увеличение печени является центральным звеном в развитии недостаточности правого сердца. Особенно это относится к таким заболеваниям, как митральный стеноз с недостаточностью трехстворчатого клапана, слипчивый перикардит, легочное сердце, а также другие заболевания сердца, плевры, легких, диафрагмы, приводящие к слабости систолы правого желудочка.
Наиболее часто наблюдается картина застойной печени. В результате различных поражений сердца наступает застой в правом предсердии, повышается давление в печеночных венах и наступает расширение центральных вен. Замедление кровообращения усиливает переполнение кровью центральных вен, центральной части долек и развивается центральная портальная гипертония, имеющая преимущественно механическое происхождение, затем присоединяется гипоксия. С помощью катетеризации вен печени у больных с недостаточностью кровообращения было показано, что в них содержится меньше кислорода, чем в нормальных условиях.
Постоянно повышенное давление в печеночных венах вызывает центролобулярный некроз клеток печени, который встречается при всех формах поражения сердца, но особенно пи недостаточности трехстворчатого клапана, митральном стенозе и слипчивом перикардите.
Наряду с расширением капилляров и центролобулярным некрозом начинается разрастание соединительной ткани. На периферии долек, где кровоснабжение хуже, наступает ожирение печеночных клеток. Если устраняется венозный застой, происходит регенерация центролобулярных клеток и печень восстанавливает свою первоначальную структуру. Правда, ряд авторов отметили, что при снижении венозного давления не всегда устраняется венозный застой, то же относится и к гистологической картине печени.
Застойные явления клинически выражаются в увеличении печени, нижний край ее достигает пупка, твердый, ровный и чувствителен при пальпации. Чувствительность увеличенной печени – ранний признак застоя, что предшествует отекам. Иногда она движется, пульсирует, так что можно наблюдать печеночный пульс. Пульсация встречается в период желудочковой систолы, имеет значение печеночно-ягулярный рефлюкс. Эти явления динамического характера наблюдаются чаще при недостаточности трехстворчатого клапана.
Больные могут жаловаться на спонтанные боли в правой половине живота, по интенсивности похожие на те, которые бывают на ранней стадии инфекционного гепатита. Очевидно, они связаны с натяжением нервных окончаний капсулы печени. Часто отмечается чувство тяжести, натяжения и полноты, наступающее во время еды и сохраняющееся долго после нее. Ухудшается аппетит, появляется тошнота и рвота, плохое самочувствие. Диспепсические явления связаны еще и с застойными явлениями в желудочно-кишечном тракте.
При застойной печени может развиться асцит, в происхождении которого имеют значение: повышение давления в венах печени, снижение содержания альбуминов в сыворотке и задержка натрия. Больные, у которых развивается асцит, чаще имеют особенно высокое венозное давление, низкий сердечный выброс в сочетании с тяжелыми центролобулярными повреждениями клеток.
Функциональные пробы печени обычно изменяются. Несколько повышается содержание билирубина и понижается уровень альбуминов в сыворотке крови. Наиболее выраженные изменения наблюдаются при применении функциональных проб, отражающих собственно функции печени (бромсульфалеиновый тест, радиоизотопное исследование). Правда, клинические симптомы застойной печени маскируются другими признаками расстройства кровообращения.
Сопоставление морфологических исследований и функционального состояния печени у больных с декомпенсацией сердца и застойной печенью показывает, что изменения функциональных проб сочетаются с центролобулярным некрозом и атрофией клеток печени. Эти изменения еще могут рассматриваться как показатели цирроза печени, что важно отметить, так как нередко в практике появление изменения функциональных проб ошибочно отождествляют с циррозом печени.
Застойная печень специального лечения не требует. Применение пиявок на область печени на фоне кардиальной терапии способствует действию диуретических препаратов. показаны также бессолевая достаточно калорийная диета с достаточным количеством белка и витаминов.
Фиброзные изменения в печени встречаются вторично в результате аноксии, центролобулярного некроза и репаративных процессов. это центральный фиброз в дальнейшем может привести к центролобулярному циррозу. Устойчивые и часто повторяющиеся повышения давления в венах приводят к постепенной конденсации и коллапсу ретикулярной ткани с пролиферацией соединительной ткани. При продолжающемся повреждении сердца нити соединительной ткани простираются к центральным венам соседних полей, связывая их друг с другом и вызывая образование ложных долек.
О кардиальном циррозе печени можно говорить в тех случаях, когда имеются изменения в архитектонике, то есть наблюдаются три основных условия: (1) деструкция паренхиматозных клеток; (2) процессы регенерации; (3) пролиферация соединительной ткани.
Относительна редкость этих изменений, а значит, и развития истинного цирроза зависят от того, что при декомпенсации сердца происходят не истинные, но постоянные поражения печени. Большинство больных умирает раньше развития пролиферации соединительной ткани и регенераторной фазы. Имеет также значение тот факт, что в конечной стадии декомпенсации застойные и дистрофические процессы в печени являются постоянными, что не бывает периодов ремиссии, когда появляются условия для узловой регенерации. Истинный цирроз печени составляет 0,4% всех аутопсий.
Кардиальный цирроз печени имеет следующую патологоанатомическую картину. Стенки расширенных центральных вен склеротичны и утолщены. Число капилляров и анастомозов между печеночной и воротной веной увеличивается. В результате разрастания соединительной ткани, центральная вена трудно распознается. Желчные пути пролиферируют и возникают островки регенерации. Самым характерным для кардиального цирроза является резко выраженная степень фиброза в центральных зонах и сдавление воротной вены разросшейся соединительной тканью. Очевидно, поэтому возник термин кардиального фиброза, которым многие авторы рекомендуют называть это повреждение печени.
Несмотря на некоторые особенности морфологического развития кардиального цирроза, клиническая его симптоматика во многом тождественна портальному циррозу. При осмотре больного довольно часто отмечается небольшая желтушность кожных покровов. Соединение желтухи с имеющимся цианозом придает кожным покровам своеобразный вид.
Печень в этих случаях не очень большая, но твердая, с острым краем и с мелкой узловатостью поверхности, иногда увеличивается селезенка. Пульсация печени исчезает, развивается асцит. Особенно трудно решить, чем обусловлен асцит – сердечно-сосудистой недостаточностью или поражением печени. Развитие асцита после длительного периода отеков, наступающее уменьшение и уплотнение печени, увеличение селезенки и гипоальбуминемия дают основания для диагноза кардиального цирроза. В этих случаях асцит, как и другие признаки цирроза, сохраняются даже после успешного лечения сердечно-сосудистой недостаточности (исчезают отеки и др.).
У больных кардиальным циррозом печени часто наблюдается плохая переносимость медикаментов, особенно повышена чувствительность к наперстянке и строфантину, по-видимому с нарушением обезвреживающей функции печени.
Основанием для диагноза кардиального цирроза является наличие длительной декомпенсации при таких заболеваниях, как митральный стеноз с недостаточностью трехстворчатого клапана, слипчитвый перикардит, легочное сердце. Функциональное исследование печени выявляет выраженные нарушения ее функции. Так, наряду с гипоальбуминемией может повышаться уровень гаммаглобулинов и билирубина, становятся положительными осадочные реакции, иногда снижаются показатели пробы Квика-Пытеля. При радиоизотопном исследовании функции печени наблюдаются выраженные ее нарушения.
Наличие кардиального цирроза само по себе не ухудшает существенно прогноза и, если поражение сердца подается лечению, цирроз может протекать латентно, без наклонности к периодическим обострениям процесса.
Несмотря на то, что явная желтуха у больных с явлениями застоя печени и кардиального цирроза встречается редко, концентрация билирубина в сыворотке повышается остаточно часто. Желтуха встречается с одинаковой частотой как при застойных явлениях в печени, так и при сердечном циррозе. Многие авторы получили статистическую корреляцию между интенсивностью желтухи и венозным давлением в правом сердце. Кроме того в развитии желтухи имеет значение инфаркт легких. Так, из 424 аутопсий погибших от болезней сердца желтуха была у 4%, из них в 10,5% случаев был инфаркт (Kugel, Lichtmann).
Желтушность кожных покровов и склер при кардиальном циррозе невелика, кожный зуд отсутствует. Обращает внимание на себя неравномерная окраска кожных покровов. Так, в местах массивных отеков кожа не окрашена в желтый цвет в связи с тем, что циркулирующий в крови билирубин связан с белком и не поступает в отечную жидкость. У небольшого числа больных желтуха приобретает черты механической: интенсивное, с сероватым оттенком окрашивания кожи, отмечаются пигменты в моче и светлый кал.
Механизм желтухи при расстройствах кровообращения различный.
(1) Печеночная желтуха. Существует предположение, что при поражении сердца клетки печени неадекватно экскретируют все пигменты и действительно самая интенсивная желтуха отмечается у больных с тяжелым и распространенным некрозом клеток печени. Однако имеются исключения из этого правила, когда при недостаточности трехстворчатого клапана с тяжелыми поражениями печени желтухи не наблюдается.
(2) Механическая желтуха. Сдавление желчных капилляров в связи с резким повышением венозного давления внутри долек, а также образование тромбов в желчных канальцах, как следствие замедленного тока желчи в билиарной системе, создают условия для холестаза.
(3) Гемолитическая желтуха часто сочетается с геморрагиями в тканях, особенно инфарктами легких. Известно внезапное появление желтухи при клинической картине инфаркта: будь то легкого, селезенки или почек, в то время как инфаркты той же локализации, но без поражения сердца не дают желтухи.
В очаге инфаркта создается дополнительное депо гемоглобина, из которого образуется билирубин. Этот избыток пигмента не может связываться измененными клетками печени. Rich и Resnik вводили в ткань больных с пороком сердца количество крови, соответствующее тому, которое обнаруживается пи инфаркте легкого, и отмечали повышение билирубина сыворотки крови. Наблюдается также избыток пигмента в тканях при застое в легких на почве поражения сердца, так как и без инфаркта, застойные явления в легких приводят к разрушению гемоглобина.
Следовательно, желтуха при поражениях сердца в большинстве случаев смешанного типа; наибольшее значение имеют поражения клеток печени и перегрузка их пигментом в результате инфарктов, что подтверждается и лабораторными данными. Моча темная с повышенным количеством уробилина, при интенсивной желтухе обнаруживаются и другие желчные пигменты; кал темный с повышенным количеством стеркобилина, в отдельных случаях серого цвета с уменьшением выделения пигмента. В крови определяется повышенное количество билирубина, чаще с прямой реакцией ван ден Берга.
Лечение направлено главным образом на профилактику и терапию основного заболевания. Кроме того, наличие поражения печени требует диеты – стол №5, комплекс витаминов, при необходимости желчегонные препараты, по строгим показаниям кортикостеоиды
источник
Длительный венозный застой в печени при тяжелой хронической правожелудочковой недостаточности может привести к повреждению гепатоцитов и развитию цирроза. В отличие от острого венозного застоя в печени при острой сердечной недостаточности и от ишемического гепатита («шоковая печень»), который развивается при артериальной гипотонии в результате снижения печеночного кровотока, для сердечного цирроза печени, как и для любого другого, характерны выраженный фиброз и образование узлов регенерации.
Патологическая анатомия и патогенез. Правожелудочковая недостаточность приводит к повышению давления в нижней полой вене и печеночных венах и застою крови в печени. Синусоиды при этом расширены и переполнены кровью, печень увеличена, капсула ее напряжена. Длительный венозный застой и ишемия, связанная с низким сердечным выбросом, приводят к центролобулярному некрозу. В итоге развивается центролобулярный фиброз ; от центральных вен по направлению к портальным трактам подобно лучам расходятся соединительнотканные перегородки. Чередование красных участков венозного застоя и бледных участков фиброза создает на разрезе характерную картину «мускатной печени».
Благодаря успехам современной кардиологии, и особенно кардиохирургии, сердечный цирроз теперь встречается намного реже, чем раньше.
Изменения лабораторных показателей довольно разнообразны. Уровень билирубина. как правило, повышен незначительно, может преобладать как прямая, так и непрямая фракция. Возможны умеренный рост активности ЩФ и удлинение ПВ. Активность АсАТ обычно слегка повышена; выраженная артериальная гипотония иногда приводит к развитию ишемического гепатита («шоковая печень»), клинически напоминающего вирусный гепатит или токсический гепатит. и резкому кратковременному повышению уровня АсАТ. При трикуспидальной недостаточности иногда наблюдается пульсация печени. но с развитием цирроза этот симптом исчезает.
При хронической правожелудочковой недостаточности печень увеличена. плотная и обычно безболезненная. Кровотечение из варикозных вен пищевода бывает редко, но может развиться печеночная энцефалопатия. для которой характерно волнообразное течение в соответствии с колебаниями тяжести правожелудочковой недостаточности. Асцит и отеки. вначале связанные лишь с сердечной недостаточностью, при развитии цирроза могут нарастать.
Диагностика. О сердечном циррозе печени следует думать, если у больного, более 10 лет страдающего приобретенным пороком сердца. констриктивным перикардитом или легочным сердцем. обнаружена увеличенная плотная печень в сочетании с другими признаками цирроза. Подтвердить диагноз можно с помощью биопсии печени, но при повышенной кровоточивости и асците она противопоказана.
В случаях, когда одновременно обнаруживают поражение печени и сердца, следует исключить гемохроматоз. амилоидоз и другие инфильтративные болезни.
ЛЕЧЕНИЕ. Главное в лечении и профилактике сердечного цирроза печени — лечение основного заболевания. Уменьшение правожелудочковой недостаточности способствует улучшению функции печени и препятствует прогрессированию цирроза.
Заболевание развивается сравнительно редко. При застое крови в печени наряду с расширением и переполнением кровью мелких вен выявляются расширение перисинусоидных пространств, атрофия гепатоцитов, а иногда и центролобулярные некрозы, которые в ряде случаев сочетаются с жировой дистрофией. Эти изменения могут сопровождаться фиброзом и регенерацией некоторых гепатоцитов с образованием узлов. Развитию цирроза печени, по-видимому, способствуют эпизоды острой сердечной недостаточности. Известно, что острый некроз гепатоцитов возникает при шоке (шоковая печень), однако в последнее время обращено внимание на значение синдрома малого выброса и при хронической сердечной недостаточности. Так, печеночная О-клеточная недостаточность и сердечный цирроз печени часто наблюдаются при заболеваниях, для которых характерно сочетание венозного застоя и уменьшение сердечного выброса (хроническая аневризма сердца, аортальный стеноз, дилатационная кардиомиопатия).
Для застойной печени характерны боли в правом подреберье вследствие растяжения ее капсулы. При сформировавшемся циррозе печени обычно наблюдается умеренное повышение уровня непрямого билирубина, как следствие сопутствующего гемолиза и сердечной недостаточности. Активность аминотрансфераз обычно повышается незначительно, но в периоды острого нарушения кровотока в печени (шок) возможно значительное повышение уровня аминотрансфераз и других ферментов, как при остром вирусном гепатите. Со временем могут появиться признаки печеночно-клеточной недостаточности.
Портальная гипертензия встречается редко. В некоторых случаях клинические симптомы поражения печени могут выходить на первый план, преимущественно при снижении минутного объема сердца.
Истинный сердечный цирроз печени развивается обычно не ранее чем через 10 лет после появления первых симптомов застойной сердечной недостаточности. В то же время при заболеваниях, сопровождающихся уменьшением минутного объема сердца, а также повторных эпизодах резкого снижения АД, обусловленных теми или иными причинами (в частности, острыми нарушениями ритма сердца), цирроз печени может сформироваться и ранее. Выраженные изменения печени наблюдаются при констриктивном перикардите, при котором возможно развитие как псевдоцирроза Пика (портальная гипертензия, асцит, увеличение печени при наличии умеренного ее фиброза), так и истинного цирроза печени.
Застойная печень наблюдается при хронической сердечной недостаточности, которая является частым осложнением всех органических болезней сердца (пороки, гипертоническая и коронарная болезни, констриктивный перикардит, миокардиты, инфекционные эндокардиты, фиброэластоз, миксома и др.), ряда хронических заболеваний внутренних органов (легких, печени, почек) и эндокринных заболеваний (сахарный диабет, тиреотоксикоз, микседема, ожирение).
Появление первых признаков сердечной недостаточности зависит от ряда причин, в том числе от сочетания нескольких заболеваний, образа жизни больного, присоединения интеркуррентных заболеваний. У некоторых больных от момента органического заболевания сердца до появления первых признаков сердечной недостаточности проходят десятилетия, а иногда она развивается довольно быстро вслед за органическим поражением сердца.
Первыми признаками хронической сердечной недостаточности являются сердцебиение и одышка при физических нагрузках. Со временем тахикардия становится постоянной, а одышка возникает и в покое, появляется цианоз. В нижних отделах легких выслушиваются влажные хрипы. Увеличивается печень, появляются отеки на ногах, затем жидкость скапливается в подкожной клетчатке и на теле, в серозных полостях, развивается анасарка.
На первых этапах сердечной недостаточности печень увеличивается в переднезаднем направлении и пальпаторно не определяется. Выявить увеличение печени можно с помощью инструментальных исследований (реогепатография, УЗИ). С нарастанием сердечной недостаточности печень заметно увеличивается, при этом она пальпируется в виде выступающего из подреберья болезненного края. Болезненность печени при пальпации связана с растяжением ее капсулы. Определяются тяжесть и давящие боли в правом подреберье, вздутие живота. Печень заметно увеличена, чувствительная или болезненная, поверхность ее гладкая, край острый. Нередко наблюдается желтуха. Функциональные печеночные пробы умеренно изменены. Эти изменения в большинстве случаев обратимы.
При гистологическом исследовании биоптатов печени выявляются расширение центральных вен и синусоидов, утолщение их стенок, атрофия гепатоцитов, развитие центроло-булярного фиброза (застойный фиброз печени). С течением времени фиброз распространяется на всю дольку (развивается септальный застойный цирроз печени).
Выявляют заболевание, которое может быть причиной сердечной недостаточности. Большую роль играет правильная оценка тахикардии и обнаружение признаков венозного застоя. Немаловажное значение имеет благоприятная динамика симптомов в процессе лечения сердечными гликозидами и мочегонными.
Лечение бывает успешным при правильном распознавании основного заболевания, которое привело к сердечной недостаточности, и проведении соответствующей каузальной терапии. Больным ограничивают двигательные нагрузки, потребление жидкости и поваренной соли.
При недостаточной эффективности общих мероприятий применяют внутрь сердечные гликозиды, длительно или постоянно (дигоксин, дигитоксин, изоланид, целанид, ацетилдигитоксин, настой адониса), тиазиды (фуросемид, бринальдикс, гипотиазид, юринекс, буринекс, урегит и др.) и калийсберегающие диуретики (триамтерен, триампур, амилорид, модуретик, верошпирон). Выбор мочегонного препарата и способ его применения определяются степенью отечного синдрома, стадией сердечной недостаточности и переносимостью.
Назначают также препараты, улучшающие обмен в миокарде,- анаболические стероиды (нероболил, ретаболил и др.), АТФ, витамины группы В, С, Е.
При наличии цианоза показана оксигенотерапия, при тяжелых нарушениях ритма — противоаритмическое лечение. Многие больные нуждаются в седативной терапии.
«Увеличение печени при хронической сердечной недостаточности» и другие статьи из раздела Заболевания печени и желчного пузыря
источник
Тесная связь между сердечной и печеночной дисфункциями изучается врачами разных специальностей на протяжении более чем двух столетий. Тем не менее сложность и особенности этой ассоциации и сейчас вызывают активный интерес ученых, а результаты относительно немногочисленных исследований нередко очень противоречивы, что может объясняться несколькими причинами.
Например, этиология сердечной недостаточности (СН) со временем изменилась. Если раньше СН главным образом была связана с ревматической клапанной болезнью, то сейчас в основном с ишемической кардиомиопатией. Кроме того, исходы СН резко улучшились вследствие эффективности фармакотерапии и широкого проведения трансплантации сердца. Поэтому кардиальный цирроз печени (ЦП), который ранее рассматривался как парадигма ассоциации печени и СН, в настоящее время встречается редко.
В связи с тем что СН является системным хроническим заболеванием, при ее наличии поражается множество органов, включая печень и почки. Особенности сосудистой системы печени и ее высокая метаболическая активность делают ее высоко уязвимой к нарушениям системной гемодинамики и инициируют многие молекулярные и гемодинамические изменения.
Печеночная дисфункция (ПД) часто встречается у пациентов с СН (по данным разных авторов, в 15-65% случаев) и тесно коррелирует с гемодинамическими параметрами.
В настоящее время систематизацию сочетанной патологии сердца и печени проводят в зависимости от первичной локализации патологического процесса (табл. 1).
В данном обзоре мы сфокусируемся на основной патологии печени, обусловленной заболеваниями сердечно-сосудистой системы, в первую очередь на застойной гепатопатии (ЗГ) и кардиогенном ишемическом гепатите, а также патологии сердца, сформировавшейся на фоне заболеваний печени (цирротическая кардиомиопатия).
ЗГ («застойная печень») включает в себя спектр клинических, биохимических, гистологических и гемодинамических нарушений, связанных с хроническим повреждением печени вследствие правожелудочковой/правопредсердной СН или любой другой причины повышения центрального венозного давления, включая бивентрикулярную СН вследствие ишемической болезни сердца или кардиомиопатии, тяжелую легочную гипертензию или легочное сердце, констриктивный перикардит, а также вальвулопатии, такие как митральный стеноз и трикуспидальная регургитация. Это состояние было впервые подробно описано выдающимся гепатологом Шейлой Шерлок в 1951 году.
Основными механизмами формирования ЗГ являются переполнение кровью центральных вен и центральной части печеночных долек, развитие в них локальной гипоксии, приводящей к возникновению дистрофических и атрофических изменений, а впоследствии – к некрозу гепатоцитов, синтезу коллагена и развитию фиброза. При этом давление в воротной вене не превышает давления в нижней и верхней полых венах, вследствие чего портокавальные анастомозы развиваются крайне редко. Тяжесть и характеристики повреждения печени зависят от вовлеченных сосудов, выраженности венозного застоя и снижения перфузии. Первое описание «мускатной печени» было сделано Kiernan и Mallory, которые показали центральный застой и очаговый некроз печени, связанные с нарушенной циркуляцией крови в печени.
Клинические проявления ЗГ зависят от скорости нарастания СН: если венозный застой в печени развивается быстро, то в клинике будут доминировать жалобы на острые боли в правом подреберье, связанные с растяжением капсулы печени, нередко симулирующие острую хирургическую патологию. Если СН развивается медленно, в течение нескольких месяцев или лет, то ее проявления будут доминировать и маскировать симптоматику ЗГ. Последний вариант встречается значительно чаще, поэтому в подавляющем большинстве случаев ЗГ протекает малосимптомно или асимптомно. В таких случаях пациенты предъявляют жалобы на одышку, ортопноэ и кардиалгии, практически не обращая внимания на тяжесть в правом подреберье и изменение цвета кожных покровов, поскольку желтуха и болевой синдром малоинтенсивны. Объективные признаки ЗГ (увеличенная, плотная и болезненная при пальпации печень с твердым и гладким краем) определяются на фоне расширения яремных вен, появления гепатоюгулярного рефлюкса и симптомов СН.
Отличительной чертой ЗГ является то, что выраженность ее симптоматики варьирует в зависимости от состояния центральной гемодинамики и эффективности лечения основной причины СН. Адекватная терапия СН приводит к быстрому уменьшению размеров печени и нивелированию клинических признаков ЗГ. Еще одна характерная особенность ЗГ состоит в отсутствии признаков портальной гипертензии (варикозное расширение вен пищевода и желудка, «caput medusaе») и так называемых малых признаков цирроза (пальмарная эритема, телеангиэктазии, «лакированный» язык). При тяжелом или рефрактерном течении СН явления ЗГ прогрессируют, и постепенно развивается кардиальный ЦП, сопровождающийся появлением асцита и спленомегалии. Печень становится плотной, ее край – острым, а размеры остаются постоянными и не зависят от эффективности лечения СН.
В большинстве случаев при легкой СН уровни сывороточных трансаминаз (АлАт, АсАт) и билирубина не превышают нормальных показателей, однако при тяжелой СН активность маркеров цитолитического и холестатического синдромов, а также уровень билирубина обычно возрастают. Примерно у 30% пациентов с ЗГ уровень трансаминаз превышает норму в 2-3 раза. Значительное снижение фракции выброса (ФВ) обычно сопровождается существенным повышением уровня сывороточных трансаминаз вследствие вторичной ишемии печени. У части больных отмечается холестатический компонент, отражающийся в повышении уровня γ-глютамилтрансферазы (ГГТ) и щелочной фосфатазы, являющихся независимыми факторами венозного застоя и снижения перфузии.
В частности, повышение уровня ГГТ не только ассоциируется с более тяжелым классом СН, более низкой ФВ и повышением уровня натрийуретического гормона В-типа, но и является независимым предиктором смерти и трансплантации сердца. Гипербилирубинемия для ЗГ не характерна, однако при тяжелой СН может отмечаться небольшое повышение уровня общего и непрямого билирубина, что рассматривается как неблагоприятный прогностический признак. При развитии кардиального цирроза появляется диспротеинемия (снижение концентрации общего белка и альбумина, повышение уровня α2– и γ-глобулинов), в 75% случаев увеличивается протромбиновое время. Характерными признаками асцита, развивающегося вследствие ЗГ и кардиального цирроза, являются высокое содержание белка в асцитической жидкости (>2,5 г/дл) и увеличение значения сывороточно-асцитического градиента альбумина (>1,1 г/дл). У многих больных, особенно с тяжелой СН, повышается уровень мочевой кислоты, что в настоящее время рассматривается как маркер воспаления, метаболических расстройств, оксидативного стресса, эндотелиальной дисфункции и, возможно, миокардиального повреждения. Гиперурикемия может быть следствием снижения ренальной перфузии и экскреции уратов, она хорошо коррелирует с более высоким давлением в легочной артерии и правом желудочке, а также с клиническими признаками застойной СН.
Для подтверждения диагноза ЗГ необходимо исключение других причин повреждения печени, в частности исключение наличия вирусного гепатита В и С при помощи иммуноферментного анализа или полимеразной цепной реакции, а также алкогольной болезни печени, неалкогольной жировой болезни печени / неалкогольного стеатогепатита и медикаментозного повреждения печени. Следует помнить, что многие медикаменты, применяющиеся для лечения кардиоваскулярной патологии, метаболизируются в печени и могут неблагоприятно воздействовать на нее (табл. 2).
Всем больным проводят эхокардиографию и ультразвуковое исследование с допплерографией сосудов печени, при котором хорошо выявляется венозный застой (расширенные печеночные вены, сливающиеся в расширенную нижнюю полую вену), как правило, при отсутствии портальной гипертензии (диаметр портальной вены 20 норм), но быстро обратимом повышении уровня сывороточных трансаминаз; 3) отсутствии других возможных причин повреждения печени. Клинически КАГ манифестирует появлением выраженной одышки, боли в правом подреберье, увеличением печени в размерах. В редких случаях могут отмечаться желтуха, олигурия, признаки печеночной энцефалопатии, вплоть до печеночной комы. Характерные изменения функциональных проб печени появляются через 12-24 ч после острого сердечно-сосудистого события и проявляются резким (в 20 раз и более) повышением уровней АсАт, АлАт и лактатдегидрогеназы, реже – гипербилирубинемией и коагулопатией (удлинение протромбинового времени, снижение уровня фибриногена, тромбоцитопения). При устранении действия провоцирующего фактора показатели возвращаются к норме в течение 5-10 дней.
Основной стратегией лечения КАГ является восстановление адекватной перфузии печени путем проведения противошоковых мероприятий, обязательного введения средств, обладающих положительным инотропным эффектом, таких как дофамин. При развитии печеночной энцефалопатии применяют L-аргинин, L-орнитин-L-аспартат, антибиотики. Прогноз при КАГ определяется кардиоваскулярным статусом пациента, поскольку смертность при этом заболевании обусловливается основным заболеванием.
Под термином «цирротическая кардиомиопатия» (ЦК) принято понимать снижение сократительной функции сердца, которая отмечается у части больных с ЦП. Первоначальные исследования в начале 1950-х годов зафиксировали существование при циррозе гипердинамического типа гемодинамики, что проявляется в увеличении сердечного выброса и снижении системного сосудистого сопротивления. H.J. Kowalski первым сообщил, что пациенты с циррозом Лаэннека имели аномальную сердечно-сосудистую функцию и удлинение интервала QT. Ранние гистологические исследования продемонстрировали гипертрофию миокарда и его ультраструктурные изменения, включая отек кардиомиоцитов, фиброз, экссудацию, ядерную вакуолизацию и необычную пигментацию.
Размер левого предсердия и ЛЖ у пациентов с ЦП нормальный или несколько увеличен, что связано с гемодинамической дисфункцией. Многие пациенты с ЦП отмечают одышку, задержку жидкости и ограничение физической активности.
Основными механизмами развития ЦК являются хронический алкоголизм и гипердинамический тип гемодинамики. Вследствие злоупотребления алкоголем ухудшается синтез сократительных белков и формирование связи сердечных белков с токсичным ацетальдегидом, что способствует ухудшению сердечной функции. При гипердинамическом типе гемодинамики сердце постоянно перегружено из-за повышенных сердечного выброса и объема циркулирующей крови, что также приводит к нарушению его сократительной функции. Другими потенциальными механизмами ухудшения сердечной функции при ЦП являются повышенная продукция таких кардиодепрессивных субстанций, как эндотоксины, эндотелины, цитокины и желчные кислоты, а также нарушение регуляторной функции β-рецепторов, функционирования мембранных калиевых и кальциевых каналов, активация каннабиоидной системы.
Физические упражнения, фармакологический стресс и терапевтические мероприятия способны повлиять на изменение давления в полостях сердца. В частности, у больных ЦП конечно-диастолическое давление увеличивается, а ФВ во время физической нагрузки падает, что указывает на аномальный желудочковый ответ на повышение желудочкового давления наполнения. Аэробные физические нагрузки и максимальная частота сердечных сокращений у большинства пациентов с циррозом должны быть меньшими по сравнению с таковыми у пациентов без цирроза. Аномальная диастолическая функция ЛЖ, вызванная снижением его релаксации, отражается в нарушении наполнения желудочков. Трансмитральный кровоток изменяется, при этом повышается вклад предсердий в позднюю фазу наполнения ЛЖ. Патофизиологической основой диастолической дисфункции при ЦП является повышенная жесткость стенки миокарда, скорее всего, из-за сочетания небольшой гипертрофии миокарда, фиброза и субэндотелиального отека.
Основным электрокардиографическим изменением при ЦП является удлинение интервала QT, скорректированного по частоте сердечных сокращений, что отмечается примерно у каждого второго пациента с ЦП и не зависит от его этиологии. У больных алкогольным ЦП удлинение интервала QT связано с повышением риска внезапной сердечной смерти. Удлинение интервала QT при циррозе также ассоциируется с наличием кардиальной автономной дисфункции, в первую очередь со снижением барорецепторной чувствительности, и частично обратимо после трансплантации печени.
Специфического лечения ЛЖ-дисфункции, связанной с ЦП, в настоящее время не существует. Поэтому терапия проводится по общим правилам путем ограничения соли, приема диуретиков и снижения постнагрузки. Назначение сердечных гликозидов не способствует существенному улучшению сократительной функции сердца при ЦК, в связи с чем они не рассматриваются как значимые препараты для ее лечения. Следует проявлять особую осторожность во время и после стрессовых событий, в первую очередь хирургических операций, включая трансюгулярное внутрипеченочное шунтирование и трансплантацию печени. Влияние удлиненного интервала QT на смертность больных ЦП является предметом будущих исследований. Принципиально новые методы лечения ЦК, такие как антицитокиновая терапия, также представляют большой интерес.
В заключение отметим, что вопросы, обсуждаемые в данной статье, имеют важное клинические значение как для гастроэнтерологов, так и для кардиологов. В частности, гастроэнтерологи, консультирующие больных с «необъяснимым» повышением трансаминаз или так называемыми идиопатическими ЦП, всегда должны помнить о потенциальной роли СН, даже латентно протекающей, и назначать соответствующее кардиологическое обследование. В свою очередь, кардиологи, наблюдающие пациентов с СН, у которых имеется сопутствующая ПД, должны рассматривать последних как группу повышенного риска и лечить более агрессивно. Надеемся, что дальнейшие исследования и более активное выявление ПД при СН поможет улучшить общее понимание патологического процесса, а также результаты лечения и клинические исходы при этом заболевании.
Список литературы находится в редакции
источник
Поражение печени при острой левожелудочковой и хронической сердечной недостаточности наблюдается у всех больных. Возможно развитие пассивного венозного застоя, гипоксемических некрозов, фиброза печени и в редких случаях — кардиального цирроза печени.
В основе поражения печени при изолированной левожелудочковой недостаточности у больных инфарктом миокарда, осложненным кардиогенным шоком, лежит уменьшение минутного объема сердца. Развитию центральных печеночных некрозов особенно способствует недостаточное кровоснабжение печени вследствие резкого снижения системного артериального давления. Такая ситуация наблюдается при кровотечениях, послеоперационных осложнениях, тепловом ударе, тяжелых ожогах и септическом шоке. Поэтому находят достоверную корреляцию частоты выявления некрозов печени на вскрытии с наличием в терминальном периоде выраженной гипотонии, почечной недостаточности, острого некроза канальцев почек и коры надпочечников на границе с мозговым слоем, свойственных шоку. Острые нарушения ритма сердца (желудочковая пароксизмальная тахикардия, фибрилляция или мерцание предсердий и др.) могут приводить к острой сердечной недостаточности и острой застойной печени с болью в правом подреберье, гипераминотрансфераземией и иногда желтухой. Наиболее часто застойная печень развивается при слабости правого желудочка сердца.
С гиподиастолией, обусловленной недостаточным расширением полостей сердца во время диастолы, связаны нарушения гемодинамики и венозный застой в большом круге кровообращения при сдавливающем (констриктивном) перикардите. Аналогичный механизм недостаточности кровообращения, но с преобладанием изменений левого желудочка сердца, лежит в основе других «констриктивных» кардиопатий, протекающих без поражения перикарда: миокардиосклероза различной этиологии, первичного амилоидоза, гемохроматоза с поражением сердца, париетального эндокардита Леффлера и алкогольной кардиомиопатии, которая может сочетаться с алкогольным циррозом печени.
Особая ранимость печени при недостаточности правого сердца объясняется тем, что печень является ближайшим к сердцу резервуаром, способным депонировать большое количество крови и тем самым значительно облегчать работу правого желудочка сердца. При сердечной недостаточности депонируемая в печени кровь может составлять до 70% массы органа (в норме около 35%). Повышение давления в правом предсердии непосредственно распространяется на нижнюю полую вену, подпеченочные вены, синусоиды и систему воротной вены, приводя к относительному снижению артериального кровоснабжения печени пропорционально уменьшению минутного объема сердца, гипоксии и ишемическим некрозам гепатоцитов. Портальная гипертензия при застойной сердечной недостаточности имеет свои особенности. Градиент заклиненного подпеченочного и свободного портального давления не повышен (давление в воротной вене и в обеих полых венах одинаково), поэтому портокавальной коллатеральной циркуляции и варикозного расширения вен пищевода не бывает.
При быстро развивающемся венозном застое увеличение и уплотнение печени сопровождается растяжением глиссоновой капсулы с резкой болью в правом подреберье и выраженной болезненностью и защитным напряжением мышц при пальпации, симулирующими острое хирургическое заболевание. Часто развивается незначительная желтуха, вначале обусловленная гипоксемическим гемолизом в печени (неконъюгированная гипербилирубинемия, уробилинурия). Позднее при развитии гипоксемических центрально-дольковых атрофических изменений гепатоцитов и некрозов возникает гепатоцеллюлярная желтуха с повышением уровня прямого билирубина крови, активности аминотрансфераз и часто щелочной фосфатазы крови. Массивный некроз паренхимы печени при остром венозном застое может обусловить развитие картины молниеносного гепатита с интенсивной желтухой, высокой активностью АлАТ и печеночной энцефалопатией.
В типичных случаях печень при хронической правосторонней сердечной недостаточности увеличена, уплотнена и болезненна. Поверхность ее гладкая. Больных часто беспокоят ощущение тяжести или длительная тупая боль в правом подреберье и подложечной области. У больных хроническим легочным сердцем и констриктивным перикардитом цианоз и одышка протекают без ортопноэ и значительного застоя в малом круге кровообращения.
При недостаточности трикуспидального клапана наблюдают характерную систолическую пульсацию увеличенной печени, ортопноэ и болезненные отеки ног. Селезенка увеличивается у 40% больных, возможно развитие гидроторакса и асцита. Биохимические изменения часто сводятся к умеренной гипербилирубинемии и гипоальбуминемии, гипераминотрансфераземии. На развернутых стадиях наблюдаются гипопротеинемия и гипопротромбинемия. Размеры печени нередко быстро уменьшаются под влиянием покоя, бессолевого режима, диуретической и кардиотонической терапии. При застойной гепатомегалии отсутствуют кожные телеангиэктазии, пальмарная эритема, признаки коллатеральной циркуляции. Отечно-асцитический синдром сочетается с одышкой и цианозом, характерно высокое содержание белка в асцитической жидкости (30-40 г/л). При эхографическом исследовании находят гепатомегалию, расширение нижней полой вены и отсутствие колебаний ее диаметра при дыхательных движениях.
Слипчивый перикардит нередко развивается вне связи с известными этиологическими факторами — туберкулезом, пиогенной инфекцией, ревматизмом или травмами сердца, т.е. бывает идиопатическим. При этом характерно сочетание раннего массивного и резистентного к диуретической терапии асцита с большой плотной безболезненной, непульсирующей печенью («псевдоцирроз Пика» вследствие фиброзного перигепатита) с рентгенологическими симптомами обызвествления перикарда и плевроперикардиальных сращений при нормальных или нерезко увеличенных размерах сердца. Рентгенологическое исследование органов грудной клетки является обязательным при любых формах патологии печени.
В пунктатах печени при хронической сердечной недостаточности (пункция печени при этой патологии показана) наиболее часто находят признаки хронического венозного застоя: расширение и переполнение кровью сублобулярных вен, центральных вен и прилежащих к ним синусоидов, расширение пространств Диссе, которые расположены между синусоидами и гепатоцитами и функционируют как лимфатические сосуды, атрофию гепатоцитов и центролобулярные некрозы, часто в сочетании с жировой дистрофией. При лапароскопии печень увеличена, край закруглен, капсула утолщена, поверхность печени имеет характерный вид «мускатного ореха» с наличием темно-красных и коричнево-желтых участков (мускатная печень). При констриктивном перикардите на поверхности печени видны обширные серовато-белые блестящие наложения фибрина, склероз и утолщение капсул печени и селезенки.
Кардиальный цирроз печени, как и циррозы печени другой этиологии, сопровождается диспротеинемией с преимущественным снижением уровня общего белка и альбуминов крови и нарастанием уровня у-глобулинов и а 2 -глобулинов.
Иногда клинические симптомы поражения печени у больных с острой или хронической недостаточностью кровообращения — тяжесть или боль в подложечной области, метеоризм, тошнота, горький вкус во рту, гепатомегалия и желтуха — выступают на передний план и нивелируют основное заболевание сердца. В таких случаях врачи допускают диагностические ошибки, предполагая самостоятельное заболевание печени.
При наличии сердечной недостаточности у больных с гепатомегалией необходимо учитывать возможность развития при циррозе печени хронического поражения сердца с гиперкинетическим синдромом, который клинически может проявляться цианозом, выраженной одышкой в покое и при нагрузке, тахикардией, высоким пульсовым давлением, расширением правого желудочка сердца вследствие значительного артериовенозного шунтирования крови в легких.
Поражение печени и сердца с гипердинамической или гиподинамической сердечной недостаточностью возможно и при идиопатическом гемохроматозе, амилоидозе, саркоидозе и хроническом алкоголизме. В редких случаях при циррозе печени или при длительной терапии ХАГ иммунодепрессантами возможно развитие подострого инфекционного эндокардита, который требует дифференциальной диагностики с хроническим активным заболеванием печени, так как протекает с гепатоспленомегалией, гиперпротеинемией, гипергамма-глобулинемией, положительными белково-осадочными пробами, умеренной гиперферментемией (аминотрансферазы, щелочная фосфатаза) и иногда с гипербилирубинемией, обусловленной сопутствующим реактивным гепатитом. Об инфекционном процессе говорят и гипер-а 2 -глобулинемия, резкое повышение СОЭ, аускультативные феномены, свидетельствующие о поражении клапанов сердца, васкулиты, тромбозы или эмболии внутренних органов, поражение почек и положительные результаты повторных бактериологических исследований крови.
Проводится патогенетическое лечение заболеваний сердца, сердечно-сосудистой и легочной недостаточности, что обычно приводит к регрессии клинических и биохимических проявлений кардиального цирроза печени.
Дополнительно назначают гепатопротекторы и витамины — антиоксиданты: легалон, симепар, эссенциале Н, ливолин, намацит, альвитил, генсамин, форматон, триовит, мультитабс с ß-каротином в обычных дозировках в течение 1-2 мес. При наличии хронического кардиального цирроза печени показано назначение гепабене в вышеописанных дозах. По показаниям проводят хирургическое лечение.
Редким заболеванием является отложение кальция в глиссоновой капсуле печени и перикарде при перикардите туберкулезной этиологии, классифицирующееся по старой терминологии как «панцирное сердце», при котором развивается псевдоцирроз Пика. При этом в некоторых случаях функциональное состояние печени улучшалось после хирургического удаления части кальцифицированного перикарда. В результате операции уменьшались явления хронической сосудистой недостаточности и как следствие проявления «застойной» мускатной печени.
источник
29. Сердечная недостаточность: 1) причины осн и хсн 2) морфология осн 3) изменения печени при хсн 4) изменения легких при хсн 5) Изменения других внутренних органов и серозных полостей при хсн
1) Сердечная недостаточность — патологическое состояние, обусловленное неспособностью сердца обеспечить адекватное кровоснабжение органов и тканей.
Причины ОСН: 1. ИБС и ИМ 2. тромбоэмболия легочной артерии (ТЭЛА) 3. острые миокардиты
Причины ХСН: 1. ИБС в форме кардиосклероза 2. врожденные и приобретенные пороки сердца 3. хронические миокардиты и кардиомиопатии 4. артериальная гипертензия
2) Морфология ОСН: острое общее ВП, при левожелудочковой ОСН — полнокровие и отек легких (сердечная астма) с присоединением полнокровия органов БКК, при правожелудочковой ОСН — только полнокровие органов БКК:
а) плазматическое пропитывание (плазморрагия) и отек в тканях
б) стазы в капиллярах и множественные диапедезные кровоизлияния
в) дистрофические и некротические изменения в паренхиматозных органах
Изменения в органах при ОСН:
1. Легкие: острый отек и геморрагии (клинически пароксизмальная одышка, резкая нехватка воздуха, влажные хрипы над всеми легкими, откашливание кровянистой пенистой жидкости)
2. Почки: дистрофические и некротические изменения эпителия канальцев; почки увеличены в объеме, плотные, наиболее полнокровны мозговое вещество и пирамиды
3. Печень: центролобулярные кровоизлияния и некрозы
4. Селезенка: увеличена, капсула напряжена, с поверхности разреза обильно стекает кровь, МиСк: расширенные синусы, заполненные кровью
3) Изменения печени: МаСк: увеличена, плотная, края загруглены, поверхность разреза пестрая, серо-желтая с темно-красным крапом, напоминает мускатный орех (бурая индурация печени). МиСк: центральные отделы долек полнокровные, гепатоциты разрушены, на периферии гепатоциты в состоянии жировой дистрофии.
4) Изменения в легких: МаСк: увеличены, плотные, бурые (бурая индурация легких). МиСк: множественные диапедезные кровоизлияния, гемосидероз, склероз.
5) Изменения других внутренних органов при ХСН:
а) цианотическая индурация селезенки (увеличена, плотная, темно-вишневая, МиСк: атрофия фолликулов и склероз пульпы)
б) кожа: холодная, цианотичная; вены и лимфатические сосуды расширены и переполнены; выраженный отек дермы и подкожной клетчатки, разрастание в коже соединительной ткани; длительно не заживающие язвы
в) цианотическая индурация почек (большие, плотные, синюшные; полнокровие вен мозгового вещества и юкстамедуллярной зоны, дистрофия нефроцитов в условиях гипоксии, не выраженный склероз стромы)
г) слизистые: цианоз, повышенная продукция слизи (застойный катар)
д) распространенные отеки подкожной жировой клетчатки (анасарка) и скопление жидкости в полостях (гидроторакс, гидроперикард, асцит)
30. Тромбоз: 1) определение и отличие от посмертного свертывания 2) стадии тромбозообразования и их характеристика 3) причины и патогенез тромбоза 4) классификация тромбов по морфологии 5) исходы
1) Тромбоз — прижизненное свертывание крови в просвете сосуда или в полостях сердца. В отличие от тромба посмертные сгустки гладкие, блестящие, эластичные, свободно лежат в просвете вен (не образуются при смерти от асфиксии).
2) Стадии тромбообразования:
1. Агглютинация тромбоцитов: выпадение тромбоцитов из тока крови и прилипание к месту повреждения эндотелия → высвобождение агглютинирующего гиаломера тромбоцитами (периферическая зона) → дегрануляция тромбоцитов → высвобождение тромбопластического фактора и образование активного тромбопластина
2. Коагуляция фибриногена и образования фибрина (матрица для фибрина — оголенная центральная зона тромбоцитов — грануломер, содержащий ретрактозим пластинок): протромбин + активный тромбопластин + ионы Са 2+ → тромбин + фибриноген → фибрин-мономер + фибринстимулирующий фактор → фибрин-полимер → ретракция («сжатие») сгустка при участии ретрактозима
3. Агглютинация эритроцитов: присоединение к фибриновому сгустку и склеивание эритроцитов
4. Преципитация белков плазмы: осаждение белков плазмы на уже имеющемся свертке.
источник
Печень круглосуточно работает и терпит наши слабости, вредные привычки, стрессы, болезни и окружающий нас мир. Функций у печени очень много: она обезвреживает токсины, переваривает еду, поддерживает постоянство организма и выполняет еще много всякой работы.
С ухудшением экологии вследствие деятельности человека, распространением вирусных гепатитов и других инфекций, алкоголизма и наркомании, ухудшением качества пищи, малоподвижным образом жизни и с развитием фармацевтической промышленности нагрузка на нашу печень значительно выросла. И когда все это сваливается одновременно и в большом количестве, печень может не справляться, и тогда развивается риск развития печеночной недостаточности, которая, в свою очередь, может привести к необратимым процессам в организме и к смерти больного.
И так, печеночная недостаточность – это патологическое состояние, синдром, характеризующийся поражением печеночных клеток и нарушением работы печени с потерей ее компенсаторных возможностей и основных функций, проявляется хронической интоксикацией организма. Печеночная недостаточность может привести к печеночной коме, то есть, полному отказу печени и обширному поражению головного мозга продуктами распада.
Немного статистики!
- От печеночной недостаточности умирает от 50 до 80% всех случаях заболевания.
- В мире каждый год умирает в среднем две тысячи человек по причине печеночной недостаточности.
- В 15% случаев печеночной недостаточности не удается объяснить причину ее развития.
- Самые частые причины развития печеночной недостаточности – поражение печени алкоголем, лекарственными препаратами и вирусными гепатитами.
Интересные факты!
- Печень имеет около 500 функций, а за одну минуту в ней происходит более 20 000 000 химически реакций.
- При проведении экспериментов на животных выяснили, что после удаления печени, животные находятся в нормальном состоянии на протяжении 4-8 часов, а через 1-2 суток умирают в состоянии печеночной комы.
- Цирроз печени всегда проявляется печеночной недостаточностью.
- Болезнь Боткина, или вирусный гепатит А, у людей старше 40 лет с наличием в анамнезе заболеваний печени и желчного пузыря в 40% случаев приводит к печеночной недостаточности. Вирусный гепатит А среди народа принято считать заболеванием детского возраста, которое достаточно легко переносится (приравнивают к ветряной оспе, краснухе, скарлатине и так далее).
- Вирусный гепатит Е у беременных в 20% заканчивается печеночной недостаточностью, в то время как, у мужчин и небеременных женщин вирусный гепатит Е может не проявляться вовсе.
- Прием такого, казалось бы, обычного препарата, как парацетамол, может привести к развитию молниеносного течения печеночной недостаточности (фульминантная печеночная недостаточность). А парацетамол во многих странах принято принимать в больших дозах при банальной простуде и ОРВИ.
- Именно от печеночной недостаточности большинство людей умирает вследствие отравления ядовитыми грибами (бледные поганки, мухоморы и другие).
- В большинстве случаев печеночной недостаточности у взрослых, помимо других причин развития синдрома, выявляется факт злоупотребления алкоголем.
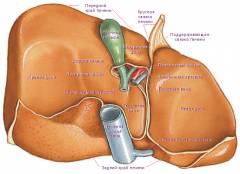
Характеристика печени:
- вес – около 1,5 кг,
- форма – грушевидная,
- нормальные размеры печени у взрослых:
- длина по косой линии – до 15 см,
- длина правой доли – 11,0-12,5 см,
- длина левой доли – 6-8 см,
- высота – 8-12 см,
- толщина – 6-8 см,
- края печени – ровные,
- консистенция – мягкая,
- структура – однородная,
- поверхности – блестящие и гладкие,
- цвет – бурый,
- покрыта брюшиной – серозной оболочкой, которая ограничивает органы брюшной полости.
- обладает способностью к регенерации (восстановлению).
Различают поверхности печени:
- диафрагмальная поверхность – соответствует форме диафрагмы,
- висцеральная (обращенная к органам) поверхность – прилежит к окружающим органам,
- нижний край – под острым углом,
- верхнезадний край – под тупым углом, закругленный.
С помощью серповидной печеночной связки, а также двух продольных и поперечной бороздой печень делится на доли:
- правая доля,
- левая доля,
- квадратная доля,
- хвостовая доля.
От серповидной связки печени отходит круговая связка, которая представляет собой преобразованную пупочную вену, которая в утробе матери соединяла плаценту с плодом.
Между квадратной и хвостовой долями печени, в правой продольной борозде находятся ворота печени, которые включают в себя структуры:
- печеночная артерия,
- портальная вена,
- желчный проток,
- нервы и лимфатические сосуды.
Восстановление печени происходит путем пролиферации гепатоцитов (роста и увеличения их количества), хотя почему это происходит до сих пор ученым не известно.
Скорость регенерации печени напрямую зависит от возраста. У детей скорость восстановления органа и объем, до которого он восстанавливается больший, чем у пожилых людей. Регенерация происходит медленно: так у детей этот период составляет 2-4 недели, а у пожилых людей – от 1 месяца. Скорость и объем регенерации также зависит от индивидуальных особенностей и заболевания, которое вызвало ее повреждение.
Восстановление печени возможно только при устранении причин развития гепатита, уменьшения на нее нагрузки, а также при поступлении в организм нормального количества полезных питательных веществ.
Не восстанавливается печень в случае наличия в ней активного инфекционного процесса (при вирусных гепатитах).
В сутки печенью выделяется огромное количество желчи – до 1 литра, не менее полулитра.
Основная функция желчи – переваривание жиров в кишечнике, за счет эмульгирования желчными мицеллами.
Желчные мицеллы – это частицы компонентов желчи, окруженные ионами, часть коллоида.
Желчь бывает:
- Молодая или печеночная желчь – выделяемая непосредственно из печени, минуя желчный пузырь, имеет желтоватый соломенный цвет, прозрачная.
- Зрелая или пузырная желчь – выделяется из желчного пузыря, имеет темный оливковый цвет, прозрачная. В желчном пузыре из желчи всасывается жидкость и выделяется слизь (муцин), таким образом, желчь становится вязкой и концентрированной.
- Базальная желчь – смесь молодой и зрелой желчи, которая поступает в двенадцатиперстную кишку, золотистого желтого цвета, прозрачная.
Что входит в желчь?
- Вода – в желчи часть воды составляет около 97%, в ней растворены основные компоненты желчи.
- Желчные кислоты:
- холевая и хенодезоксихолевая кислоты – первичные желчные кислоты,
- гликохолевая и таурохолевая кислоты (соединения с аминокислотами),
- дезоксихолевая и литохолевая кислоты (вторичные желчные кислоты, образуются в кишечнике под действием кишечной микрофлоры).
Желчные кислоты образуются из холестерина в гепатоцитах. В желчи они находятся в виде солей и анионов. Роль желчных кислот велика в переваривании жиров и всасывании жирных кислот и триглицеридов в кишечнике. Часть желчных кислот всасывается в кишечнике обратно в кровь, и снова попадают в печень.
- Желчные пигменты:
- билирубин
- биливердин.
Желчные пигменты образуются из гемоглобина в селезенке и в клетках Купфера. Любой эритроцит образуется в красном костном мозге (эритропоэз) и разрушается в селезенке, и небольшая их часть в печени. Эритроциты содержат в себе гемоглобин, который переносит на себе атомы кислорода и углекислого газа, то есть осуществляет газообмен в тканях. После разрушения эритроцита стоит вопрос об утилизации гемоглобина. Желчные пигменты – промежуточные продукты распада гемоглобина, с помощью желчи они выводятся из организма.
Эти пигменты окрашивают желчь в желтый, зеленый и коричневый цвета. А также после связывания с кислородом незначительно окрашивает мочу (уробилиноген) и кал (стеркобилиноген).
- Печеночные фосфолипиды (лецитины) – образуются путем синтеза фосфолипидов, которые поступают с пищей. Отличается от обычных фосфолипидов тем, что на них не действуют ферменты поджелудочной железы, а в неизмененном виде вместе с желчными кислотами участвуют в переваривании жиров и частично всасываются обратно в кровь и поступают в гепатоциты, а затем в желчь.
- Холестерин – в желчи находится в свободном виде или в виде синтезированных из него желчных кислот. Поступает в организм вместе с пищей. Участвует в переваривании жиров в кишечнике.
- Ионы:
- натрий,
- кальций,
- калий,
- хлор,
- бикарбонаты
Ионы попадают в кровь и печень вместе с едой. Главная их роль – улучшение проницаемости клеточных стенок, а также ионы входят в состав мицеллы в тонком кишечнике. За счет них происходит всасывание воды из желчи в желчном пузыре и ее концентрация, а также улучшение всасывания питательных веществ в кишечной стенке.
Также в желчи содержаться иммуноглобулины, тяжелые металлы, и чужеродные химические соединения, которые попадают из окружающей среды.
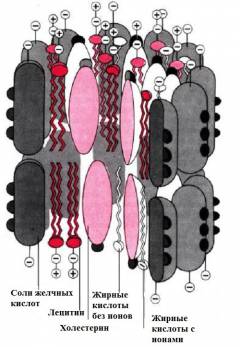
- Образование желчи – желчь способствует расщеплению и всасыванию жира в кишечнике.
- Обезвреживание токсинов и других инородных веществ, поступающих из вне, преобразовывая их в безвредные вещества, которые, в свою очередь, выводятся почками с мочой. Это происходит с помощью химических реакций в гепатоцитах (биотрансформация). Биотрансформация осуществляется за счет соединения с белками, ионами, кислотами и другими химическими веществами.
- Участие в белковом обмене – образование мочевины из продуктов распада белковых молекул – аммиака. При повышенном количестве аммиак становится ядом для организма. Мочевина из печени попадает в кровь, а далее выводится с почками.
- Участие в углеводном обмене – при избытке глюкозы в крови печень синтезирует из нее гликоген – реакция гликогенеза. Печень, а также скелетная мускулатура являются депо для запаса гликогена. При нехватке глюкозы в организме гликоген трансформируется в глюкозу – реакция глюкогенолиза. Гликоген – запас глюкозы в организме и энергия для работы скелетно-мышечной системы.
- Участие в жировом обмене – при недостатке жиров в организме печень способна углеводы (а именно гликоген) синтезировать в жиры (триглицериды).
- Утилизация продуктов распада гемоглобина путем преобразования его в желчные пигменты и выведение их с желчью.
- Кроветворение у плода во время беременности. Печень также участвует в образовании факторов свертываемости крови.
- Разрушение и утилизация избытка гормонов, витаминов и других биологически активных веществ.
- Депо для некоторых витаминов и микроэлементов, таких, как витамины В12, А, Д.
| Причины развития данного заболевания | Что происходит в печени? | |
| Цирроз печени |
| Процесс развития цирроза печени длительный, иногда длиться годами. Под действием гепато-токсических факторов постоянно происходит частичное разрушение гепатоцитов, но благодаря регенерационной функции печени гепатоциты частично восстанавливаются. При длительном непрекращающемся воздействии токсических факторов, при подключении аутоиммунных процессов, меняется генный материал печеночных клеток. При этом печеночная ткань постепенно начинает замещаться соединительной тканью (не имеющей специализированных функций). Соединительная ткань деформирует и перекрывает печеночные сосуды, что повышает давление в портальной вене (портальная гипертензия), как результат – появление сосудистых анастомозов между портальной и нижней полой венами, появление жидкости в брюшной полости – асцит, увеличение селезенки – спленомегалия. Печень при этом уменьшается в размерах, сморщивается, появляется синдром печеночной недостаточности. |
| Дистрофии печени (гепатозы):
|
| Поступление в печень избыточного количества жира (также повышенное содержание в печени углеводов, усиленные затраты гликогена) или затруднение выхода жиров из печени (недостаток белков, нарушение ферментной работы печени) приводят к отложению «лишнего» жира (триглицеридов) в цитоплазме гепатоцитов. Жир накапливается и постепенно разрывает гепатоцит. Жировая ткань постепенно замещает печеночную ткань, что приводит к синдрому печеночной недостаточности. |
|
| Различают три вида белковой дистрофии печени:
|
|
| Гликоген в норме депонируется в цитоплазме гепатоцитов. При развитии углеводной дистрофии гликоген накапливается не в цитоплазме, а в ядре гепатоцита. При этом гепатоциты значительно увеличиваются в размерах. При длительном процессе наступает гибель гепатоцитов или развивается соединительная ткань (цирроз печени). Исход – печеночная недостаточность. |
|
| Амилоидоз – системное заболевание, связанное с нарушением работы иммунной системы, характеризуется отложением амилоида (нерастворимого белка) в стенке печеночных сосудов и желчных ходов. Амилоид вырабатывается в мутирующих иммунных клетках: плазматических клетках, эозинофилах, иммуноглобулинах и так далее. Уплотненные сосуды печени не могут полноценно работать, наблюдается застой желчи в печени, портальная гипертензия (повышение давления в портальной вене), а далее печеночная недостаточность. |
| Гепатиты – воспаление печени |
| Патогенез вирусных гепатитов достаточно сложный. Но основную роль в поражении гепатоцитов играет иммунитет. Если при вирусных гепатитах А и Е иммунитет способствует высвобождению гепатоцитов от вируса, то при вирусных гепатитах В, D, и F иммунитет поражает зараженные гепатоциты вместе с вирусом. А когда вырабатываются специальные иммуноглобулины, иммунитет все-таки выводит вирусы из печеночных клеток и наступает выздоровление. Выздоровление от всех вирусных гепатитов возможно только при устранении других гепато-токсических факторов, в противном случае развивается хронический гепатит, некроз или цирроз печени, а исход – печеночная недостаточность. При вирусном гепатите С (специалисты его называют «ласковым убийцей»), элиминация вируса не наступает из-за его изменчивости. А исход этого заболевания – хронический гепатит, цирроз или рак печени, а далее печеночная недостаточность. Алкогольный, лекарственный, токсический гепатиты имеют схожие механизмы развития. Гепато-токсические факторы частично разрушают гепатоциты – возникает гепатит. Затем присоединятся аутоиммунный процесс. При длительном его течении возможно развитие некроза печени и печеночной недостаточности. |
| Рак печени |
| Раковые клетки разрастаются и замещают или сдавливают гепатоциты. При этом печень постепенно утрачивает свои функциональные возможности за счет поражения клеток, нарушения оттока желчи и нарушения кровообращения в системе печеночных вен (портальная гипертензия). При разрушении гепатоцитов раковыми клетками, выделяется большое количество продуктов распада от разрушенных клеток, что дополнительно способствует интоксикации. |
| Паразитарные заболевания печени |
| Гельминты (глисты) попадая в печень, живут там, растут и размножаются. Когда их количество и размеры значительно увеличиваются, они могут способствовать застою желчи в печени, сдавливать печеночные сосуды, повышая давление в портальной вене, их токсины действуют на гепатоциты, повреждая их. При длительном течении возможно развитие печеночной недостаточности. При наличии эхинококка, кисты могут разорваться с обсеменением всей печени, что может привести к острой печеночной недостаточности. |
| Расстройства кровообращения |
| При портальной гипертензии нарушается кровообращение и в печеночной дольке, вследствие чего формируются сосудистые анастомозы между портальной и нижней полой венами, а кровь в печень не поступает в полном объеме, проходя по анастомозам, в результате вен нарушается трофика печени. Возможно развитие некроза печеночных клеток и печеночной недостаточности. Помимо печеночных проблем при портальной гипертензии развивается варикозное расширение вен в портальной системе, а также перегрузка лимфатической системы, которая перестает полностью собирать жидкость из брюшной полости. Развиваются осложнения портальной гипертензии:
|
Также к печеночной недостаточности могут привести внепеченочные причины:
- гипо- или авитаминозы,
- хроническая почечная недостаточность (ХПН),
- гормональные заболевания,
- недостаток кислорода в организме, включая анемии,
- массивные кровопотери,
- переливание несовместимой группы крови,
- хирургические операции в брюшной полости.
Острая печеночная недостаточность – вид печеночной недостаточности, который развивается в результате быстрого поражения печени. Клиническая картина этого синдрома развивается очень быстро (от нескольких часов до 8 недель) и также скоро приводит к печеночной энцефалопатии и коме.
Также возможно молниеносное развитие печеночной недостаточности – фульминантная печеночная недостаточность, которая чаще возникает при отравлении ядами, химикатами, лекарственными препаратами и так далее.
Причины, которые могут привести к острой печеночной недостаточности:
- вирусные гепатиты с тяжелым течением,
- прием лекарственных препаратов, особенно вместе с алкоголем,
- обширные потери крови и ДВС-синдром (диссеминированное сосудистое свертывание крови, связано с нарушением системы свертывания крови в результате массивного кровотечения или выраженного интоксикационного синдрома, может привести к смерти пациента, требует реанимационных мероприятий),
- переливание несовместимой группы крови,
- отравление ядовитыми грибами,
- отравление ядохимикатами,
- отравление алкоголем,
- острые нарушения кровообращения в печеночных сосудах, а также в системах воротной и нижней полой вен,
- разрыв эхинококковой кисты и другие распространенные паразитарные заболевания печени,
- оперативные вмешательства на брюшной полости,
- обезвоживание, нарушение водно-солевого баланса, откачивание большого объема жидкости из брюшной полости при асците.
- острая или хроническая почечная недостаточность (ОПН и ХПН),
- проявление печеночной недостаточности как один из синдромов полиорганной недостаточности, которая возникает в результате распространенных инфекционных процессов или тяжелые поражения головного мозга и характеризуется отказом жизненно-важных органов (легочная, сердечная, почечная недостаточность, отек мозга, парез кишечника и так далее),
- любые хронические заболевания печени (цирроз, гепатиты, гепатозы, заболевания желчевыводящих путей и другие) при несоблюдении лечебных мероприятий и режима, наличии дополнительных факторов негативного воздействия на печень (например, прием алкоголя, несоблюдение диеты, прием гепато-токсических лекарственных препаратов и так далее).
Механизм развития острой печеночной недостаточности:
В зависимости от причин развития различают формы острой печеночной недостаточности:
- Эндогенная или печеночно-клеточная форма – возникает при поражении клеток печени в результате воздействия на них гепато-токсических факторов. Характеризуется быстрым некрозом (или отмиранием) гепатоцитов.
- Экзогенная форма – развивается в результате нарушения печеночного и/или внепеченочного кровообращения (в системах портальной и нижней полой вен), чаще всего при циррозе печени. При этом кровь с токсическими веществами минует печень, воздействуя на все органы и системы организма.
- Смешанная форма – при воздействии как печеночно-клеточных, так и сосудистых факторов нарушения работы печени.
После развития острой печеночной недостаточности все токсины, которые поступают из окружающей среды или образуются в результате обмена веществ, оказывают негативное влияние на клетки всего организма. При поражении головного мозга наступает печеночная энцефалопатия, затем, кома и смерть пациента.
Острая печеночная недостаточность – крайне тяжелое состояние организма, требующее немедленной дезинтоксикационной терапии.
Прогноз заболевания – в большинстве случаев, неблагоприятный, шанс на восстановление жизненных функций печени зависит от способности печени к регенерации (ее компенсаторных возможностей), времени до начала лечебных мероприятий, степени поражения головного мозга и устранения гепато-токсических факторов. Сама острая печеночная недостаточность – обратимый процесс. А из печеночной комы выходят только в 10-15% случаев.
Хроническая печеночная недостаточность – вид печеночной недостаточности, который развивается постепенно при длительном (хроническом) воздействии гепато-токсических факторов (от 2-х месяцев до нескольких лет).
Характеризуется постепенным развитием симптомов на фоне обострения хронических заболеваний печени и желчевыводящей системы.
Причины хронической печеночной недостаточности:
- алкоголизм,
- вирусные гепатиты, особенно В и С,
- цирроз печени,
- длительный прием некоторых лекарственных препаратов,
- опухоли печени,
- паразитарные заболевания печени,
- дискинезии желчевыводящих путей и желчекаменная болезнь,
- гепатозы (печеночные дистрофии),
- сахарный диабет и другие эндокринные заболевания,
- хронические инфекционные заболевания (сифилис, туберкулез),
- аутоиммунные заболевания,
- анемии и другие заболевания крови,
- другие заболевания и состояния.
Механизм развития хронической печеночной недостаточности:
Как и при острой печеночной недостаточности различают формы:
- экзогенная форма – поражение и некроз печеночных клеток происходит постепенно, часть клеток регенерируется, но при продолжении воздействия неблагоприятных факторов, отмирание гепатоцитов продолжается.
- эндогенная форма – нарушение кровообращения печени,
- смешанная форма.
При хронической печеночной недостаточности более развиты компенсаторные возможности печени, то есть у печени есть время восстановить часть своих клеток, которые частично продолжают выполнять свои функции. Но токсины, которые не утилизируются в печени, попадают в кровь и хронически отравляют организм.
При наличии дополнительных гепато-токсических факторов происходит декомпенсация (утеря возможностей регенерации гепатоцитов), при этом может развиться печеночная энцефалопатия и далее кома и летальный исход.
Факторы, которые могут привести к энцефалопатии и коме при хронической печеночной недостаточности:
- употребление алкоголя,
- самостоятельный прием лекарств,
- нарушение диеты, употребление в пищу большого количества белков и жиров,
- нервный стресс,
- распространенный инфекционный процесс (сепсис, грипп, менингококцемия, ветряная оспа, туберкулез и другие),
- беременность, роды, прерывание беременности,
- обезвоживание,
- операции на брюшной полости и так далее.
Течение – тяжелое. С нарастанием печеночной недостаточности постепенно ухудшается и состояние пациента.
Заболевание требует неотложного адекватного лечения и дезинтоксикации.
Прогноз: неблагоприятный, в 50-80% случаев печеночной энцефалопатии наступает смерть больного. При компенсированной хронической печеночной недостаточности возможно восстановление печени только при устранении всех гепато-токсических факторов и проведения адекватной терапии. Часто хроническая печеночная недостаточность на ее начальных стадиях протекает бессимптомно и диагноз можно поставить только на основании данных целенаправленных обследований. Это является причиной несвоевременной диагностики и лечения заболевания, что значительно снижает шансы на выздоровление.
| Критерии | Острая печеночная недостаточность | Хроническая печеночная недостаточность |
| Сроки развития | От нескольких дней до 8 недель. | От 2-х месяцев до нескольких лет. |
| Механизм развития | Развивается в результате быстрого некроза печеночной ткани или резкого нарушения кровообращения печени. | Некроз печени происходит постепенно, часть поврежденных клеток успевает регенерироваться, печень способна частично компенсировать свои функции. Также может развиться при постепенном нарушении кровообращения. |
| Степень поражения печени | Быстрое поражение более 80-90% всех клеток печени. | Постепенное поражение более 80% гепатоцитов. Хроническая печеночная недостаточность практически всегда способствует развитию симптомов портальной гипертензии, в отличие от острого течения печеночной недостаточности, при которой портальная гипертензия не является обязательным симптомом. |
| Тяжесть течения | Течение заболевания крайне тяжелое, тяжелее, чем при хронической печеночной недостаточности. | Течение тяжелое, на начальных стадиях возможно бессимптомное течение. |
| Прогноз | Прогноз неблагоприятный, часто развивается печеночная энцефалопатия, а затем и кома. Но процесс обратимый при своевременных лечебных мероприятиях и устранении гепато-токсических факторов. | Прогноз неблагоприятный, при отсутствии своевременного лечения и устранения провоцирующих факторов приводит рано или поздно к печеночной энцефалопатии. Хроническая печеночная недостаточность – необратимый процесс. Лечение направлено для предупреждения развития печеночной комы. |
| Группа симптомов | Симптом | Как проявляется | Механизм возникновения |
| Синдром холестаза | Желтуха | Окрашивание кожных покровов и видимых слизистых оболочек в желтые оттенки: от зеленого и лимонного до оранжевого цвета. У смуглых людей желтуха может быть заметной только на слизистых оболочках, особенно на склерах глазных яблок. | Синдром холестаза связанный с нарушением оттока желчи из печени. Это происходит из-за сдавливания желчевыводящих путей и неспособностью поврежденных гепатоцитов вывести желчь. При этом продукт распада гемоглобина билирубин не выводится с желчью и калом. В крови наблюдается большое количество желчных пигментов (билирубина и биливердина), которые обеспечивают окрашивание всех тканей в цвет желчи. А вот кал лишается окрашивания стеркобилином. Лишний билирубин из крови пытаются вывести почки, при этом наблюдается повышенное содержание желчных пигментов в моче, и как результат – ее более интенсивное окрашивание. Повышенное количество билирубина также оказывает токсико-аллергическое действие на кожу, что способствует развитию зуда. |
| Обесцвечивание кала | Кал приобретает светлый цвет, вплоть до белого и бежевого. | ||
| Потемнение мочи | Цвет мочи становится темнее, его сравнивают с оттенками темного пива. | ||
| Зуд кожных покровов | Больного с наличием холестаза сопровождает зуд по всему телу, при этом сыпи может и не быть. | ||
| Боль в правом подреберье | Не обязательный симптом при печеночной недостаточности. Боли могут появляться после приема пищи, носят ноющий или спазмирующий характер. | Боли в правом подреберье возникают из-за обструкции желчевыводящих сосудов. При этом желчь распирает желчные ходы и сдавливают дольковые нервы. | |
| Диспептические расстройства | Тошнота, рвота, нарушение стула, снижение и извращение аппетита. | Тошнота и рвота связаны с приемом пищи, носят периодический или постоянный характер. Расстройства стула в виде поноса, более 3 раз в сутки. Аппетит плохой, вплоть до отказа от приема пищи. У некоторых пациентов появляется желание попробовать несъедобное (землю, мел, волосы, несовместимые продукты питания и другое). | Нарушение пищеварения связаны с неспособностью печени участвовать в переваривании жиров. Снижение аппетита может быть еще и признаком поражения нервной системы и интоксикации, которая развивается на фоне некроза печени. |
| Интоксикационные симптомы | Повышение температуры тела, слабость, недомогание, боль в суставах (артралгия), потеря аппетита. | Температура тела может повышаться до высоких цифр или носить постоянный субфебрильный характер (до 38С). Слабость и недомогание слабовыраженные или приковывают больного к постели. Артралгия в крупных или во всех группах суставов. | Интоксикационные симптомы развиваются в результате попадания в кровь продуктов распада тканей печени. При острой печеночной недостаточности эти симптомы более выражены, чем при хронической форме. Также интоксикацию могут обуславливать вирусные гепатиты, в этом случае в кровь попадают не только токсины разрушенной печени, но и токсины, выделяющиеся в процессе жизнедеятельности вируса. |
| Изменение размеров печени | Увеличение печени (гепатомегалия) | Эти изменения в печени может определить врач при помощи пальпации живота, а также при проведении дополнительных методов исследований. | Увеличение печени – частый симптом печеночной недостаточности, связанный с нарушениями кровообращения в печеночных сосудах, холестазом, наличием гепатоза, а также опухолей, кист, абсцессов, туберкулом и так далее. |
| Уменьшение печени | Уменьшение печени наблюдается при циррозе печени, когда печеночная ткань полностью замещается соединительной тканью. | ||
| Синдром портальной гипертензии | Асцит | Живот значительно увеличивается в размерах, напоминая беременность. | Асцит – накопление жидкости в брюшной полости. Его развитие связано с нарушением проходимости лимфатических сосудов, которое развивается в результате их сдавливания в печени расширенными печеночными сосудами. Лимфатическая система способствует дренажу жидкости в мягких тканях. |
| Сосудистые звездочки | Сосудистые звездочки представляют собой расширение сосудов, внешне напоминают медузы. Появляются на передней стенке живота и на плечах. | Сосудистые звездочки – это расширенные сосуды, которые отходят от портальных вен. На фоне портальной гипертензии развиваются анастомозы – дополнительные (аномальные) сосуды, которые соединяют более крупные вены между собой. Таким образом, организм пытается восстановить нарушенное кровообращение. | |
| Спленомегалия – увеличение селезенки | Этот симптом можно определить с помощью пальпации живота и инструментальных методов исследования. | Спленомегалия развивается из-за нарушения кровообращения в селезенке, которая является депо крови. Она кровоснабжается с системы портальной и нижней полой вен. При повышении давлении в этих сосудах, в селезенке депонируется большее количество крови. Также селезенка берет на себя некоторые функции печени, в частности – разрушение эритроцитов и утилизация гемоглобина. | |
| Кровотечение из расширенных вен пищевода | Наблюдается рвота кровавым содержимым (или «кофейной гущей»), иногда остатки крови выявляют только в кале (мелена). Оно бывает острым или хроническим. Объем кровопотери также индивидуально отличается. Необходимо дифференцировать от легочного кровотечения, когда выделяемая кровь ярко алого цвета, с пузырьками воздуха. Опасна аспирация кровью (попадание крови в легкие – удушье). | Вены пищевода расширяются на фоне портальной гипертензии. Постоянно и длительно расширенные сосуды теряют свою подвижность и проницаемость, поэтому и возникает из них кровотечение. Кровотечению способствует также нарушение свертываемости крови (связано с нарушениями функции печени, одной из которых является синтез некоторых факторов свертываемости). | |
| Печеночная энцефалопатия | Нарушение работы нервной системы |
| Продукты обмена и токсины не обезвреживаются в печени из-за ее недостаточности, и воздействуют на структуры головного мозга, развивается энцефалопатия. Дальнейшее поражение головного мозга может привести к печеночной коме. |
| Легочные симптомы | Одышка, кашель | Больные могут предъявлять жалобы на затруднение дыхания, его учащение (более 20 в одну минуту в покое для взрослых). Одышка сначала проявляется во время физических нагрузок, а затем и во время покоя, особенно в положении лежа. Во время сна могут быть приступы резкого учащения дыхания (у больного развивается страх задохнуться). Для облегчения дыхания больные занимают вынужденное положение сидя. Также может быть кашель с выделением кровянистой мокроты с пузырьками. | Появление легочных симптомов связано с нарастанием отека легких. Отек легких – кровенаполнение легочных сосудов. Это происходит из-за нарушения белкового обмена в результате поражения печени. Кровь начинает просто пропотевать через стенки сосудов в альвеолы. Развитие этого симптома опасно для жизни, так как при заполнении альвеол жидкостью полностью, возможна остановка дыхания. |
| Нарушение кровообращения | Повышение артериального давления, аритмия сердца. | Повышение артериального давления свыше 140/90 мм рт. ст. Артериальная гипертензия вскоре сменится гипотонией, снижением давления ниже 90/60 мм рт. ст. Аритмия сердца сначала проявляется в виде брадикардии (менее 60 ударов в час), а затем, в виде тахикардии (более 90 ударов в час). | Нарушение общего кровообращения связаны с портальной гипертензией. При наличии отеков и асцита жидкость в большом количестве покидает кровеносное русло, попадает в мягкие ткани. При этом снижается артериальное давление. С этими изменениями в кровеносном русле связана и работа сердца, появляется аритмия. |
| Атрофия мышц | Мышечная слабость | Мышцы уменьшаются в размерах, становятся дряблыми, слабыми. Больному тяжело выполнить даже самые простые физические упражнения. | Атрофия мышц связана с недостатком гликогена – основного источника энергии для работы мускулатуры. Преобразование глюкозы в гликоген происходит в печени, а при печеночной недостаточности гликоген практически не синтезируется. После использования запасенного гликогена, постепенно нарастает атрофия скелетной мускулатуры. |
| Нарушение свертываемости крови | Кровотечения | Кровотечения из расширенных вен пищевода, из сосудов желудка¸ носовые кровотечения, геморрагическая сыпь (как синяки) и так далее. | Нарушение свертываемости крови наступает из-за невыполнения печенью функции – образования факторов свертываемости крови. При этом кровь становится «жидкой», а кровотечение остановить крайне тяжело. |
Также при печеночной недостаточности может развиться анемия, легочно-сердечная недостаточность, острая или хроническая почечная недостаточность, парез кишечника. Страдают абсолютно все органы и системы организма.
При печеночной недостаточности характерен специфический печеночный запах изо рта.
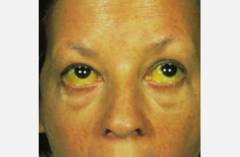
Стадии острой печеночной недостаточности:
- Латентная стадия печеночной энцефалопатии – на этой стадии у пациентов нет жалоб, и нет ярко выраженных симптомов поражения печени. Изменения можно выявить только при обследовании.
- I стадия печеночной энцефалопатии – прекома. При этом нарастают симптомы печеночной недостаточности: синдромы холестаза, портальной гипертензии, интоксикационные симптомы, появляются первые симптомы поражения нервной системы в виде ее торможения.
- II стадия печеночной энцефалопатии – прекома. В этой стадии наблюдается отягощение состояния пациента, нарастают симптомы печеночной энцефалопатии, торможение сменяется возбуждением нервной системы, появляются немногочисленные патологические рефлексы. Более ярко становятся выраженными симптомы нарушения свертываемости крови, нарастает интоксикация, печень резко уменьшается в размерах, при пальпации ее выявить не удается (симптом «пустого подреберья»). На этой стадии появляется печеночный запах изо рта.
- Кома – потеря сознания, больной проявляет рефлексы только на более сильные раздражители, появляются признаки полиорганной недостаточности (одновременное течение печеночной, легочной, сердечной, почечной недостаточности, отека мозга).
- Глубокая кома – больной без сознания, наблюдается полное отсутствие рефлексов на любые раздражители в результате отека головного мозга, развивается полиорганная недостаточность. В большинстве случаев – это необратимый процесс, наступает смерть пациента.
Главной особенностью острой печеночной недостаточности является то, что каждая стадия длиться от нескольких часов до нескольких дней, реже недель.
Благоприятным фактом является возможность обратимости процесса в случае своевременной дезинтоксикационной терапии на ранних стадиях.
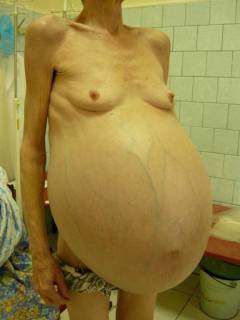
Стадии хронической печеночной недостаточности:
- I стадия – функциональные возможности печени еще сохранены. Эта стадия характеризуется появлением диспептических расстройств, слабовыраженной интоксикации (слабость, сонливость).
- II стадия – нарастание диспептических расстройств, интоксикации, появление симптомов поражения нервной системы в виде торможения, потери памяти, нарушения координации движения. Появляется печеночный запах изо рта. На этой стадии возможны кратковременные потери памяти. На этом этапе печень лишь частично выполняет свои функции.
- III стадия – значительное снижение функциональных возможностей печени. Ранее появившиеся симптомы становятся более выраженными. Появляются проявления холестаза и портальной гипертензии, нарушения свертываемости крови, отягощение состояния нервной системы (выраженная слабость, нарушение речи).
- IV стадия (печеночная кома) – печень полностью погибает и совсем не функционирует. Наблюдается потеря сознания, снижение рефлексов, затем их отсутствие. Развивается отек головного мозга. Нарастает полиорганная недостаточность. Чаще всего – это необратимый процесс, больной погибает.
Особенности клинических проявлений хронической печеночной недостаточности:
- каждая ее стадия развивается постепенно, неделями, месяцами, годами;
- обязательными симптомами являются проявления портальной гипертензии;
- все симптомы менее выражены, чем при остром течении синдрома.
- хроническая печеночная недостаточность – необратимый процесс и рано или поздно приведет к печеночной энцефалопатии и коме.
Лабораторная диагностика позволяет оценить функциональное состояние печени, степень ее поражения.
| Показатели | Норма показателей* | Изменения при печеночной недостаточности | ||
| Общий билирубин | Общий билирубин: 8 – 20 мкмоль/л, непрямой билирубин: до 15 мкмоль/л, прямой билирубин: до 5 мкмоль/л. | Значительное повышение показателей желчных пигментов – в 50-100 раз и более, до 1000 мкмоль/л. Печеночная энцефалопатия наступает при уровне билирубина более 200 мкмоль/л. | ||
| АлТ (аланинаминотрансфераза) | 0,1 – 0,68 мкмоль/л или до 40 МЕ | Трансаминазы – это ферменты, которые выделяются из разрушающихся клеток печени или сердца. Чем больше трансаминазы, тем более выражен процесс некроза печеночной ткани. При печеночной недостаточности трансаминазы повышаются в десятки раз. При полном разрушении печени отмечается резкое снижение показателей трансаминаз. | ||
| АсТ (аспартатаминотрансфераза) | 0,1 – 0,45 мкмоль/л или до 40 МЕ | |||
| Тимоловая проба | 0 – 5 ЕД – негативная проба. | Тимоловая проба – определение качественного соотношения белковых компонентов сыворотки крови. Положительная проба указывает на наличие нарушения белкового обмена, практически всегда положительна при печеночной недостаточности. | ||
| Коэффициент Де Ритиса | 1,3 – 1,4 | Этот коэффициент отражает соотношение АсТ к АлТ. При печеночной недостаточности вследствие хронических заболеваний печени этот показатель повышается более 2. А при остром процессе вирусного гепатита наоборот уменьшается менее 1. | ||
| ГГТ (гамма-глутаматтрансфераза) | 6 – 42 ЕД/л для женщин, 10 – 71 ЕД/л для взрослых. | ГГТ – фермент, участвующий в обмене белка. При печеночной недостаточности этот показатель может увеличиваться в несколько раз, если у пациента есть симптомы застоя желчи. Интересно, ГГТ используют наркологи в диагностике алкоголизма. | ||
| Глюкоза | 3,3 – 5,5 ммоль/л | Наблюдается снижение уровня глюкозы или, реже, его повышение, это обусловлено нарушением углеводного обмена, в котором печень играет важную роль. | ||
| Мочевина | 2,5 – 8,3 ммоль/л | При печеночной недостаточности наблюдается снижение уровня мочевины, это связано с нарушениями белкового обмена, отсутствием синтеза мочевины в печени из аммиака – продуктов распада белка. | ||
| Общий белок, глобулины, альбумины | Общий белок: 65 – 85 г/л, глобулины: 20 – 36 г/л, альбумины: 30 – 65 г/л | Снижение уровня общего белка, альбуминов и глобулинов происходит из-за нарушения белкового обмена | ||
| Холестерин | 3,4 – 6,5 ммоль/л | Повышение уровня холестерина наблюдается при выраженном синдроме холестаза, но при дальнейшем некрозе печени происходит резкое снижение уровня холестерина. | ||
| Железо | 10 – 35 мкмоль/л | Повышение уровня железа в крови связано с некрозом гепатоцитов, в которых оно депонируется в результате разрушения гемоглобина. | ||
| Щелочная фосфатаза | До 240 ед/л для женщин и до 270 ед/л для мужчин | При печеночной недостаточности наблюдается повышение активности щелочной фосфатазы в 3 – 10 раз из-за синдрома холестаза, внутренние оболочки желчевыводящих путей являются источником щелочной фосфатазы. | ||
| Аммиак крови | 11-32 мкмоль/л | При печеночной недостаточности содержание в крови азота аммиака увеличивается до 2 раз, с нарастанием печеночной энцефалопатии растет уровень аммиака. | ||
| Фибриноген | 2 – 4 г/л | Наблюдается снижение уровня фибриногена из-за нарушения его образования в печени. Фибриноген – фактор свертываемости крови, его недостаток в совокупности с недостатком других факторов приводит к развитию геморрагического синдрома. | ||
| Гемоглобин | 120 – 140 г/л | При печеночной недостаточности всегда происходит снижение гемоглобина менее 90 г/л. Это связано с нарушениями обмена белка и железа, а также наличием кровопотери при геморрагическом синдроме. | ||
| Лейкоциты | 4 – 9*10 9 /л | Повышение уровня лейкоцитов и СОЭ сопровождает интоксикационный синдром вследствие некроза печени или действия вирусных гепатитов, то есть, воспаления. | ||
| СОЭ (скорость оседания эритроцитов) | 2 – 15 мм/ч | |||
| Тромбоциты | 180 – 320*10 9 /л | Наблюдается снижение уровня тромбоцитов за счет повышенной в них потребности, в результате геморрагического синдрома. | ||
| Цвет | Соломенный, светло-желтый | Потемнение мочи, цвет темного пива связано с появлением в ней желчных пигментов, вследствие холестаза. | ||
| Уробилин | 5 – 10 мг/л | Повышение уровня уробилина в моче связано с синдромом холестаза и нарушением обмена желчных пигментов. | ||
| Белок | В норме в моче нет белка | Появление белка в моче связано с нарушением белкового обмена, может свидетельствовать о развитии почечной недостаточности. | ||
| Стеркобилин | В норме стеркобилин в кале есть, способствует окраске кала в желто-коричневые цвета. | Отсутствие стеркобилина в кале связано с нарушением оттока желчи. | ||
| Скрытая кровь | В норме скрытой крови в кале быть не должно | Появление скрытой крови в кале указывает на наличие кровотечений из расширенных вен пищевода или желудка. | ||
| Маркеры вирусного гепатита А: Ig M HAV; вирусного гепатита В: антитела к HBs-антигену; вирусного гепатита С: Anti-HCV | В норме у человека, не страдающего вирусными гепатитами, маркеры к гепатитам не выявляются. | Определение маркеров к вирусным гепатитам указывают на острый или хронический процесс. | ||
С помощью специальной аппаратуры можно визуализировать печень, оценить ее состояние, размеры, наличие в ней дополнительных образований, состояние сосудов печени, желчных протоков.
- Ультразвуковое исследование (УЗИ) брюшной полости.
УЗИ печени при печеночной недостаточности указывает на:
- изменение размеров печени: увеличение или уменьшение,
- изменение структуры: зернистость, наличие патологических включений,
- состояние желчной системы: сдавление желчных протоков, наличие камней в желчном пузыре и так далее,
- состояние кровеносных сосудов: сужение или их расширение, наличие анастомозов между портальной и нижней полой венами, их проходимость, при печеночной недостаточности можно выявить признаки портальной гипертензии (возможно при исследовании УЗИ Доплера).
Также оценивают состояние селезенки, при печеночной недостаточности часто увеличивается и этот орган.
- Компьютерная томография и магнитно-резонансная томография позволяют более детально оценить состояние печени и сосудов, чем УЗИ.
- Электроэнцефалография (ЭЭГ) – при недостаточности печени наблюдается замедление и уменьшение амплитуд ритма головного мозга. С тяжестью печеночной энцефалопатии и глубиной комы, эти показатели усугубляются.
- Радиоизотопное сканирование печени: в печеночные сосуды вводят контрастное вещество, затем оценивают накопление и распределение его в печеночной ткани. В разрушенных и цирротических тканях печени контраст накапливаться не будет. Также, с помощью данного метода можно оценить проходимость печеночных сосудов.
- Пункционная биопсия печени – инвазивный метод (хирургическое вмешательство). Проводят прокол в области печени и под контролем УЗИ забирают материал печеночной ткани. Далее полученный биоптат подвергают гистологическому и гистохимическому исследованию. С помощью данного метода можно точно определить причину, которая привела к развитию печеночной недостаточности. Гистологическая картина может быть очень разнообразной.
- Самое главное, при возможности, устранить возможную причину развития печеночной недостаточности.
- Лечение необходимо начать немедленно.
- Госпитализация обязательна! Острую печеночную недостаточность лечат только в условиях стационара, при выраженной энцефалопатии – в реанимационном отделении.
- Лечение направлено на поддержание состояния организма и обмена веществ.
- Если исключить причину развития недостаточности печени и в течение 10 дней полноценно поддерживать жизнеобеспечение больного, наступает регенерация гепатоцитов, что дает возможность больному выжить.
- Остановка кровотечений при наличии геморрагического синдрома:
- При необходимости хирургическое лечение, направленное на восстановление целостности сосудов
- Введение кровеостанавливающих препаратов: аминокапроновая кислота (этамзилат), витамин К (викасол), аскорбиновая кислота (витамин С), витамин Р (рутин), фибриноген и другие.
- При неэффективности данных мероприятий, возможно переливание препаратов донорской крови, а именно, тромбоцитарной массы и других факторов свертывания крови.
- Уменьшение интоксикации:
- очистка кишечника,
- безбелковая диета,
- введение препаратов, стимулирующие перистальтику кишечника (церукал, метаклопрамид и другие),
- вливание неогемадеза, реосорбилакта с целью детоксикации.
- Восстановление объема циркулирующей крови: внутривенное капельное введение физ. раствора, других солевых растворов под контролем объема выделенной мочи.
- Улучшение кровоснабжения печени:
- Кислородная маска или искусственная вентиляция легких при наличии симптомов отека легких,
- уменьшение отека печеночных клеток: введение осмотических препаратов (реополиглюкин, сорбитол),
- расширение внутрипеченочных сосудов: эуфиллин, дроперидол, тиотриазолин,
- препараты, улучшающие способностью печени воспринимать кислород: кокарбоксилаза, цитохром С и другие.
- Восполнение необходимых энергетических запасов организма: введение глюкозы, альбумина.
- Уменьшение всасываемости в кишечнике – лактулоза (дуфалак, нормазе и другие), назначение антибиотиков для нарушения кишечной микрофлоры.
- Восстановление функций печени и способствование ее регенерации:
- Аргинин, орнитин, Гепа-Мерц – улучшают функцию печени образования мочевины из аммиака,
- витамины Р, группы В,
- гепатопротекторы с фосфолипидами и жирными кислотами: эссенциале, ЛИВ-52, эссливер, липоид С и другие,
- аминокислоты, кроме фенилаланина, триптофана, метионина, тирозина.
- Коррекция работы головного мозга:
- седативные (успокоительные) препараты,
- улучшение кровообращения головного мозга (актовегин, церебролизин и другие),
- диуретики (мочегонные, например, лазикс, маннит) для уменьшения отека головного мозга.
| Вид препаратов | Представители | Механизм действия | Как применяется |
| Лактулоза | Дуфалак, Нормазе, Гудлак, Портолак | Лактулоза изменяет кислотность кишечника, тем самым угнетая патогенную микрофлору кишечника, выделяющая азот. Азот всасывается в кровь и, соединяясь с атомами водорода воды, образует аммиак. Поврежденная печень не способна образовывать из этого аммиака мочевину, происходит аммиачная интоксикация. | 30 – 50 мл 3 раза в сутки с едой. Лактулозу можно применять длительно. |
| Антибиотики широкого спектра действия | Неомицин наиболее хорошо себя зарекомендовал в лечении печеночной недостаточности. | Антибиотики необходимы для подавления кишечной микрофлоры, которая выделяет аммиак. Можно применять любые антибактериальные препараты, за исключением тех, которые оказывают гепато-токсическое влияние. | Таблетки 100 мг – по 1-2 таблетки 2 раза в сутки. Курс лечения 5-10 дней. |
| Аминокислоты | Глутаминовая кислота | Аминокислоты этих групп связывают аммиак в крови и выводят его из организма. Назначается при аммиачной интоксикации, развившейся в результате хронической печеночной недостаточности. Нельзя применять с викасолом (витамином К), который назначается для остановки кровотечений, например из расширенных вен пищевода. | Внутрь по 1 г 2-3 раза в сутки. Курс лечения длительный от 1 месяца до 1 года. |
| Орнитин (орницетил) | Внутрь гранулы по 3 г, развести в стакне жидкости 2-3 раза в сутки. Для внутривенного капельного введения – 20-40г/сутки на 500 мл глюкозы 5% или физиологического раствора. | ||
| Дезинтоксикационная инфузионная терапия | Глюкоза 5% | Глюкоза способствует восполнению необходимых энергетических запасов. | До 200 — 500 мл в сутки каждого из растворов внутривенно капельно. Всего растворов в сутки можно лить до 2 – 3 литров, только под контролем объема выделенной мочи (диуреза). |
| Раствор натрия хлорида 0,9% (физ. раствор), раствор Рингера, Лакт | Растворы электролитов восполняет объем циркулирующей крови, электролитный состав крови улучшая кровоснабжение печени. | ||
| Препараты калия | Калия хлорид | Восполняет недостаток калия, который практически всегда есть при печеночной недостаточности. Только под контролем уровня калия в крови, так как его избыток может привести к сердечной недостаточности. | 10 мл 4% раствора, разведенного в 200 мл любой жидкости для инфузии. |
| Витамины | Витамин С | Многие витамины являются антиоксидантами, улучшают состояние стенки сосудов, улучшают кровообращение, способствуют улучшению регенерации печеночных клеток. | До 5 мл в сутки внутримышечно или внутривенно. |
| Витамины группы В (В1, В6, В12) | По 1 мл в сутки внутримышечно или внутривенно с инфузионными растворами | ||
| Витамин РР (никотиновая кислота) | По 1 мл на 10 мл воды для инъекций внутривенно 1 раз в сутки. | ||
| Гепатопротекторы | Эссенциале форте | Содержит в себе фосфолипиды, витамины В1, В2, В6, В12, РР, пантотенат — вещество, способствующее выведению алкоголя. Фосфолипиды являются источником для строения гепатоцитов, улучшает их регенерацию. | Раствор для инъекций – по 5 мл 2-4 раза в сутки, разводить на физ. растворе или глюкозе. После 10 дней инъекций можно перейти на прием таблетированного эссенциале. Для приема внутрь: 1-й месяц – по 600 мг (2 капсулы по 300 мг) 2-3 раза в сутки с едой. Далее – по 300 мг (1 капсулу) 2-3 раза в сутки. Курс лечения – от 2-3 месяцев. |
| Гептрал | Содержит в себе аминокислоты, улучшающие регенерацию печени, способствуют обезвреживанию желчных кислот. | 1 таблетка на каждые 20 кг веса пациента утром между едой. |
Гемодиализ – очищение и фильтрация крови, через аппарат искусственной почки, также возможно через листок брюшины (брюшной гемодиализ). При этом кровь прогоняется через фильтры, освобождая ее от токсинов.
Плазмаферез – очистка крови от токсических веществ с помощью специальных фильтров, с последующим возвращением плазмы обратно в кровеносное русло. Именно плазмаферез лучше себя зарекомендовал при лечении печеночной недостаточности.
Показания:
- Развитие почечно-печеночной недостаточности, обычно это происходит на этапе печеночной комы;
- Фульминантная печеночная недостаточность, развивающаяся на фоне отравления ядами и токсинами;
- Острая и хроническая печеночная недостаточность при выраженной интоксикации аммиаком, желчными пигментами, желчными кислотами и другими токсическими веществами.
Пересаженная часть печени в организме реципиента (тот, которому пересадили орган) начинает постепенно регенерироваться до размеров здоровой печени. При этом гепатоциты начинают выполнять основные свои функции.
Опасностью данного метода является возможное отторжение пересаженного органа (чужеродного агента), поэтому больному в течение всей жизни придется принимать специальные препараты (цитостатики и гормоны).
Также проблемой в использовании данного метода в лечении печеночной недостаточности является его дороговизна и трудности в подборе максимально подходящего донора.
Осложнения состояния в виде геморрагического синдрома, легочно-сердечной недостаточности затрудняют подготовку такого пациента к тяжелой и длительной операции.
Показания:
- острая и фульминантная печеночная недостаточность,
- цирроз печени,
- врожденные патологии печени,
- дистрофии печени в терминальных стадиях,
- опухоли печени при невозможности сохранить орган частично,
- аутоиммунные гепатиты,
- альвеококкоз печени при распространенном ее поражении – паразитарное заболевания печени (альвеококк),
- некоторые другие состояния, необходимость в трансплантации определяется индивидуально.

Принципы диетотерапии при печеночной недостаточности:
- малобелковая, а лучше безбелковая диета;
- суточная калорийность еды не должна быть менее 1500 ккал;
- еда должна быть вкусной и выглядеть аппетитно, так как у больных наблюдается резкое снижение аппетита;
- кушать надо часто, дробно;
- пища должна содержать достаточное количество легкоусвояемых углеводов (мед, сахар, фрукты, овощи);
- еда должна содержать в себе большое количество витаминов и микроэлементов;
- необходимо получать повышенное количество клетчатки;
- ограничение жира необходимо только при наличии симптомов холестаза;
- после улучшения состояния больного можно восстановить обычный рацион, вводя белковые продукты постепенно (как детям прикорм), начиная с белка растительного происхождения (гречка, злаки, бобовые), затем молочные продукты и при хорошей переносимости белка – мясо;
- при развитии у пациента печеночной энцефалопатии с нарушением акта глотания или печеночной комы рекомендовано парентеральное питание (введение растворов аминокислот, углеводов, липопротеидов, витаминов, микроэлементов через вену).
Режим дня:
- необходимо отказаться от приема алкоголя и других гепато-токсических веществ (особенно, лекарственных препаратов без консультации врача),
- употреблять достаточное количество жидкости,
- отказаться от тяжелых физических нагрузок,
- высыпаться, наладить психологическое состояние,
- не допускать запоры, необходимо проведение очистительных клизм 2 раза в сутки,
- если позволяет состояние, больше находиться на свежем воздухе, избегая при этом открытых солнечных лучей.
Берегите свое здоровье!
источник

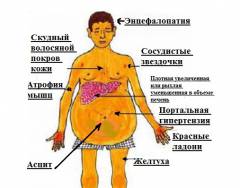
 УЗИ печени при печеночной недостаточности указывает на:
УЗИ печени при печеночной недостаточности указывает на: