Гормональная регуляция энергетического метаболизма
Действие гормонов, влияющих на энергетический метаболизм можно увидеть при определении некоторых биохимических показателей. Например, концентрации глюкозы в крови. Гормоны делят на:
1. Повышающие уровень глюкозы в крови;
2. Понижающие уровень глюкозы в крови.
Ко второй группе относится только ИНСУЛИН.
Также гормоны можно разделить на ГОРМОНЫ ПРЯМОГО ДЕЙСТВИЯ на энергетический метаболизм и ГОРМОНЫ КОСВЕННОГО ДЕЙСТВИЯ.
Основные механизмы действия инсулина:
1. Инсулин повышает проницаемость плазматических мембран для глюкозы. Этот эффект инсулина является главным лимитирующим звеном метаболизма углеводов в клетках.
2. Инсулин снимает тормозящее действие глюкокортикостероидов на гексокиназу.
3. На генетическом уровне инсулин стимулирует биосинтез ферментов метаболизма углеводов, в том числе ключевых ферментов.
4. Инсулин в клетках жировой ткани ингибирует триглицеридлипазу — ключевой фермент распада жиров.
Регуляция секреции инсулина в кровь происходит с участием нейро-рефлекторных механизмов. В стенках кровеносных сосудов есть особые хеморецепторы, чувствительные к глюкозе. Повышение концентрации глюкозы в крови вызывает рефлекторную секркцию инсулина в кровь, глюкоза проникает в клетки и ее концентрация в крови снижается.
Остальные гормоны вызывают повышение концентрации глюкозы в крови.
Относится к белково-пептидным гормонам. Обладает мембранным типом взаимодействия с клеткой-мишенью. Эффект оказывает через аденилатциклазную систему.
1. Вызывает повышение активности гликоген-фосфорилазы. В результате ускоряется распад гликогена. Так как глюкагон оказывает эффект только в печени то можно сказать, что он «гонит глюкозу из печени».
2. Понижает активность гликоген-синтетазы, замедляя синтез гликогена.
3. Активирует липазу в жировых депо.
Имеет рецепторы во многих тканях, а механизмы действия у него такие же, как у глюкагона.
1. Ускоряет распад гликогена.
2. Замедляет синтез гликогена.
Относятся к стероидным гормонам, поэтому обладают внутриклеточным типом взаимодействия с клеткой-мишенью. Проникая в клетку-мишень, они взаимодействуют с клеточным рецептором и обладают следующими эффектами:
1. Ингибируют гексокиназу — таким образом они замедляют утилизацию глюкозы. В результате концентрация глюкозы в крови возрастает.
2. Данные гормоны обеспечивают процесс гликонеогенеза субстратами.
3. На генетическом уровне усиливают биосинтез ферментов катаболизма белков.
Гормоны косвенного действия
1. Усиливает выделение глюкагона, поэтому наблюдается ускорение распада гликогена.
2. Вызывает активацию липолиза, поэтому способствует утилизации жира в качестве источника энергии.
ЙОДСОДЕРЖАЩИЕ ГОРМОНЫ ЩИТОВИДНОЙ ЖЕЛЕЗЫ.
Это гормоны — производные аминокислоты тирозина. Обладают внутриклеточным типом взаимодействия с клетками-мишенями. Рецептор Т3/Т4 находится в ядре клетки. Поэтому эти гормоны усиливают биосинтез белков на уровне транскрипции. Среди этих белков — окислительные ферменты, в частности разнообразные дегидрогеназы. Кроме того, они стимулируют синтез АТФаз, т.е. ферментов, которые разрушают АТФ. Для процессов биоокисления требуются субстраты — продукты окисления углеводов и жиров. Поэтому при увеличении продукции этих гормонов наблюдается усиление распада углеводов и жиров. Гиперфункция щитовидной железы называется Базедова болезнь или тиреотоксикоз. Один из симптомов этого заболевания — понижение массы тела. Для этого заболевания характерно повышение температуры тела. В опытах in vitro наблюдается разобщение митохондриального окисления и окислительного фосфорилирования при высоких дозах этих гормонов.
Регуляция углеводного обмена осуществляется при участии очень сложных механизмов, которые могут оказывать влияние на индуцирование или подавление синтеза различных ферментов углеводного обмена либо способствовать активации или торможению их действия. Инсулин, катехоламины, глюкагон, соматотропный и стероидные гормоны оказывают различное, но очень выраженное влияние на разные процессы углеводного обмена. Так, например, инсулин способствует накоплению в печени и мышцах гликогена, активируя фермент гликогенсинтетазу, и подавляет гликогенолиз и глюконеогенез. Антагонист инсулина — глюкагон стимулирует гликогенолиз. Адреналин, стимулируя действие аденилатциклазы, оказывает влияние на весь каскад реакций фосфоролиза. Гонадотропные гормоны активируют гликогенолиз в плаценте. Глюкокортикоидные гормоны стимулируют процесс глюконеогенеза. Соматотропный гормон оказывает влияние на активность ферментов пентозофосфатного пути и снижает утилизацию глюкозы периферическими тканями. В регуляции глюконеогенеза принимают участие ацетил-КоА и восстановленный никотинамидадениндинуклеотид. Повышение содержания жирных кислот в плазме крови тормозит активность ключевых ферментов гликолиза. В регуляции ферментативных реакций углеводного обмена важную цель играют ионы Са2+, непосредственно или при участии гормонов, часто в связи с особым Са2+-связывающим белком — кальмодулином. В регуляции активности многих ферментов большое значение имеют процессы их фосфорилирования — дефосфорилирования. В организме существует прямая связь между углеводным обменом и обменом белков, липидов и минеральных веществ.
Пути регуляции метаболизма углеводов крайне разнообразны. На любых уровнях организации живого организма обмен углеводов регулируется факторами, влияющими на активность ферментов, участвующих в реакциях углеводного обмена. К этим факторам относятся концентрация субстратов, содержание продуктов (метаболитов) отдельных реакций, кислородный режим, температура, проницаемость биологических мембран, концентрация коферментов, необходимых для отдельных реакций, и т.д
Современная схема пентозофосфатного пути окисления углеводов, отражающая его связь с гликолизом (по Херсу).
1 — транскетолаза; 2 — трансальдолаза; 3 — альдолаза; 4 — фосфофруктокиназа; 5 — фруктозо-1,6-бисфосфатаза; 6 — гексокиназа; 7 — глюкозофосфатизомераза; 8 — триозофосфатизомераза; 9 -глюкозо-6-фосфатдегидрогеназа; 10 — 6-фосфоглюконолактоназа; 11 — 6-фосфоглюконатдегид-рогеназа; 12 — изомераза; 13 — эпимераза; 14 — лактатдегидрогеназа.
Десять реакций гликолиза протекают в цитозоле.
Гликолитический путь играет двоякую роль: приводит к генерированию АТФ в результате распада глюкозы, и он же поставляет строительные блоки для синтеза клеточных компонентов. Реакции гликолитического пути в физиологических условиях легкообратимы, кроме реакций, катализируемых гексокиназой, фосфофруктокиназой и пируват-киназой. Фосфофруктокиназа – наиболее важный регуляторный элемент (фермент) в процессе гликолиза, ингибируется высокими концентрациями АТФ и цитрата и активируется АМФ.
Скорость цикла трикарбоновых кислот зависит от потребности в АТФ. Высокий энергетический заряд клетки понижает активность цитратсинтазы, изоцитратдегидрогеназы и α-кетоглутаратдегидрогеназы. Еще один важный регуляторный момент – необратимое образование ацетил-КоА из пи-рувата. В результате пентозофосфатного пути происходит генерирование НАДФН и рибозо-5-фосфата в цитозоле. НАДФН участвует в восстановительных биосинтезах, а рибозо-5-фосфат используется в синтезах РНК, ДНК и нуклеотидных коферментов.
Взаимодействие гликолитического и пентозофосфатного путей обеспечивает возможность постоянного приспособления концентраций НАДФН, АТФ и строительных блоков, например рибозо-5-фосфата и пирувата, для удовлетворения потребностей клеток.
Наконец, глюконеогенез и гликолиз регулируются реципрокно, так что, если активность одного из путей относительно понижается, то активность другого пути повышается.
У человека на всех стадиях синтеза и распада углеводов регуляция углеводного обмена осуществляется при участии ЦНС и гормонов.
Например, установлено, что концентрация глюкозы (норма 4,4 – 6,1 ммоль/л) в крови ниже 3,3–3,4 ммоль/л (60–70 мг/100 мл) приводит к рефлекторному возбуждению высших метаболических центров, расположенных в гипоталамусе. В регуляции углеводного обмена особая роль принадлежит высшему отделу ЦНС – коре большого мозга. Наряду с ЦНС важное влияние на содержание глюкозы оказывают гормональные факторы, т.е. регуляции уровня глюкозы в крови осуществляется ЦНС через ряд эндокринных желез .
Нормальный уровень глюкозы в крови составляет 3,5 – 5,55 ммоль.
Гипогликемия– это снижение уровня глюкозы в крови. Различают физиологическую и патологическую гипогликемию.
Причины физиологической гипогликемии:
1) физический труд (повышенные затраты)
2) беременность и лактация
Причины патологической гипогликемии:
1) нарушение депонирования глюкозы в печени
2) нарушение всасывания углеводов в ЖКТ
3) нарушение мобилизации гликогена
6) приём в– ганглиоблокаторов
Гипергликемия– это повышение уровня глюкозы в крови.
2) избыток контринсумерных гормонов, которые препятствуют утилизации глюкозы мышечной тканью и одновременно стимулируют глюконеогенез
5) расстройство мозгового кровообращения
6) заболевания печени воспалительного или дегенеративного характера
Уровень глюкозы в крови является одним из гомеостатических параметров. Регуляция уровня глюкозы в крови – это сложный комплекс механизмов, обеспечивающий постоянство энергетического гомеостаза для наиболее жизненно важных органов (мозг, эритроциты). Глюкоза – главный и едва не единственный субстрат энергетического обмена. Существует два механизма регуляции:
Постоянный (через гормональное влияние)
Срочный механизм срабатывает практически всегда при действии на организм любых экстремальных факторов. Он осуществляется по классической модели (через зрительный анализатор воспринимается информация об опасности. Возбуждение из одного очага в коре распространяется по всем зонам коры. Затем возбуждение передаётся на гипоталамус, где находится центр симпатической нервной системы. По спинному мозгу импульсы поступают в симпатический ствол и по постганглионарным волокнам к коре надпочечников. При этом происходит выброс адреналина, который запускает аденилатциклазный механизм мобилизации гликогена).
Срочный механизм поддерживает стабильную гликемию на протяжении 24 часов. В дальнейшем запас гликогена уменьшается и уже спустя 15 – 16 часов подключается постоянный механизм, в основе которого лежит глюконеогенез. После истощения запасов гликогена, возбуждённая кора продолжает посылать импульсы в гипоталамус. Отсюда выделяются либерины, которые с током крови заносятся переднюю долю гипофиза, которая, в свою очередь, синтезирует в кровоток СТГ, АКТГ, ТТГ, которые в свою очередь стимулируют выброс трийодтиронина и тиреотропина. Эти гормоны стимулируют липолиз. Тиреотропные гормоны активируют протеолиз, в результате чего образуются свободные аминокислоты, которые как и продукты липолиза используются как субстраты глюконеогенеза и цикла трикарбоновых кислот.
В ответ на повышение уровня глюкозы в крови, происходит выброс инсулина, однако вследствие того, что жирные кислоты и выделяемые гормоны выключают гликолиз в мышечной ткани, потребление глюкозы мышцами не происходит, вся глюкоза сохраняется для мозга и эритроцитов.
В условиях длительного воздействия отрицательных факторов на организм (постоянный стресс) может возникнуть дефицит инсулина, что является одной из причин сахарного диабета.
Повышение уровня глюкозы (гипергликемия):
Физиологический подъем уровня глюкозы – психоэмоциональный стресс, усиленная физическая нагрузка, «боязнь белого халата»);
Болезни поджелудочной железы, характеризующиеся стойким или временным снижением продукции инсулина (панкреатит, гемохроматоз, муковисцидоз, онкозаболевания железы)
Заболевания эндокринных органов (акромегалия и гигантизм, синдром Иценко-Кушинга, феохромацитома, тиреотоксикоз, соматостатинома)
Прием лекарственных препаратов: тиазиды, кофеин, эстрогены, глюкокортикостероиды.
Понижение уровня глюкозы (гипогликемия):
Длительное голодание, запой, усиленная физическая нагрузка, лихорадка;
Нарушение со стороны ЖКТ: перистальтическая дисфункция, мальабсорбция, гастроэнтеростома, постгастроэктомия;
Нарушения со стороны поджелудочной железы: онкозаболевания, дефицит глюкагона(поражение альфа-клеток островков Лангенгарска);
Нарушения со стороны эндокринных органов: адреногенитальный синдром, болезнь Аддисона, гипотиреоз, гипопитуитаризм;
Нарушение в ферментативной системе: гликогенозы, нарушение толерантности к фруктозе, галактоземия;
Нарушение печеночных функций: гепатиты различной этиологии, гемохроматоз, цирроз;
Онкозаболевания: печени, желудка, надпочечников, фибросаркома;
Прием лекарственных средств: анаболические стероиды, психоактивные вещества, неселективные бета-адреноблокаторы. Передозировка: салицилаты, алкоголь, мышьяк, хлороформ, антигистаминные препараты.
источник
Инсулин – гормон поджелудочной железы, снижающий уровень глюкозы крови. Он действует как ключ, «открывающий двери» для глюкозы внутрь клетки. Инсулин имеет важное значение для организма и ему посвящен отдельный раздел «Инсулин и его значение для организма».
Глюкагон, адреналин, кортизол, гормон роста – гормоны, повышающие уровень глюкозы крови. Подробней о каждом из них далее в статье.
У людей без сахарного диабета организм способен регулировать уровень глюкозы крови в узких пределах, примерно между 4 и 7 ммоль/л. Когда уровень глюкозы крови падает ниже 3,5 – 4,0 ммоль/л, человек чувствует себя плохо. Снижение уровня глюкозы крови влияет на все реакции, происходящие в организме, таким образом организм пытается сказать мозгу, что у него осталось мало глюкозы. Организм старается высвободить глюкозу из имеющихся у него источников, а также создать глюкозу из жиров и белков (схема 1).
Схема 1. Источник: Ragnar Hanas Type 1 Diabetes in Children and Adolescents
Мозг не может хранить глюкозу, поэтому он зависит от равномерной и непрерывной подачи глюкозы с током крови.
Мозг не может работать без адекватного снабжения его глюкозой.
Интересно, что мозгу не нужен инсулин для перемещения глюкозы внутрь клетки, он относится к «инсулиннезависимым» органам. На первый взгляд это может показаться нелогичным, однако, в ситуациях, когда в организме низкий уровень глюкозы, продукция инсулина останавливается, тем самым сохраняя глюкозу для наиболее важных органов, а именно для головного мозга. Но если организм и дальше не получит глюкозу (если человек голодает), то мозг адаптируется и будет использовать другой источник энергии, в основном кетоны.
Несмотря на то, что клетки головного мозга извлекают определенную энергию из кетонов, ее все равно меньше чем, когда они используют глюкозу.
С другой стороны, если у человека есть сахарный диабет и у него уровень глюкозы крови высокий, инсулиннезависимые клетки будут поглощать большое количество глюкозы, и в результате это приведет к их повреждению и, следовательно, нарушению функционирования органа в целом.
В то время как гормон инсулин снижает уровень глюкозы крови, группа гормонов (глюкагон, адреналин, кортизол, гормон роста) повышают его (схема 2). Низкий уровень глюкозы крови (гипогликемия) представляет собой серьезную угрозу для жизнедеятельности организма. Поэтому целая группа гормонов отвечает за повышение уровня глюкозы крови, также эта группа гормонов называется контринсулярными или контррегуляторными гормонами. А реакции организма, направленные на повышения уровня глюкозы крови, называются контррегуляторными реакциями. Помимо гормонов в контррегуляторных реакциях также участвует вегетативная нервная система.
Глюкагон — это гормон, вырабатываемый поджелудочной железой, а именно альфа-клетками островков Лангерганса.
1\AppData\Local\Temp\msohtmlclip1\01\clip_image001.png» />
Одной из функций печени является хранение глюкозы. Когда в крови много глюкозы, например, после приема пищи, глюкоза под воздействием инсулина заходит в клетки печени и хранится в них в виде гликогена. Как деньги, которые вы кладете на счет в банке, когда у вас их много (Рис.1).
Рис.1. Источник: Ragnar Hanas Type 1 Diabetes in Children and Adolescents
Когда уровень глюкозы крови снижается, например, через несколько часов после еды или ночью, то начинает действовать глюкагон. Он разрушает гликоген до глюкозы, которая затем поступает в кровь. Также и вы можете снять деньги в банке, если настали тяжелые времена (рис. 2).
Рис. 2. Источник: Ragnar Hanas Type 1 Diabetes in Children and Adolescents
В течение дня человек ощущает чувство голода с интервалами примерно в 4 часа, в то время как в ночное время организм может находиться без пищи 8-10 часов. Это происходит потому, что ночью гликоген из печени под воздействием гормонов глюкагона и адреналина разрушается до глюкозы, которая поступает в кровь.
Людям с сахарным диабетом важно помнить, что если у них не будет запаса гликогена в печени, то глюкагон ночью не сможет повысить уровень глюкозы крови, следовательно, случится гипогликемия. Такое может возникнуть если вы не съели достаточное количество углеводов при занятиях спортом, и вашему организму пришлось тратить свои запасы гликогена днем. Также отсроченные гипогликемии (гипогликемии ночью) наступают после употребления алкоголя, так как алкоголь нейтрализует действие глюкагона.
Исследования показывают, что при сахарном диабете 1 типа не только снижается функция бета-клеток (производство инсулина), но также изменяется функция альфа-клеток. Нарушается способность поджелудочной железы производить адекватное количество глюкагона в ответ на гипогликемию. То есть наступает дисбаланс между инсулином и глюкагоном. В свою очередь, это приводит к нарушению контррегуляторного ответа на гипогликемию.
Также у людей с сахарным диабетом не снижается производство глюкагона, когда повышается уровень глюкозы крови. Это происходит потому, что инъекции инсулина делаются в подкожно-жировую клетчатку и к тому времени, когда инсулин дойдет до альфа-клеток поджелудочной железы, его концентрация будет низкой, и он не сможет подавить продукцию глюкагона. Следовательно, в дополнение к глюкозе, полученной из еды, в крови будет глюкоза из печени, полученная при распаде гликогена до глюкозы под воздействием глюкагона.
В настоящее время проходят исследования помпы, содержащие резервуары с инсулином и с глюкагоном, чтобы еще более точно имитировать уровень глюкозы крови у людей без сахарного диабета. В большей степени этот метод используется в исследованиях по разработке искусственной поджелудочной железы. Но есть и свои трудности, так как человеку с сахарным диабетом приходится контролировать не только введение инсулина, но и введение глюкагона, то есть создается в два раза больше проблем. Что, в свою очередь, может привести к синдрому эмоционального выгорания, снижению качества жизни и ухудшению гликемического контроля.
Инъекции глюкагона – это хорошее средство для купирования тяжелых гипогликемий. Тяжелая гипогликемия — это гипогликемия, потребовавшая помощи другого лица, а именно, если человек с сахарным диабетом потерял сознание, у него судороги или он не способен выпить или съесть продукты необходимые для купирования гипогликемии. Всем людям с сахарным диабетом на инсулинотерапии, а также их родственникам и друзьям необходимо иметь при себе глюкагон и знать, как им пользоваться.
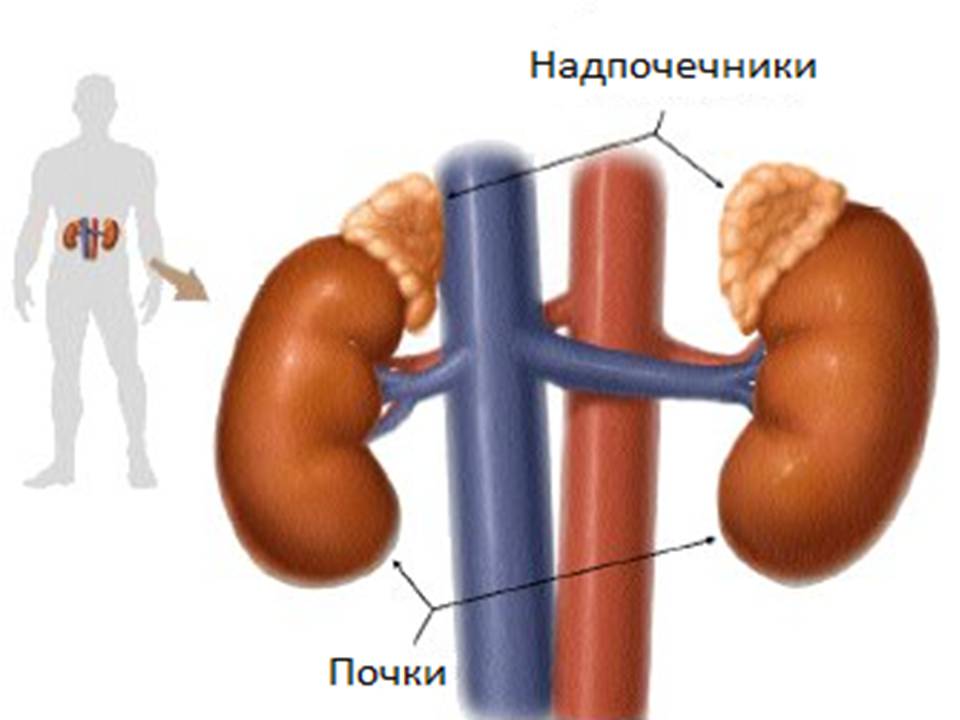
Адреналин — гормон стресса, выделяемый надпочечниками (Рис.3).
Рис.3. Анатомическое расположение надпочечников и почек.
Адреналин повышает уровень глюкозы крови, прежде всего, за счет разрушения гликогена в печени. Концентрация адреналина повышается, когда организм подвергается воздействию стресса, лихорадки или при ацидозе (например, при диабетическом кетоацидозе). Адреналин также снижает поглощение глюкозы клетками организма. Это может показаться вам странным, пока вы не вспомните, что все реакции организма при гипогликемии направлены на сохранение любой доступной глюкозы для мозга.
Человеческое тело изначально было создано для проживания в каменном веке. Если человек сталкивался с мамонтом или другим диким зверем, то у него оставалось два варианта бороться или бежать (рис 4). В обоих случаях дополнительное топливо, в виде глюкозы, было необходимо для организма. В нашем нынешнем образе жизни адреналин также выделяется, когда мы переживаем или испытываем страх. Но, по большей части, наши страхи вызваны пугающими новостями из телевизора или интернета, а они не требуют прилива дополнительной физической силы.
Рис. 4. Охота на оленя. Вальторта artyx.ru
У людей без сахарного диабета при возникновении стрессовой ситуации повышается продукция инсулина и уровень глюкозы остается в норме. А вот у людей с сахарным диабетом сложнее спрогнозировать реакцию уровня глюкозы крови на стресс. Так как у разных людей разный уровень стрессоустойчивости и в принципе разные обстоятельства вызывают страх. Следовательно, к коррекции доз инсулина надо подходить индивидуально.
Когда у человека с сахарным диабетом гипогликемия, то секреция адреналина может поднять уровень глюкозы крови, стимулируя распад гликогена в печени, но в тоже время адреналин вызывает повышенное потоотделение, беспокойство и сердцебиение, то есть симптомы гипогликемии.
Адреналин также стимулирует распад жиров до свободных жирных кислот, из которых могут создаваться кетоны в печени.
Кортизол является еще одним важным гормоном, который высвобождается надпочечниками (рис.3) в ответ на стресс и влияет на многие функции в организме, в том числе повышает уровень глюкозы крови.
Кортизол повышает уровень глюкозы крови путем синтеза глюкозы из белков (этот процесс называется глюконеогенез) и уменьшения поглощения глюкозы клетками организма. Кортизол также способствует расщеплению жиров до свободных жирных кислот, из которых могут создаваться кетоны.
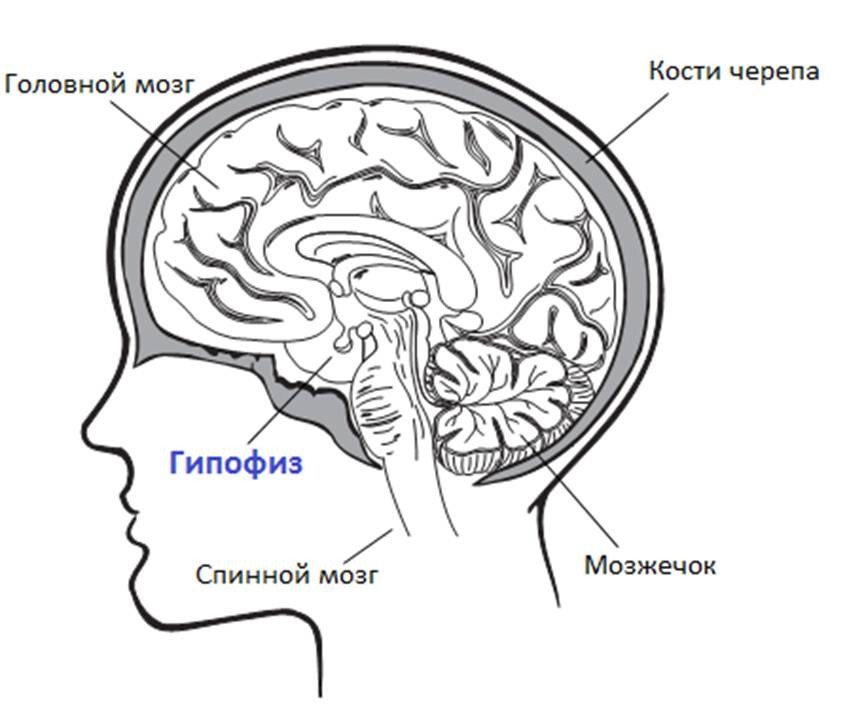
Гормон роста вырабатывается в гипофизе, который находится чуть ниже головного мозга (Рис. 5).
Рис.5. Источник: Ragnar Hanas Type 1 Diabetes in Children and Adolescents
Главной функцией гормона роста является стимуляция роста. Также он повышает уровень глюкозы крови путем снижения захвата глюкозы клетками организма. Гормон роста приводит к увеличению мышечной ткани и повышению распада жиров.
В период полового созревания, когда подростки быстро растут, у них вырабатывается большое количество гормона роста, следовательно, это приводит к повышению потребности в инсулине.
источник
Инсулин – гормон поджелудочной железы, снижающий уровень глюкозы крови. Он действует как ключ, «открывающий двери» для глюкозы внутрь клетки. Инсулин имеет важное значение для организма и ему посвящен отдельный раздел «Инсулин и его значение для организма».
Глюкагон, адреналин, кортизол, гормон роста – гормоны, повышающие уровень глюкозы крови. Подробней о каждом из них далее в статье.
У людей без сахарного диабета организм способен регулировать уровень глюкозы крови в узких пределах, примерно между 4 и 7 ммоль/л. Когда уровень глюкозы крови падает ниже 3,5 – 4,0 ммоль/л, человек чувствует себя плохо. Снижение уровня глюкозы крови влияет на все реакции, происходящие в организме, таким образом организм пытается сказать мозгу, что у него осталось мало глюкозы. Организм старается высвободить глюкозу из имеющихся у него источников, а также создать глюкозу из жиров и белков (схема 1).
Схема 1. Источник: Ragnar Hanas Type 1 Diabetes in Children and Adolescents
Мозг не может хранить глюкозу, поэтому он зависит от равномерной и непрерывной подачи глюкозы с током крови.
Мозг не может работать без адекватного снабжения его глюкозой.
Интересно, что мозгу не нужен инсулин для перемещения глюкозы внутрь клетки, он относится к «инсулиннезависимым» органам. На первый взгляд это может показаться нелогичным, однако, в ситуациях, когда в организме низкий уровень глюкозы, продукция инсулина останавливается, тем самым сохраняя глюкозу для наиболее важных органов, а именно для головного мозга. Но если организм и дальше не получит глюкозу (если человек голодает), то мозг адаптируется и будет использовать другой источник энергии, в основном кетоны.
Несмотря на то, что клетки головного мозга извлекают определенную энергию из кетонов, ее все равно меньше чем, когда они используют глюкозу.
С другой стороны, если у человека есть сахарный диабет и у него уровень глюкозы крови высокий, инсулиннезависимые клетки будут поглощать большое количество глюкозы, и в результате это приведет к их повреждению и, следовательно, нарушению функционирования органа в целом.
В то время как гормон инсулин снижает уровень глюкозы крови, группа гормонов (глюкагон, адреналин, кортизол, гормон роста) повышают его (схема 2). Низкий уровень глюкозы крови (гипогликемия) представляет собой серьезную угрозу для жизнедеятельности организма. Поэтому целая группа гормонов отвечает за повышение уровня глюкозы крови, также эта группа гормонов называется контринсулярными или контррегуляторными гормонами. А реакции организма, направленные на повышения уровня глюкозы крови, называются контррегуляторными реакциями. Помимо гормонов в контррегуляторных реакциях также участвует вегетативная нервная система.
Глюкагон — это гормон, вырабатываемый поджелудочной железой, а именно альфа-клетками островков Лангерганса.
1\AppData\Local\Temp\msohtmlclip1\01\clip_image001.png» />
Одной из функций печени является хранение глюкозы. Когда в крови много глюкозы, например, после приема пищи, глюкоза под воздействием инсулина заходит в клетки печени и хранится в них в виде гликогена. Как деньги, которые вы кладете на счет в банке, когда у вас их много (Рис.1).
Рис.1. Источник: Ragnar Hanas Type 1 Diabetes in Children and Adolescents
Когда уровень глюкозы крови снижается, например, через несколько часов после еды или ночью, то начинает действовать глюкагон. Он разрушает гликоген до глюкозы, которая затем поступает в кровь. Также и вы можете снять деньги в банке, если настали тяжелые времена (рис. 2).
Рис. 2. Источник: Ragnar Hanas Type 1 Diabetes in Children and Adolescents
В течение дня человек ощущает чувство голода с интервалами примерно в 4 часа, в то время как в ночное время организм может находиться без пищи 8-10 часов. Это происходит потому, что ночью гликоген из печени под воздействием гормонов глюкагона и адреналина разрушается до глюкозы, которая поступает в кровь.
Людям с сахарным диабетом важно помнить, что если у них не будет запаса гликогена в печени, то глюкагон ночью не сможет повысить уровень глюкозы крови, следовательно, случится гипогликемия. Такое может возникнуть если вы не съели достаточное количество углеводов при занятиях спортом, и вашему организму пришлось тратить свои запасы гликогена днем. Также отсроченные гипогликемии (гипогликемии ночью) наступают после употребления алкоголя, так как алкоголь нейтрализует действие глюкагона.
Исследования показывают, что при сахарном диабете 1 типа не только снижается функция бета-клеток (производство инсулина), но также изменяется функция альфа-клеток. Нарушается способность поджелудочной железы производить адекватное количество глюкагона в ответ на гипогликемию. То есть наступает дисбаланс между инсулином и глюкагоном. В свою очередь, это приводит к нарушению контррегуляторного ответа на гипогликемию.
Также у людей с сахарным диабетом не снижается производство глюкагона, когда повышается уровень глюкозы крови. Это происходит потому, что инъекции инсулина делаются в подкожно-жировую клетчатку и к тому времени, когда инсулин дойдет до альфа-клеток поджелудочной железы, его концентрация будет низкой, и он не сможет подавить продукцию глюкагона. Следовательно, в дополнение к глюкозе, полученной из еды, в крови будет глюкоза из печени, полученная при распаде гликогена до глюкозы под воздействием глюкагона.
В настоящее время проходят исследования помпы, содержащие резервуары с инсулином и с глюкагоном, чтобы еще более точно имитировать уровень глюкозы крови у людей без сахарного диабета. В большей степени этот метод используется в исследованиях по разработке искусственной поджелудочной железы. Но есть и свои трудности, так как человеку с сахарным диабетом приходится контролировать не только введение инсулина, но и введение глюкагона, то есть создается в два раза больше проблем. Что, в свою очередь, может привести к синдрому эмоционального выгорания, снижению качества жизни и ухудшению гликемического контроля.
Инъекции глюкагона – это хорошее средство для купирования тяжелых гипогликемий. Тяжелая гипогликемия — это гипогликемия, потребовавшая помощи другого лица, а именно, если человек с сахарным диабетом потерял сознание, у него судороги или он не способен выпить или съесть продукты необходимые для купирования гипогликемии. Всем людям с сахарным диабетом на инсулинотерапии, а также их родственникам и друзьям необходимо иметь при себе глюкагон и знать, как им пользоваться.
Адреналин — гормон стресса, выделяемый надпочечниками (Рис.3).
Рис.3. Анатомическое расположение надпочечников и почек.
Адреналин повышает уровень глюкозы крови, прежде всего, за счет разрушения гликогена в печени. Концентрация адреналина повышается, когда организм подвергается воздействию стресса, лихорадки или при ацидозе (например, при диабетическом кетоацидозе). Адреналин также снижает поглощение глюкозы клетками организма. Это может показаться вам странным, пока вы не вспомните, что все реакции организма при гипогликемии направлены на сохранение любой доступной глюкозы для мозга.
Человеческое тело изначально было создано для проживания в каменном веке. Если человек сталкивался с мамонтом или другим диким зверем, то у него оставалось два варианта бороться или бежать (рис 4). В обоих случаях дополнительное топливо, в виде глюкозы, было необходимо для организма. В нашем нынешнем образе жизни адреналин также выделяется, когда мы переживаем или испытываем страх. Но, по большей части, наши страхи вызваны пугающими новостями из телевизора или интернета, а они не требуют прилива дополнительной физической силы.
Рис. 4. Охота на оленя. Вальторта artyx.ru
У людей без сахарного диабета при возникновении стрессовой ситуации повышается продукция инсулина и уровень глюкозы остается в норме. А вот у людей с сахарным диабетом сложнее спрогнозировать реакцию уровня глюкозы крови на стресс. Так как у разных людей разный уровень стрессоустойчивости и в принципе разные обстоятельства вызывают страх. Следовательно, к коррекции доз инсулина надо подходить индивидуально.
Когда у человека с сахарным диабетом гипогликемия, то секреция адреналина может поднять уровень глюкозы крови, стимулируя распад гликогена в печени, но в тоже время адреналин вызывает повышенное потоотделение, беспокойство и сердцебиение, то есть симптомы гипогликемии.
Адреналин также стимулирует распад жиров до свободных жирных кислот, из которых могут создаваться кетоны в печени.
Кортизол является еще одним важным гормоном, который высвобождается надпочечниками (рис.3) в ответ на стресс и влияет на многие функции в организме, в том числе повышает уровень глюкозы крови.
Кортизол повышает уровень глюкозы крови путем синтеза глюкозы из белков (этот процесс называется глюконеогенез) и уменьшения поглощения глюкозы клетками организма. Кортизол также способствует расщеплению жиров до свободных жирных кислот, из которых могут создаваться кетоны.
Гормон роста вырабатывается в гипофизе, который находится чуть ниже головного мозга (Рис. 5).
Рис.5. Источник: Ragnar Hanas Type 1 Diabetes in Children and Adolescents
Главной функцией гормона роста является стимуляция роста. Также он повышает уровень глюкозы крови путем снижения захвата глюкозы клетками организма. Гормон роста приводит к увеличению мышечной ткани и повышению распада жиров.
В период полового созревания, когда подростки быстро растут, у них вырабатывается большое количество гормона роста, следовательно, это приводит к повышению потребности в инсулине.
У всех контринсулярных гормонов пик секреции приходится на предутренние часы. Таким образом у людей с сахарным диабетом 1 типа происходит повышение уровня глюкозы крови примерно с 3-4 до 7-8 часов утра, и они могут просыпаться утром с высоким уровнем глюкозы крови. Подробнее о феномене утренней зари здесь
Сахар — важнейший источник энергии для организма. Он изначально присутствует в крови в виде глюкозы. Жизненно необходимый уровень сахара в крови регулируется гормоном, вырабатываемымподжелудочной железой.
Глюкоза — простой сахар, который необходим для функции мозга, а также важнейший источник энергии для всего организма. Глюкоза хранится в организме в печени и мышцах в виде гликогена, который представляет собой длинную цепочку молекул сахара, и транспортируется по организму кровью. Существует естественный уровень глюкозы в крови. Но когда мы едим или, наоборот, питаемся недостаточно, этот уровень изменяется. Степень этого изменения регулируется гормонами поджелудочной железы (от греч. hormao — привожу в движение, побуждаю).
Поджелудочная железа
Поджелудочная железа, вытянутый белесоватый орган длиной около 20-25 см, расположена непосредственно за нижней частью желудка и соединена с двенадцатиперстной кишкой. Она вырабатывает ферменты, которые по протоку попадают в двенадцатиперстную кишку и участвуют в переваривании пищи. Но это не единственная ее функция. Пищеварительная часть поджелудочной железы составляет более 90 процентов ее массы. Около пяти процентов приходится на клетки, которые вырабатывают гормоны, регулирующие уровень сахара в крови: инсулин и глюкагон.
Эти «эндокринные» клетки, известные как островки Лангерганса, объединяются в группы, расположенные по всей массе поджелудочной железы. В отличие от большинства продуктов, вырабатываемых поджелудочной железой, гормоны не поступают в протоки, ведущие в двенадцатиперстную кишку. Они выделяются непосредственно в кровоток.
Существуют разные типы клеток поджелудочной железы, которые отвечают за выработку разных гормонов. Инсулин в норме выделяется бета-клетками островков поджелудочной железы. Небольшое количество гормона вырабатывается постоянно. Если уровень глюкозы в крови возрастает, метки начинают вырабатывать больше инсулина. Если уровень глюкозы в крови падает, выработка инсулина снижается. Инсулин действует на ряд клеток организма, включая мышечные клетки, эритроциты и жировые клетки. При повышении уровня инсулина эти клетки побуждаются к абсорбции большего количества глюкозы из крови и используют ее для выработки энергии. Количество инсулина контролируется другим гормоном поджелудочной — соматостатином. Он секретируется в ответ на высокий уровень некоторых гормонов, и его функция — подавлять их выработку, в том числе снижать уровень инсулина.
Глюкагон вырабатывается альфа-клетками островков Лангерганса. Эти клетки стимулируются к действию, когда уровень глюкозы в крови становится слишком низким. Гормон вызывает превращение гликогена, в основном содержащегося в печени, в глюкозу и выделение ее в кровь, а также побуждает печень, мышцы и другие клетки организма вырабатывать глюкозу из других веществ, например из белков.
Сахар крови
Идеальный уровень глюкозы в крови колеблется от 70 до 110 г на 100 мл. После еды уровень сахара на несколько часов возрастает, но в норме не должен превышать 180 мг.
Индивид с более высоким уровнем сахара квалифицируется как страдающий гипергликемией.
Состояние, при котором уровень сахара в крови 70 мг и ниже, описывается как гипогликемия.
Роль гормонов и витаминов в регуляции кальции-фосфорного обмена
Концентрация кальция внутри клеток зависит от его концентрации во внеклеточной жидкости. Пределы колебаний общей концентрации Са 2+ в плазме крови здоровых людей составляют 2,12-2,6 ммоль/л, или 9-11 мг/дл.
Основными регуляторами обмена Са 2+ в крови являются паратгормон, калыщтриол и каль-цитонин.
А. Паратгормон
Паратгормон (ПТГ) — одноцепочечный полипептид, состоящий из 84 аминокислотных остатков (около 9,5 кД), действие которого направлено на повышение концентрации ионов кальция и снижение концентрации фосфатов в плазме крови.ПТГ синтезируется в паращитовидных железах в виде предшественника — препрогормона, содержащего 115 аминокислотных остатков. Во время переноса в ЭР от препрогормона отщепляется сигнальный пептид, содержащий 25 аминокислотных остатков. Образующийся прогормон транспортируется в аппарат Гольджи, где происходит превращение предшественника в зрелый гормон, включающий 84 аминокислотных остатка
Роль паратгормона в регуляции обмена
кальция и фосфатов
Органы-мишенидля ПТГ — кости и почки. В клетках почек и костной ткани локализованы специфические рецепторы, которые взаимодействуют с паратгормоном, в результате чего инициируется каскад событий, приводящий к активации аденилатциклазы. Внутри клетки возрастает концентрация молекул цАМФ, действие которых стимулирует мобилизацию ионов кальция из внутриклеточных запасов. Ионы кальция активируют киназы, которые фосфорилируют особые белки, индуцирующие транскрипцию специфических генов.
В почках ПТГ стимулирует реабсорбцию кальция в дистальных извитых канальцах и тем самым снижает экскрецию кальция с мочой, уменьшает реабсорбцию фосфатов.
Кроме того, паратгормон индуцирует синтез кальцитриола (1,25(OH)2D3), который усиливает всасывание кальция в кишечнике.
Таким образом, паратгормон восстанавливает нормальный уровень ионов кальция во внеклеточной жидкости как путём прямого воздействия на кости и почки, так и действуя опосредованно (через стимуляцию синтеза кальцитриола) на слизистую оболочку кишечника, увеличивая в этом случае эффективность всасывания Са 2+ в кишечнике. Снижая реабсорбцию фосфатов из почек, паратгормон способствует уменьшению концентрации фосфатов во внеклеточной жидкости.
Б. Кальцитриол
Как и другие стероидные гормоны, кальцитриол синтезируется из холестерола. Действие гормона направлено на повышение концентрации кальция в плазме крови. Кальцитриол оказывает воздействие на тонкий кишечник, почки и кости. Подобно другим стероидным гормонам, кальцитриол связывается с внутриклеточным рецептором клетки-мишени. Образуется комплекс гормон-рецептор, который взаимодействует с хроматином и индуцирует транскрипцию структурных генов, в результате чего синтезируются белки, опосредующие действие кальцитриола. Так, например, в клетках кишечника кальцитриол индуцирует синтез Са 2+ -переносящих белков, которые обеспечивают всасывание ионов кальция и фосфатов из полости кишечника в эпителиальную клетку кишечника и далее транспорт из клетки в кровь, благодаря чему концентрация ионов кальция во внеклеточной жидкости поддерживается на уровне, необходимом для минерализации органического матрикса костной ткани. В почках кальцитриол стимулирует реабсорбцию ионов кальция и фосфатов. При недостатке кальцитриола нарушается образование аморфного фосфата кальция и кристаллов гидроксиапатитов в органическом матриксе костной ткани, что приводит к развитию рахита и остеомаляции. Обнаружено также, что при низкой концентрации ионов кальция кальцитриол способствует мобилизации кальция из костной ткани.
Дата добавления: 2018-02-18 ; просмотров: 1179 ; ЗАКАЗАТЬ РАБОТУ
У многих ли из вас было сильное желание что-нибудь съесть во время менструального цикла? Было ли у вас когда-нибудь сильное желание наесться шоколада за неделю до менструации? И когда были поздние ночные набеги за «дозами шоколада», чтобы помочь перенести подготовку к экзаменам, но только в том случае, если время усиленного и напряженного обучения падало на период за неделю до менструации! Что происходит с гормонами яичника, из-за которых мы теряем способность контролировать себя в еде во второй половине цикла и по мере приближения климактерического периода?
Инсулинорезистентность и синдром X
Инсулин — основной анаболический (укрепляющий ткани) гормон обмена веществ, контролирующий многие аспекты регулирования глюкозы, отложение жиров в организме и множество других функций. Вы умрете без достаточного количества инсулина, потому что инсулин необходим при доставке глюкозы из крови к клеткам, которые должны использовать ее как топливо для существования и для отложения глюкозы в жировых клетках в качестве триглицеридов при потреблении энергии в будущем. Но в отличие от анаболического действия тестостерона, используемого для строения мышц и костей, инсулин — анаболический гормон, накапливающий жир. Инсулин — это очень мощный источник образования жира (липогенез) и очень сильный ингибитор расщепления жира (липолиз). Инсулин действительно оказывает действие на увеличение соотношения жира и мышц, поэтому чем больше инсулиновой стимуляции, тем меньше мышечных клеток, сжигающих жир. Избыток инсулина — неизбежная расплата, если вы женщина и у вас проблемы с лишним весом.
Симптомы избыточного количества инсулина, появляющиеся в зрелом возрасте:
Обычно при повышении уровня глюкозы вырабатывается инсулин для способствования передвижению глюкозы из крови в мышцы или ее отложению. Считается, что уровень инсулина быстро падает до обычного после выполнения этой функции. Но по мере старения и отложения жиров в организме инсулиновые рецепторы действуют не так хорошо. Молекулы глюкозы больше не могут нормально связываться с этими рецепторами. Когда это происходит, уровень глюкозы остается высоким после еды, потому что инсулин хотя и существует, но не оказывает предполагаемого действия. Рецепторы мозга выявляют постоянный высокий уровень глюкозы, и мозг посылает сигналы поджелудочной железе для выброса большего количества инсулина, чтобы снизить уровень глюкозы. Кровь и клетки переполнены инсулином. Неожиданно, когда начинается действие инсулина, глюкоза быстро доставляется клеткам, и уровень глюкозы в крови становится низким.
Такая реакция называется «возвратная гипогликемия» (низкий уровень сахара в крови); когда это происходит, вы чувствуете сильный голод, также возможны плохое самочувствие, потливость, тошнота, головокружение, беспорядок в мыслях, сердцебиение и учащенный пульс. Вы можете проследить, как падение уровня сахара в крови способствует появлению сильного аппетита, а особенно желанию съесть сладкое. Однако, как только вы удовлетворяете его, все начинается заново. Быстро поднимается уровень глюкозы, что способствует появлению вялости и сонливости, вы не можете сосредоточиться. Затем, когда от избыточного количества инсулина быстро падает уровень глюкозы, вы чувствуете испарину, беспокойство, раздражительность или плаксивость. У женщин, приближающихся к климактерическому периоду, это состояние усугубляется гормональными изменениями менструального цикла. Если вы обратите внимание на то, как вы себя чувствуете, когда и что вы едите и какой у вас день цикла, можете начинать искать симптомы того, что у вас анормальная чувствительность к инсулину, это означает, что у вас развивается инсулинорезистентность. Объем талии больше 33 дюймов — это другой пример того, что у вас развивается инсулинорезистентность.
Инсулинорезистентность относится к такому состоянию, когда наблюдаются высокий уровень инсулина и глюкозы в крови и избыточное количество инсулина, способствующее отложению глюкозы в виде жира, вместо того чтобы сразу же ее использовать в качестве энергии. Поскольку инсулин не оказывает нужного действия для доставки постоянного запаса глюкозы функционирующим мышечным клеткам, создается впечатление, как если бы вы не получали достаточного количества пищи. Клетки не получают необходимого им топлива, поэтому вы постоянно получаете сигналы о голоде и больше едите, хотя в крови достаточно топлива (глюкозы). Это напоминает утечку газа. Хотя вы заполняете резервуар (питание), топливо не доходит до двигателя, чтобы он мог работать. Хуже всего, что жировые клетки также требуют больше пищи. Избыточное количество инсулина способствует отложению жиров в организме и является менее результативным при превращении этих жировых отложений в энергию для мышц и других тканей организма. Такая структура повторяется изо дня в день, вы становитесь полнее, хотя поглощаете меньше пищи.
Инсулинорезистентность также вызывает:
Довольно грустная картина. Благодаря такому поражающему действию на кровеносные сосуды можно понять, почему избыточное количество инсулина , особенно при очень низком содержании эстрадиола, считается фактором риска при развитии болезней сердца и ранних сердечных приступов.
Этот процесс способствует развитию синдрома X — тяжелого заболевания, связанного с нарушением обмена веществ, часто встречающегося у женщин. Он увеличивает вероятность ранних заболеваний сердца, диабета и смерти. «Смертельный квартет», который составляет синдром X — избыточное количество инсулина (инсулинорезистентность), тучность в средней части тела, повышенное кровяное давление, высокий уровень холестерина и/или высокое содержание триглицеридов. Синдром W — другое название, которое вы можете прочитать в газетах, обозначающее те же проблемы, чаще встречающиеся у женщин. Синдром W означает:
При оптимальном уровне эстрадиола существует меньшая вероятность появления проблем, связанных с инсулинорезистентностью, т. к. эстрадиол способствует улучшению реакции инсулина в клетках. Ho недостаток эстрадиола — не единственная проблема, при которой инсулин затрагивает функционирование яичников. Исследователи нашли рецепторы инсулина в яичнике. Действие инсулина на рецепторы яичника заключается в изменении ферментов яичника таким образом, что они вырабатывают больше андрогенов, а не поддерживают нормальный баланс эстрадиола-эстрона. Высокое содержание андрогенов сказывается на гормонах, регулирующих уровень глюкозы, и способствует большему вырабатыванию инсулина; высокий уровень инсулина стимулирует больше андрогенов, произведенных яичником. Получается замкнутый круг, а это способствует тому, что женщина становится полнее. Это главная причина заметного увеличения веса у молодых женщин.
Более мягкая форма этого дисбаланса встречается у женщин климактерического возраста, у которых ощущается недостаток эстрадиола и демаскизация действий андрогенов, дегидроэпиандростерона и тестостерона. По мере увеличения действия андрогенов вместо нормального баланса эстрадиола появляется большее количество жира вокруг талии и внутри брюшной полости (висцеральный жир), как у мужчин. Диеты с низким содержанием жира и высоким содержанием углеводов усугубляют эту проблему, способствуя вырабатыванию поджелудочной железой большого количества инсулина. Чрезмерное количество инсулина способствует отложению жира в брюшной полости. Соответственно излишек жира в брюшной полости способствует большей инсулинорезистентности. Мы становимся все полнее и полнее.
Существует четыре основных фактора, которые нужно уравновесить, чтобы предотвратить выработку избыточного количества инсулина, увеличение массы тела и возникновение диабета по мере старения. Вы прочитаете об этом в следующих главах. Вот несколько ключевых понятий, способствующих тому, чтобы вы сейчас задумались о том, как все это соотносится. Основные составляющие «Жизненного плана силы гормонов»:
Питание в разное время и прием большого количества пищи по вечерам способствуют вырабатыванию большего количества инсулина и жировых отложений. Еда с высоким содержанием углеводов увеличивает производство инсулина;
Упражнение действует, как «невидимый инсулин», облегчая доставку глюкозы к мышцам, снижая высокое содержание глюкозы в крови. Тренировка помогает решить проблему инсулинорезистентности, способствуя сжиганию жира для получения энергии и наращивания мышц, а это, в свою очередь, увеличивает скорость обмена веществ;
Он помогает наблюдать за тем, сколько жира в организме и в какой части тела он находится. Восстановление оптимального уровня эст-радиола, тестостерона и работы щитовидной железы способствует уменьшению инсулинорезистентности, увеличивает скорость обмена веществ и наращивает мышцы (в этом случае у вас есть силы, чтобы тренироваться!);
Теперь вы видите, как все это сочетается? Каждое из этих составляющих играет важную роль в контролировании гипогликемии, непереносимости глюкозы, инсулинорезистентности или диабета. «Жизненный план силы гормонов» продемонстрирует вам лучшее сочетание белков, углеводов и полезных видов жиров, чтобы выйти из инсулиновой ловушки, о которой вы прочитаете в главах 15 и 16.
Гипогликемия и непереносимость глюкозы
Гипогликемия — низкое содержание сахара в крови — обычно сопровождается проблемой регулирования нормального уровня глюкозы, состоянием, которое называется «непереносимость глюкозы». Оба эти нарушения обычно являются ранними фазами развития диабета. Диагноз «гипогликемия» ставится при уровне глюкозы в крови ниже 50 мг/дл, но у вас могут быть симптомы гипогликемии и при более высоком уровне глюкозы, если содержание глюкозы стремительно падает. Это похоже на противопожарное устройство у вас дома, которое не различает сильный дым, пожар и предполагаемый дым, возникающий, когда вы жарите мясо в духовке. Аварийная сигнализация включается в любом случае.
Поскольку глюкоза является необходимым топливом для клеток мозга, рецепторы мозга предназначены для того, чтобы предостерегать нас при малейшем признаке, когда содержание глюкозы является недостаточным, а именно — либо при падении уровня глюкозы, либо при действительно низком уровне. Вот почему диабетики иногда проверяют уровень сахара в крови при симптомах гипогликемии, но обнаруживают, что уровень высокий. Вероятно, у них произошло резкое падение глюкозы до критического уровня, которое вызывает сигнал тревоги в мозге, хотя в действительности уровень выше обычного. То же самое происходит, когда вы чувствуете симптомы гипогликемии после еды. Превышение выработки инсулина , вызванное приемом большого количества рафинированных углеводов, способствует резкому падению уровня глюкозы, даже если он не опускается ниже магической отметки 50, чтобы поставить диагноз гипогликемии. Ваш мозг и организм не читали определений из нашего учебника, но они знают, что им необходимо для функционирования!
Непереносимость глюкозы означает, что у вас склонность к колебанию между высоким уровнем сахара в крови после еды и резким падением или низким уровнем спустя 2-4 часа. Это признак того, что у вас начинаются проблемы с регулированием глюкозы при поддержании его на постоянном уровне. Это состояние должно стать причиной изменения режима питания. Иногда трудно осознать, что тот же механизм — резкое падение уровня глюкозы — может вызвать сильный голод, беспокойство и панику.
Если вы спросите врача, что с вами не так, вам шаблонно ответят, что у вас расстройство от волнения или вы переедаете от депрессии и вам необходимо лечение антидепрессантами. Многие врачи не осознают, что быстрое падение уровня глюкозы может вызвать гипогликемическую реакцию, даже если уровень глюкозы не опускается ниже 50. Поэтому если вам сказали, что у вас не может быть этих проблем, потому что уровень глюкозы «нормальный», это не всегда верно. У вас могут быть симптомы гипогликемии, когда уровень глюкозы быстро падает, даже если он не выходит за пределы «нормального». Эта проблема часто встречается при непереносимости глюкозы и инсулинорезистентноспи и может быть решена при изменении питания и восстановлении гормонального баланса, о чем мы скажем в дальнейшем.
Обследования для выявления инсулинорезинстентности
Существует несколько хороших способов определения инсулинорезистентности. Один из них — реакция инсулина на тест глюкозы. Он предполагает употребление определенного количества глюкозы, затем измерение уровня глюкозы и инсулина через интервалы в 6 часов, чтобы выяснить структуру падения и повышения их уровня в соответствии с симптомами, появляющимися при изменении уровня глюкозы и инсулина. Если в этом тесте не учитывается уровень инсулина, он называется «тест толерантности к глюкозе» (ТТГ). ТТГ свидетельствует о том, как ваш организм регулирует уровень глюкозы, но не выявляет инсулинорезистентность.
Когда уровень глюкозы слишком высок
Очень высокий уровень глюкозы или ее быстрый подъем вызывает нарушения в мозге: беспокойство, сонливость, головные боли, хаотичность мышления, малую активность или усталость и невозможность сосредоточиться. Другие симптомы высокого содержания глюкозы в крови — сильная жажда, частое мочеиспускание, «пелена» перед глазами, замедленное опорожнение кишечника (вызывает жгучую рефлекторную боль), инертный кишечник и т. д.
Когда уровень глюкозы выше 200, это состояние называется гипергликемией (высокое содержание глюкозы в крови). Со временем гипергликемия переходит в сахарный диабет.
КОГДА УРОВЕНЬ ГЛЮКОЗЫ СЛИШКОМ НИЗКИЙ ИЛИ ПАДАЕТ
источник